Clear Sky Science · de
Translationale Regulation durch oxidative Desulfurierung von tRNA-Modifikationen
Wie Zellen die Proteinproduktion unter Stress einstellen
Jede Zelle muss entscheiden, welche Proteine sie produziert, wie schnell das geschieht und wann sie die Produktion drosselt. Diese Studie beschreibt einen feinen chemischen Schalter an Transfer-RNA (tRNA)-Molekülen, der Zellen dabei hilft, die Proteinproduktion herunterzufahren, wenn die Umgebung oxidierender wird, etwa bei Entzündungen oder metabolischem Stress. Durch Beobachtungen dieses Schalters in Säugetierzellen und in Reagensglas-Systemen decken die Forschenden eine neue Weise auf, in der schädigungsähnliche Veränderungen an RNA als regulatives Signal dienen können.
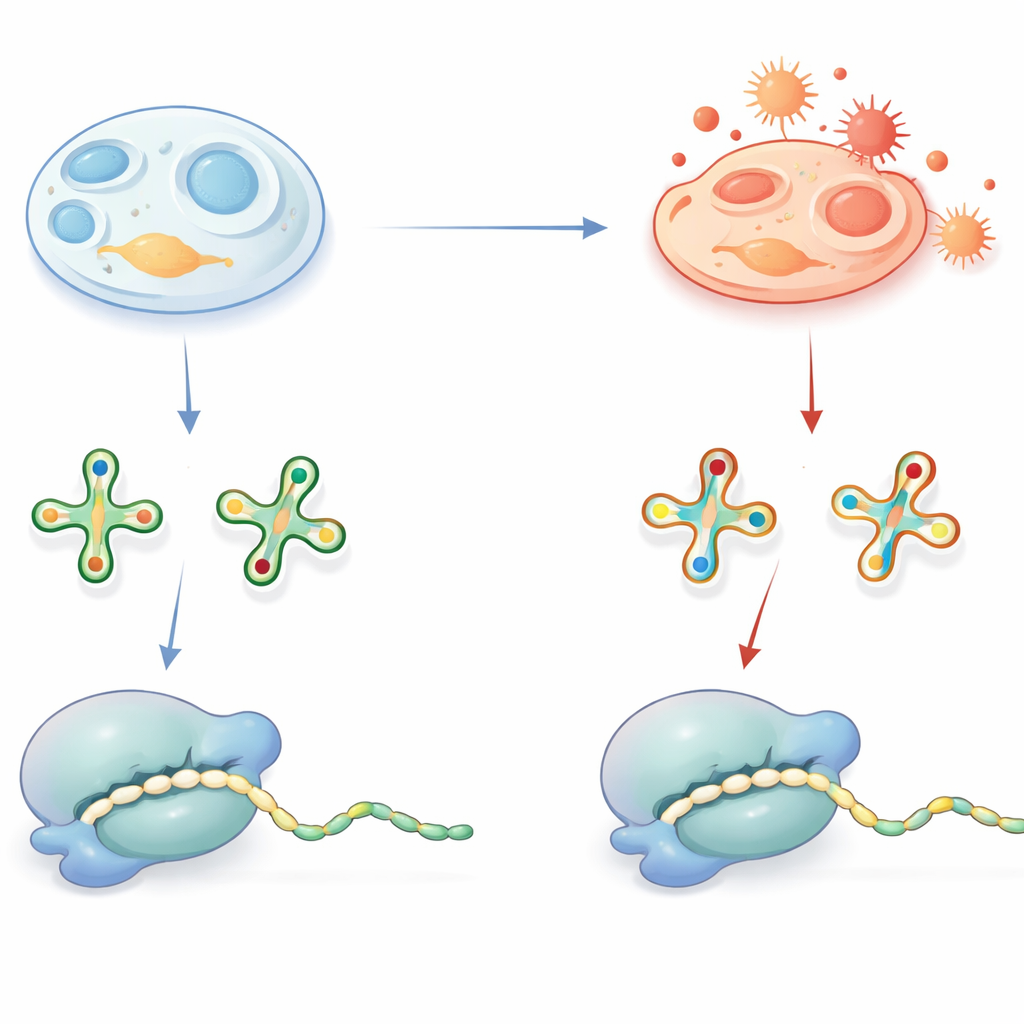
Kleine Kennzeichen auf tRNA mit großer Wirkung
tRNAs fungieren als Adapter, die drei-Buchstaben-“Wörter” in Boten-RNA lesen und die passenden Aminosäuren während der Proteinsynthese anliefern. Damit sie diese Aufgabe genau und effizient erfüllen, tragen viele tRNAs spezielle chemische Verzierungen, besonders an einer Schlüsselposition, die den dritten Buchstaben jedes Codons berührt. Eine weit verbreitete Modifikation ist eine schwefelhaltige Gruppe an einer Uridin-Basis, oft als 2-Thiouridin-Derivat bezeichnet. Unter gesunden Bedingungen hilft diese Schwefelgruppe der tRNA, die richtigen Codons mit endendem A oder G zu erkennen, und unterstützt eine schnelle, fehlerarme Translation. Defekte in diesen Modifikationen sind bereits als Ursache menschlicher Erkrankungen bekannt, was ihre Bedeutung unterstreicht.
Wenn oxidativer Stress die tRNA umschreibt
Die schwefelhaltige Gruppe, die das Decodieren fördert, hat einen Nachteil: sie ist chemisch anfällig für Oxidation. Das Team fragte, ob diese Gruppe in der Zelle unter oxidativen Bedingungen tatsächlich entfernt wird und welche Folgen das für die Proteinsynthese hätte. Mit empfindlicher Massenspektrometrie identifizierten sie oxidierte, schwefelfreie Varianten dieser tRNA-Basen — sogenannte h2U-Derivate — in Mausgeweben, Schweinemitochondrien, Bakterien, Hefen und verschiedenen menschlichen Zelllinien. Ein cleveres Spike-in-Experiment mit einem bakteriellen tRNA-Tracer zeigte, dass diese h2U-Marker nicht während der Probenaufbereitung entstehen, sondern im lebenden Zellmilieu gebildet werden. Obwohl die oxidierten Varianten nur in einem Bruchteil der tRNAs vorhanden waren, variierte ihre Häufigkeit zwischen Geweben und Zelltypen, was darauf hindeutet, dass der redoxische Zustand der Zelle und ihre antioxidative Kapazität beeinflussen, wie oft diese Umwandlung stattfindet.
Wie oxidierte tRNAs die Produktionslinie verlangsamen
Die Forschenden prüften anschließend, wie sich diese veränderten tRNAs während der Proteinsynthese verhalten. Sie wandelten die schwefelhaltige Form chemisch in die oxidierte h2U-Form in Gesamt-tRNA um und nutzten ein vollständig rekonstituiertes humanes Translationssystem in vitro. Ein Reporterin-Protein, dessen Produktion stark von diesen modifizierten tRNAs abhängt, zeigte bei desulfurisierten tRNAs eine deutlich reduzierte Ausbeute, während ein Kontrollreporter, der die betroffenen Codons vermeidet, normal übersetzt wurde. Biochemische Tests zeigten warum: oxidierte tRNAs für Lysin, Glutamin und Glutamat wurden deutlich schlechter mit ihren Aminosäuren beladen, wohingegen die entsprechenden Arginin-tRNAs weitgehend verschont blieben. Wichtig ist, dass h2U-tragende tRNAs dennoch in ribosomgebundenen (polysomalen) Fraktionen aus Zellen nachweisbar waren, was darauf hindeutet, dass sie zwar an der Translation teilnehmen, dies aber ineffizient tun.
Eine strukturelle Sicht auf geschwächtes Decodieren
Um genau zu sehen, wie Oxidation das Decodieren verändert, nutzte das Team kryogene Elektronenmikroskopie mit hoher Auflösung, um bakterielle Ribosomen zu beobachten, die mit humaner Lysin-tRNA und spezifischen Codons programmiert waren. Im normalen, schwefelhaltigen Zustand bildete die modifizierte Base an der tRNA-“Wobble”-Position entweder ein Standard-Basenpaar mit einem auf A endenden Codon oder ein spezielles Wobble-Paar mit einem auf G endenden Codon, beide fest im Decodierzentrum des Ribosoms verankert. Nach der Desulfurierung konnte die gleiche Base nur noch eine einzelne schwache Kontaktstelle mit dem A-endenden Codon ausbilden und bildete ein weniger stabiles Wobble-Paar mit dem G-endenden Codon. Bindungsexperimente stimmten mit diesen Strukturen überein: oxidierte Lysin-tRNA verlor praktisch die Fähigkeit, das AAA-Codon zu erkennen, und erkannte das AAG-Codon deutlich weniger effizient. Zusammengenommen zeigen diese Befunde, dass eine scheinbar kleine chemische Änderung zu codonspezifischen Verlangsamungen in der Proteinsynthese führen kann.
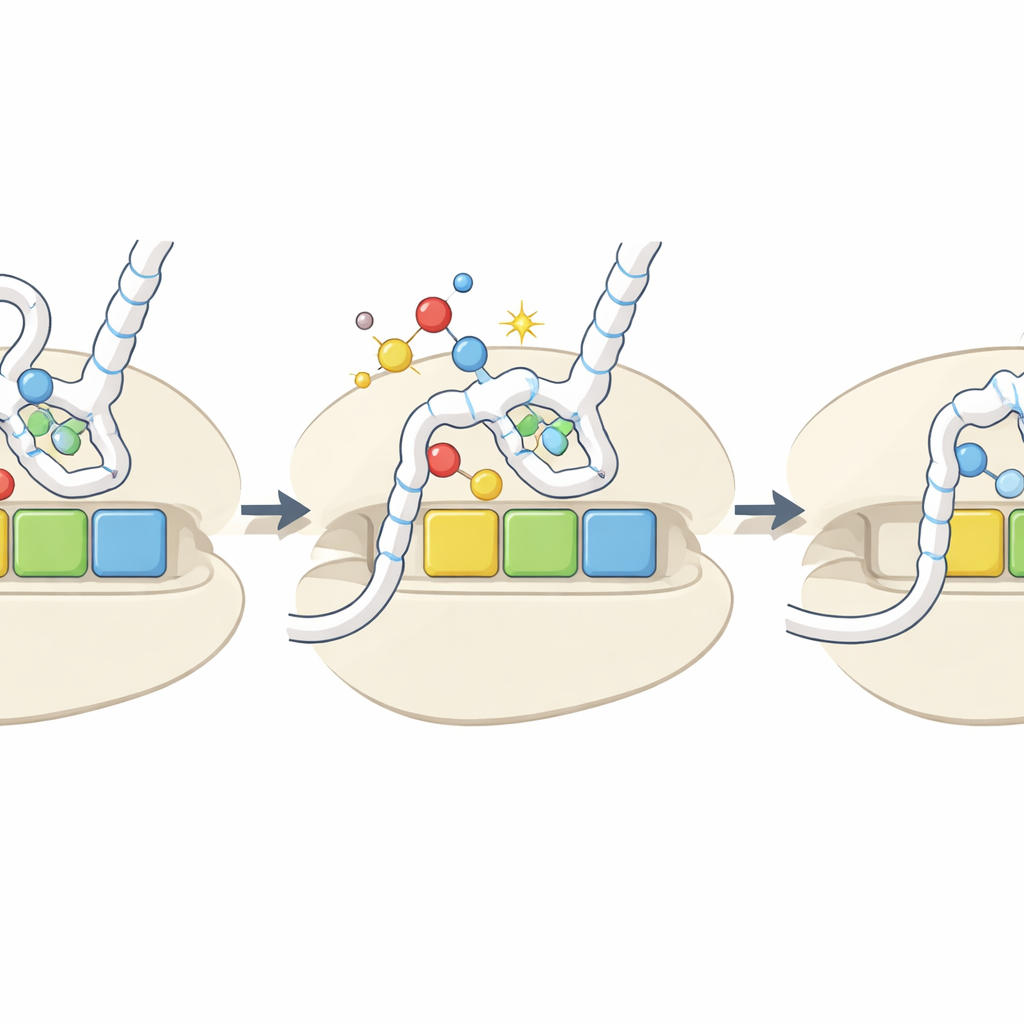
Ein Schadenssignal, das zum Regulierungsrad wird
Insgesamt schlägt die Studie vor, dass die oxidative Entfernung von Schwefel aus Schlüsselbasen der tRNA als eingebauter Sensor für das redoxische Milieu der Zelle fungiert. Unter oxidativem Stress werden mehr tRNAs in die h2U-Form umgewandelt, die schlecht beladen sind und schwach an bestimmte Codons binden. Dies verlangsamt gezielt die Translation an diesen Codons, kann die Stabilität betroffener mRNAs verändern, die Proteinfaltung beeinflussen und Stressantwortwege auslösen, wenn Ribosomen ins Stocken geraten. Obwohl die oxidierten Marker relativ selten sind und ihre Mengen nicht immer unter experimentellem Stress stark ansteigen, bedeuten ihre codon- und aminosäurespezifischen Effekte, dass bereits moderate Änderungen die Zusammensetzung und Geschwindigkeit der Proteinproduktion unter belastenden Bedingungen neu gestalten können.
Zitation: Mo, Y., Ishiguro, K., Miyauchi, K. et al. Translational regulation by oxidative desulfuration of tRNA modifications. Nat Commun 17, 2125 (2026). https://doi.org/10.1038/s41467-026-70126-7
Schlüsselwörter: tRNA-Modifikation, oxidativer Stress, Proteinsynthese, Translationsregulation, RNA-Schädigung