Clear Sky Science · de
Die Nutzung von tRNA-abhängigem Tyrosin gezielt stören deckt eine metabolische Verwundbarkeit im hepatozellulären Karzinom auf
Krebszellen ein häufiges Baustein entziehen
Leberkrebszellen, wie alle schnell teilenden Zellen, benötigen eine ständige Zufuhr von Aminosäuren – den winzigen Bausteinen von Proteinen. Diese Studie zeigt, dass das hepatozelluläre Karzinom, die häufigste Form von Leberkrebs, eine unerwartete Schwachstelle hat: Es ist stark abhängig von der Aminosäure Tyrosin sowohl für die Energieerzeugung als auch für das Überleben. Durch selektive Einschränkung, wie Krebszellen Tyrosin verwenden, konnten die Forscher das Tumorwachstum verlangsamen, die Kraftwerke der Krebszellen schädigen und eine Form des Zelltods auslösen, die für neue Therapien nutzbar sein könnte.
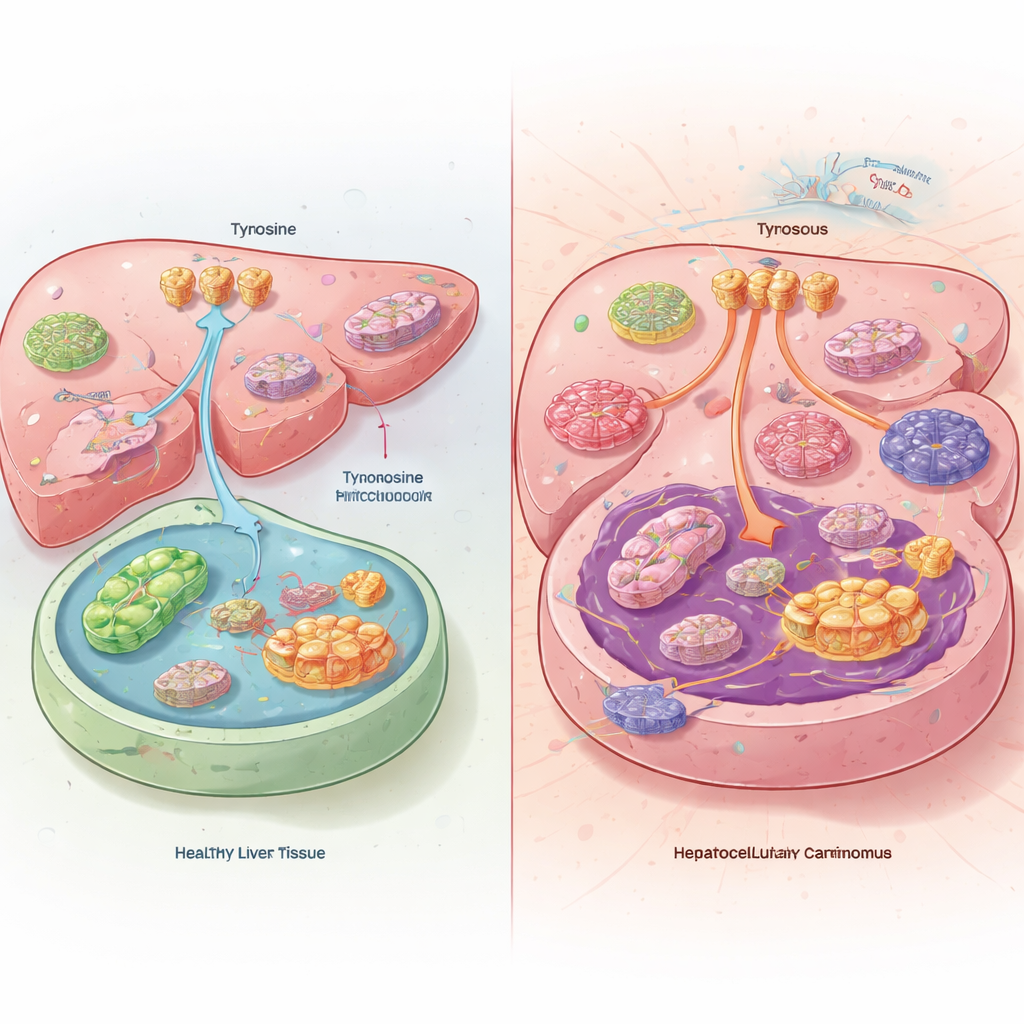
Ein verstecktes Ungleichgewicht in Lebertumoren
Als das Team Lebertumoren mit gesundem Lebergewebe von Patienten und Mäusen verglich, entdeckten sie etwas Rätselhaftes. Innerhalb der Krebszellen waren die Tyrosinspiegel tatsächlich niedrig, obwohl die Tumore mehr Tyrosin aus dem Blut aufnahmen und weniger davon abbauten. Anstatt Tyrosin als Brennstoff zu verwerten, leiteten die Lebertumore es in die Proteinproduktion um. Die Tumore erreichten dies, indem sie die Aktivität von Tyrosintransportern an der Zelloberfläche erhöhten und die Enzyme herunterfuhren, die Tyrosin normalerweise in der Leber abbauen. Mäuse, die eine tyrosinfreie Diät erhielten, entwickelten kleinere Tumore und lebten länger, während zusätzliches Tyrosin in der Nahrung das Tumorwachstum beschleunigte.
Wie Krebs die Proteinsynthese umprogrammiert
Die Forscher verfolgten diesen Tyrosin-Hunger bis zu einem starken krebsfördernden Gen namens MYC. In Lebertumoren schaltet MYC ein Protein namens YARS1 ein, das Tyrosin an eine spezifische Transfer-RNA (tRNA-TyrGUA) anhängt. Diese beladene tRNA benötigen Ribosomen, um tyrosinreiche Proteine zu bauen. Die Studie zeigte, dass Leberkrebse sowohl YARS1 als auch die passende tRNA hochregulieren und damit eine privilegierte Pipeline von Tyrosin in die Proteinsynthese sicherstellen. Die Störung dieser Pipeline – sei es durch Senkung der Tyrosinspiegel, Herunterregeln von YARS1 oder tRNA-TyrGUA oder durch Blockade der Tyrosin-Beladung – machte Leberkrebszellen in Zellkulturen und in Mäusen deutlich weniger widerstandsfähig und offenbarte eine metabolische Verwundbarkeit, die eng mit ihrem hohen Bedarf an Proteinproduktion verknüpft ist.
Die Kraftwerke und das Lipidgleichgewicht schwächen
Durch die Kombination genomweiter Messungen von RNA, Proteinsynthese und Metaboliten identifizierte das Team zwei besonders empfindliche Ziele der Tyrosin-Restriktion. Zum einen NDUFB8, ein Bestandteil des mitochondrialen Komplex I, ein Kernbestandteil der zellulären Energieerzeugung. Zum anderen SCD1, das hilft, gesättigte Fette in einfach ungesättigte Fette umzuwandeln, die sicherer in Membranen und Fetttröpfchen gespeichert werden können. Wenn Tyrosin für die Translation eingeschränkt wurde, sank die Produktion von NDUFB8 und SCD1, während deren RNA-Spiegel weitgehend unverändert blieben – ein klares Indiz dafür, dass die Translation und nicht die Genexpression betroffen war. Dies führte zu schlecht zusammengesetztem Komplex I, verringerter Zellatmung, vermehrten reaktiven Sauerstoffspezies und einer Verschiebung der Fette von einfach ungesättigten hin zu empfindlicheren mehrfach ungesättigten Formen, die leicht oxidierbar sind.
Krebszellen in einen eisenabhängigen Tod zwingen
Die kombinierte mitochondriale Schädigung und die instabilen Lipide trieben Leberkrebszellen in Richtung Ferroptose, eine eisenabhängige Form des Zelltods, die durch Lipidperoxidation ausgelöst wird. Die Tumore versuchten gegenzusteuern, indem sie natürliche Ferroptose-Blocker wie GPX4 und verwandte Moleküle hochfuhren, aber ein großes CRISPR-Gen-Editing-Screen zeigte, dass das Abschalten dieser Schutzfaktoren die Tyrosin-Restriktion noch tödlicher machte. In Zell- und Mausmodellen erzeugte die Kombination von Tyrosin-Einschränkungsstrategien mit Wirkstoffen, die GPX4 oder BCL2 hemmen – oder mit bereits zugelassenen Leberkrebsmedikamenten wie Sorafenib und Venetoclax – eine stärkere Tumorkontrolle, geringere Tumorlasten und längeres Überleben.
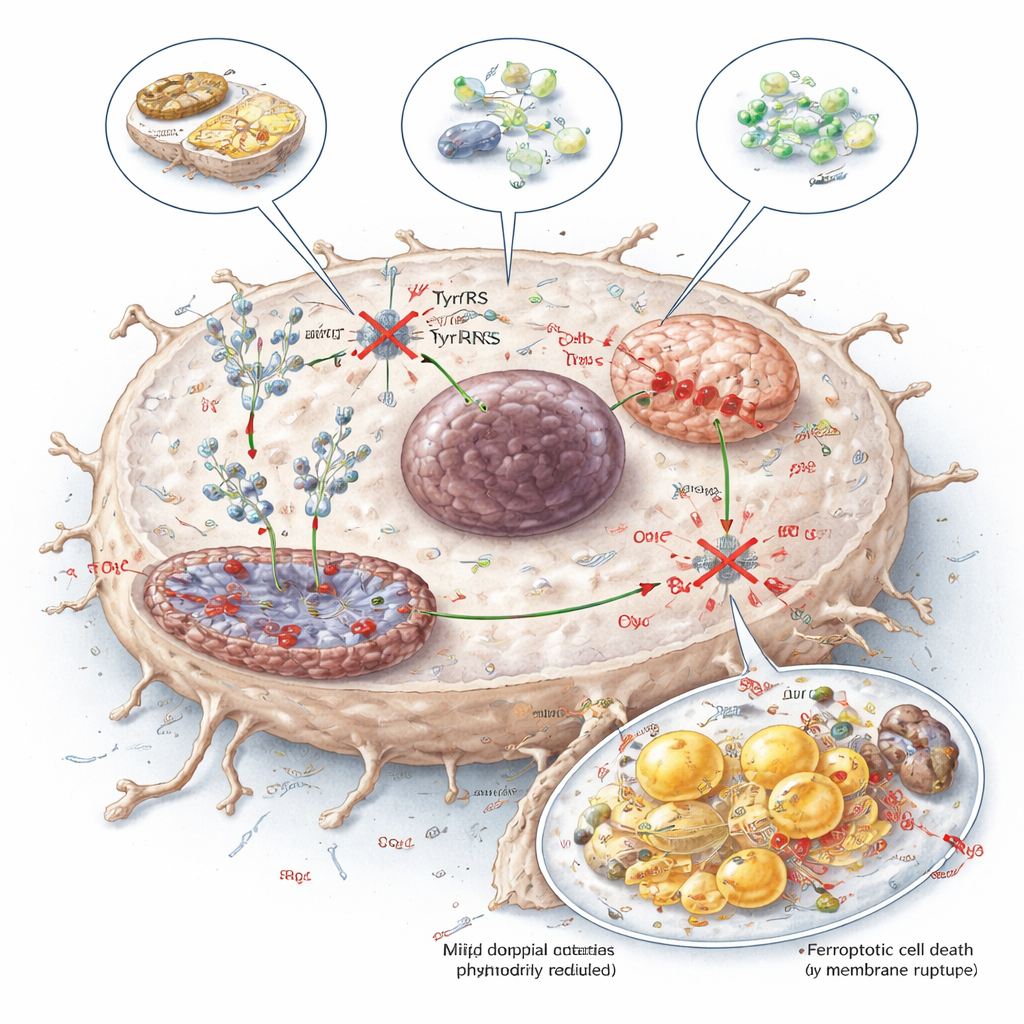
Aus einer metabolischen Schwäche eine Therapie machen
Um praktische Wege zur Ausnutzung dieser Schwäche zu untersuchen, testeten die Forscher drei Ansätze: eine tyrosinreduzierte Diät, ein Enzym (TAL), das Tyrosin enzymatisch abbaut, und ein kleines Molekül namens Tyrosinol, das mit Tyrosin um die Bindung an YARS1 konkurriert. Alle drei verringerten die Verfügbarkeit von Tyrosin für die Proteinsynthese, senkten NDUFB8- und SCD1-Spiegel, schädigten die mitochondriale Funktion und erhöhten die Ferroptose in Lebertumoren, während sie in Mäusen nur handhabbare Effekte in normalen Geweben zeigten. Für Laien lautet die Botschaft: Leberkrebse scheinen nicht nur aus Nährstoffgründen an Tyrosin gebunden zu sein, sondern nutzen es gezielt als Treibstoff für ihre Proteinproduktionsmaschinerie. Das Angehen dieser Abhängigkeit – durch Diät, Enzyme oder Medikamente – bietet einen vielversprechenden neuen Weg, Tumore zu schwächen und die Wirkung bestehender Therapien zu verstärken.
Zitation: Zhang, H., Wang, Z., Zhao, Y. et al. Targeting tRNA-dependent tyrosine usage unveils a metabolic vulnerability in hepatocellular carcinoma. Nat Commun 17, 2244 (2026). https://doi.org/10.1038/s41467-026-70112-z
Schlüsselwörter: Leberkrebs, Aminosäurestoffwechsel, Tyrosin, Mitochondrien, Ferroptose