Clear Sky Science · de
Systematische Identifizierung variantspezifischer RNA‑Struktur–Kleinstmolekül‑Interaktionen am Beispiel von RNA‑G‑Quadruplexen
Warum winzige Veränderungen in RNA für künftige Medikamente wichtig sind
Die meisten von uns erben kleine Unterschiede in unserer DNA, die uns einzigartig machen. Diese winzigen Änderungen können die Faltung von RNA‑Molekülen in unseren Zellen subtil umformen. Die neue Studie stellt eine Methode vor, mit der sich zeigen lässt, wie solche genetischen Feinheiten den Halt experimenteller Wirkstoffe, die auf RNA abzielen, verändern. Das ist wichtig, weil dasselbe Medikament bei verschiedenen Personen — insbesondere bei Krebs- oder Erbkrankheiten — sehr unterschiedlich wirken kann.
Neue Methode, um zu sehen, wo Medikamente RNA berühren
Viele Arzneimittelentwickler betrachten inzwischen RNA und nicht nur Proteine als Therapieziele. Kleinstmoleküle können an spezielle RNA‑Formen andocken und beeinflussen, wie Gene abgelesen werden. Bisher funktionierten die meisten Methoden jedoch nur für eine einzelne „Referenz“‑RNA‑Sequenz und vernachlässigten die zahllosen einzelbuchstabigen Varianten, die bei realen Patienten vorkommen. Die Autoren entwickelten einen Hochdurchsatzansatz namens BIVID‑MaP, mit dem sich gleichzeitig Tausende RNA‑Varianten testen lassen und für jede Variante die Bindungsstelle eines Kleinstmoleküls bis auf Einzel‑Nukleotid‑Auflösung bestimmt werden kann. 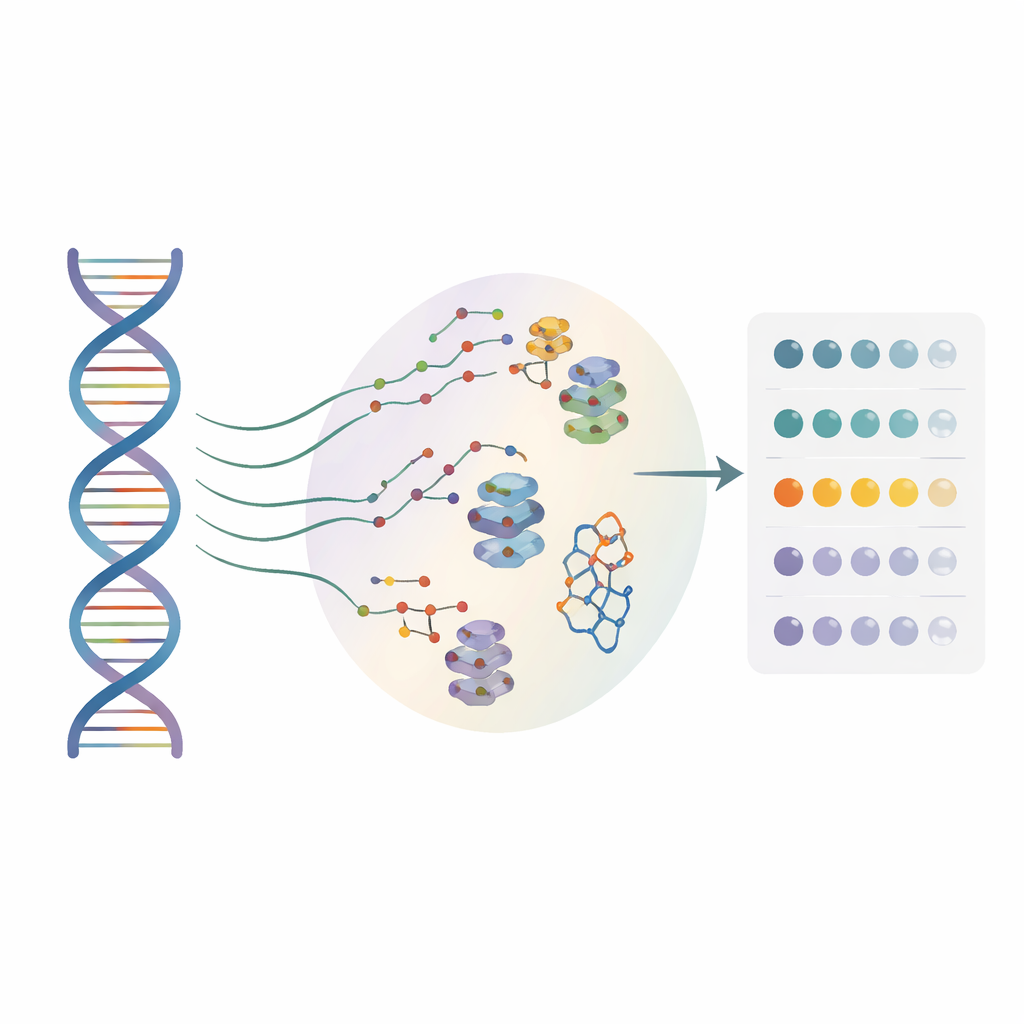
Chemische Markierungen in ein lesbares Signal verwandeln
BIVID‑MaP funktioniert in drei Hauptschritten. Zunächst koppelt das Team eine reaktive Kennzeichnung an ein RNA‑bindendes Kleinstmolekül. Sobald sich die markierte Verbindung in eine bevorzugte RNA‑Struktur einlagert — etwa ein kompaktes G‑Quadruplex, das sich aus guaninreichen Abschnitten bildet — geht die Markierung eine dauerhafte chemische Bindung mit einer benachbarten RNA‑Base ein. Zweitens kopiert ein spezielles Enzym die modifizierte RNA in DNA. Trifft es auf eine solche chemische Markierung, neigt es dazu, ein einzelnes Nukleotid zu „überspringen“ und erzeugt so eine winzige Deletion in der Kopie. Drittens liest Deep‑Sequencing diese Deletionssignaturen über Millionen Moleküle aus. Weil der Großteil der umgebenden Sequenz erhalten bleibt, lassen sich die Deletionen in einer Gemengelage präzise bestimmten genetischen Varianten zuordnen.
Validierung der Methode an einem kontrollierten Testfall
Um zu bestätigen, dass BIVID‑MaP tatsächlich variantspezifische Bindung detektiert, untersuchten die Forschenden ein RNA‑Segment aus dem CD44‑Gen, das normalerweise ein G‑Quadruplex bildet. Eine einzelne G‑zu‑A‑Änderung zerstört diese Struktur. In einer Mischung mit beiden Versionen zeigte nur die intakte Form starke Deletionssignale in der Nähe der gefalteten Region, wenn sie einem berberinbasierten Sondenmolekül ausgesetzt wurde; unabhängige Tests bestätigten dort ebenfalls stärkere Bindung. Das Mutant‑Fragment, das dieselbe Form nicht ausbilden kann, erzeugte deutlich weniger Deletionen und schwächere Bindung. Andere gängige Kartierungsverfahren übersahen diesen Unterschied teilweise oder lieferten verwirrenden Untergrund, was die verbesserte Sensitivität und Spezifität des neuen Ansatzes unterstreicht.
Durchmustern krebsassoziierter Mutationen in vielen Genen
Anschließend skalierten die Forschenden die Methode. Sie bauten eine RNA‑Bibliothek mit 5′‑untranslatierten Regionen (5′‑UTRs) von 283 krebsrelevanten Genen auf, jeweils ergänzt um somatische Mutationen, wie sie in Tumoren berichtet wurden. Mit einer Sonde, die G‑Quadruplex‑ähnliche Strukturen erkennt, deckte BIVID‑MaP zahlreiche Mutationen auf, die die Bindung von Kleinstmolekülen entweder verstärkten oder abschwächten. In Genen wie DAXX und ING2 veränderten einzelne Buchstaben in guaninreichen Abschnitten die Bindung deutlich, was mit unabhängigen biophysikalischen Tests zur G‑Quadruplex‑Bildung und direkten Bindungsmessungen per Massenspektrometrie übereinstimmte. In einigen Fällen verschoben Mutationen außerhalb offensichtlicher G‑Trakte die Bindung, indem sie fein die Paarungsneigung benachbarter Basen veränderten und so das strukturelle „Ensemble“ umformten, ohne die vorhergesagte Gesamtfaltung grob zu verändern. 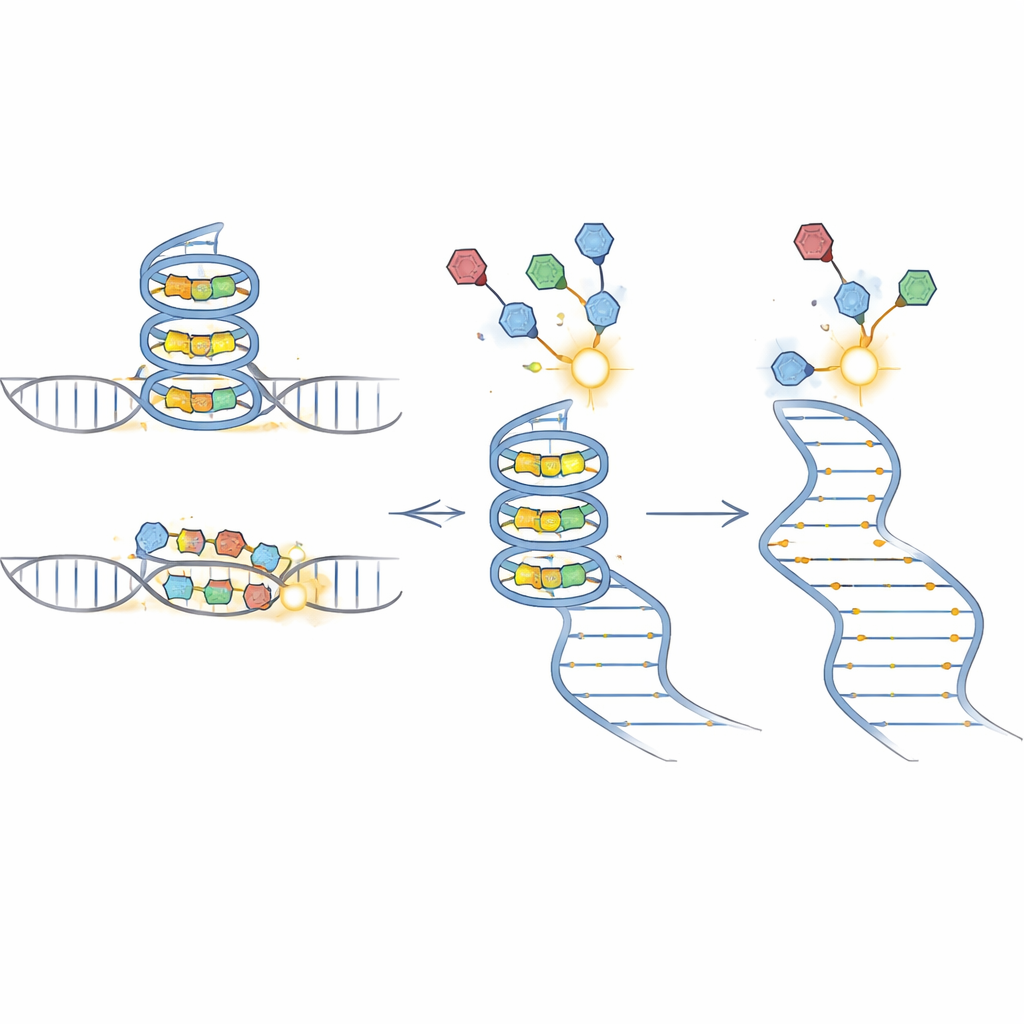
Was Computervorhersagen übersehen
Bedeutsam ist, dass bestehende Werkzeuge zur Vorhersage von RNA‑Struktur und G‑Quadruplexen oft nicht die Änderungen vorhersagten, die BIVID‑MaP offenbarte. Manche Varianten, die in computationalen Scores kaum auffielen, führten in der Realität zu großen Unterschieden in der Bindung. Andere wirkten sich auf eine ganze Familie von G‑Quadruplex‑zielenden Verbindungen aus, während bestimmte Mutationen eher wirkstoffspezifische Effekte zeigten. Das demonstriert, dass Einzel‑Nukleotid‑Varianten die Landschaft von RNA‑Faltungen und Medikamentenkontakten auf Weisen feinjustieren können, die sich aus der Sequenz allein nur schwer ableiten lassen.
Folgen für personalisierte RNA‑Medikamente
Die Autoren kommen zu dem Schluss, dass BIVID‑MaP einen leistungsfähigen Weg bietet, um zu kartieren, wie individuelle genetische Unterschiede RNA‑Strukturen und deren Wechselwirkungen mit Kleinstmolekül‑Medikamenten umgestalten. Indem lokale chemische Modifikationen in präzise Deletionssignaturen verwandelt werden, kann die Methode Tausende Varianten parallel untersuchen und diejenigen hervorheben, die die Wirkstoffbindung bedeutsam verändern. Langfristig könnten solche Karten die Entwicklung von RNA‑gerichteten Medikamenten leiten, die über verschiedene Patientengruppen hinweg wirksamer und sicherer sind, und bislang verborgene RNA‑Strukturen aufdecken, die als neue Arzneimittelziele dienen könnten.
Zitation: Miyashita, E., Onizuka, K., Chen, Y. et al. Systematic identification of variant-specific RNA structure-small molecule interactions exemplified by RNA G-quadruplexes. Nat Commun 17, 2243 (2026). https://doi.org/10.1038/s41467-026-70097-9
Schlüsselwörter: RNA‑zielgerichtete Medikamente, G‑Quadruplex, genetische Varianten, Bindung von Kleinstmolekülen, Krebs‑Mutationen