Clear Sky Science · de
Optimierung der räumlichen Anordnung von FtsZ-Ringen für großmaßstäbliche Einschnürung in synthetischen Zellen
Warum winzige Ringe beim Bau synthetischer Zellen wichtig sind
Stellen Sie sich vor, man konstruiert eine einfache, künstliche Zelle, die von selbst wachsen und sich in zwei Teile teilen kann. Dafür müssen Forschende lernen, wie man eine weiche, seifenblasenähnliche Membran kontrolliert zusammenzieht, und das nur mit wenigen biologischen Bauteilen. Diese Studie zeigt, wie ein bakterielles Protein dabei unterstützt werden kann, große, stabile Ringe auf riesigen Fetttropfen zu bilden, sodass diese Modell‑„Zellen“ beinahe bis zur Teilung einschnüren. Sie liefert Einsichten, welche Proteinar‑chitektur nötig ist, um eine Membran in der Größenordnung einer ganzen Zelle zu verbiegen und umzuformen.
Das Teilchenwerkzeug der Natur nutzen
Viele Bakterien teilen sich mithilfe eines Proteins namens FtsZ, einem entfernten Verwandten des Tubulins, das das innere Gerüst unserer eigenen Zellen bildet. FtsZ lagert sich zu Filamenten zusammen, die einen Ring in der Mitte der Zelle bilden und damit die Teilungsstelle markieren. In lebenden Bakterien befestigt eine Reihe von Helferproteinen diesen Ring an der inneren Membran, positioniert ihn in der Zellmitte und verknüpft ihn mit Enzymen, die die Zellwand umbauen. Frühere Laborversuche, diese Maschinerie in großen, zellgroßen Vesikeln nachzubilden, hatten zwar Ringe und kleine Eindellungen der Membran erzeugt, aber keine gleichmäßige, fortschreitende Einschnürung, die ein riesiges Vesikel in zwei fast separate Hälften umformt.
Ein minimalistischer Ansatz für eine teilende Hülle
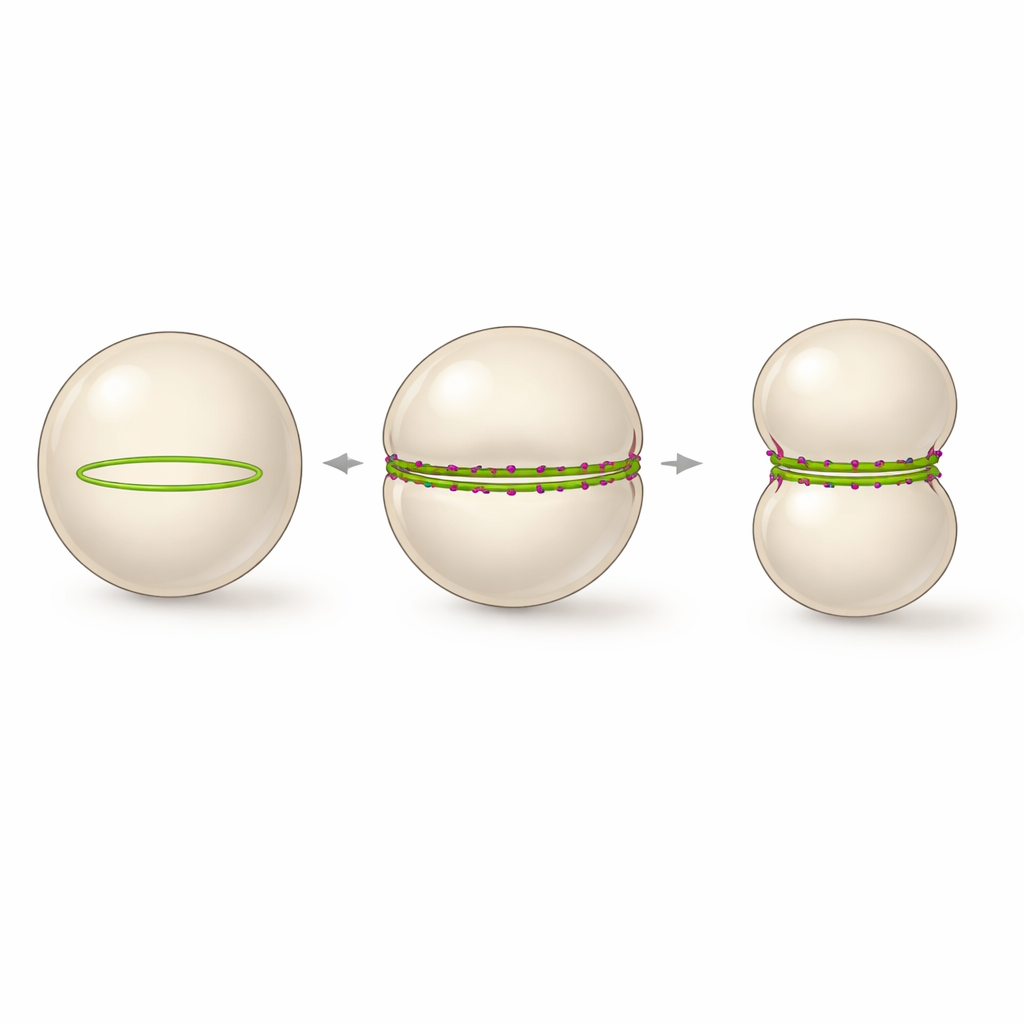
Die Autorinnen und Autoren fragten, ob sich das System auf nur zwei Komponenten reduzieren lässt: eine Variante von FtsZ, die direkt an Membranen haftet, und einen kurzen positiv geladenen Schwanz eines anderen Teilungsproteins, FtsN. Sie kapselten diese Komponenten in riesigen unilamellaren Vesikeln ein — hohle Lipidsphären, die vereinfachten Zellen ähneln — und versorgten sie mit dem Energieträger GTP sowie einem langsam wirkenden GTP‑Analogon, um die Proteindynamik zu justieren. Ohne den FtsN‑Schwanz bildete FtsZ viele winzige Ringe und Flecken, die nur lokale Dellen verursachten. Mit einem Überschuss des FtsN‑Fragments (cytoFtsN genannt) reorganisierten sich diese kleinen Ringe zu einem einzigen großen Ring, der den Vesikeläquator umschloss und sich über mehrere Stunden einschnüren konnte.
Vom verfilzten Netzwerk zum einzelnen kontraktilen Ring
Um zu verstehen, wie dieses kleine Peptid das Verhalten so drastisch verändert, beobachtete das Team FtsZ‑Filamente auf flachen, gestützten Membranen mit hochauflösender Mikroskopie. Normalerweise bildet FtsZ auf solchen Oberflächen wirbelnde, geschwungene Vortices. Mit zunehmender Zugabe von cytoFtsN verschwanden diese Spiralen allmählich und wurden durch geradere, stärker ausgerichtete Bündel ersetzt. Quantitative Bildauswertung bestätigte, dass das Netzwerk kohärenter und geordneter wurde, je höher die Peptidkonzentration war. Messungen der Fluoreszenz‑Erholung zeigten, dass Untereinheiten in diesen Bündeln langsamer ausgetauscht wurden, was darauf hindeutet, dass das Peptid die Filamente stabilisiert und ihre turbulente Dynamik dämpft.

Elektrostatisches „Klettband“, das Filamente zusammenriegeln
Biochemische Messungen zeigten, dass cytoFtsN und FtsZ hauptsächlich durch entgegengesetzte elektrische Ladungen interagieren: FtsZ ist insgesamt negativ geladen, während das Peptid Cluster positiver Ladungen trägt. Bei niedrigeren Salzkonzentrationen band das Peptid stärker, förderte die Bildung dickerer FtsZ‑Bündel in Lösung und verlangsamte den Abbau der Filamente, indem es die GTP‑Hydrolyse des Proteins dämpfte. Als die Forschenden zentrale positiv geladene Reste im Peptid austauschten oder die Salzkonzentration erhöhten, wodurch die elektrostatische Anziehung abgeschirmt wurde, verschwanden die Bündelungs‑ und Reorganisations‑Effekte. Das deutet auf einen einfachen physikalischen Mechanismus hin, bei dem das positiv geladene Peptid wie molekulares „Klettband“ wirkt und die Abstoßung zwischen FtsZ‑Filamenten reduziert, sodass sie Seite an Seite zu steifen Bündeln zusammenpacken können.
Wie ein einzelner Ring ein riesiges Vesikel umformt
Innerhalb der Vesikel hat diese peptidstabilisierte Bündelung eine auffällige Konsequenz. Anstelle vieler kleiner gekrümmter Ringe werden die geglätteten FtsZ‑Bündel gezwungen, der großen Krümmung des Vesikels zu folgen, und ordnen sich zu einem durchgehenden Ring an, der den gesamten Umfang überspannt. Zeitrafferaufnahmen zeigten, dass immer wenn ein solcher vollständig geschlossener Ring entstand, das Vesikel zuverlässig von einer Kugel zu einer Hantelgestalt deformiert wurde, mit einer schmalen Taille an der Stelle des Rings. Der Prozess ließ sich in Echtzeit verfolgen, während der Vesikeldurchmesser schrumpfte und die Einschnürung tiefer wurde, sodass das Kompartiment fast in zwei Teile geteilt wurde, obwohl die endgültige Abtrennung nicht erreicht wurde. Die Autorinnen und Autoren schlagen vor, dass ein stabiler, den Äquator überspannender FtsZ‑Ring mit verlangsamtem, aber weiterhin aktivem Austausch die minimale Architektur ist, die großmaßstäbliche Membraneinschnürung in einer synthetischen Zelle antreiben kann.
Was das für zukünftiges synthetisches Leben bedeutet
Indem gezeigt wird, dass eine membranverankerte FtsZ‑Variante plus ein kurzes kationisches Peptid riesige Lipidvesikel fast bis zur Teilung umformen können, definiert diese Arbeit eine klare Gestaltungsregel für künstliche Zellen: Ein einzelner, kohärenter Proteinring, der zur Größe der Zelle passt und über die Zeit mechanisch stabil bleibt, reicht aus, um an einer weichen Grenze auf Zellskalenniveau einzuknicken. Für das vollständige Durchtrennen der Membran könnten noch komplexere Faktoren nötig sein, doch die Studie demonstriert, dass kontrollierte großmaßstäbliche Einschnürung kein komplettes Ensemble bakterieller Teilungsproteine erfordert. Stattdessen kann durch gezielte Feinabstimmung von Filamentorganisation und Dynamik ein einfaches Proteingerüst in einen effektiven kontraktilen Ring verwandelt werden — ein Schritt näher an wirklich selbstteilenden synthetischen Zellen.
Zitation: Panevska, A., Šakanović, A., Paccione, G. et al. Optimizing spatial organization of FtsZ rings for large-scale constriction in synthetic cells. Nat Commun 17, 2320 (2026). https://doi.org/10.1038/s41467-026-70091-1
Schlüsselwörter: synthetische Zellteilung, FtsZ-Ring, Membraneinschnürung, minimales Divisom, zytoskelettale Selbstorganisation