Clear Sky Science · de
Subzelluläres Proteomik zeigt einen Bauplan für die Integration von Endosymbionten in dem Trypanosomatiden Angomonas deanei
Verborgene Partner in einzelligen Lebewesen
Viele einzellige Organismen sind nicht wirklich allein. Einige beherbergen Bakterien, die dauerhaft in ihnen leben und als ständige Mieter Nährstoffe und Dienste tauschen — Beziehungen, die an die Ursprünge unserer eigenen Mitochondrien erinnern. Diese Studie untersucht eine solche Partnerschaft in Angomonas deanei, einem mikroskopischen Insektenparasiten, und zeigt, wie ein einst frei lebendes Bakterium tief in die inneren Abläufe der Wirtszelle eingebunden wurde.
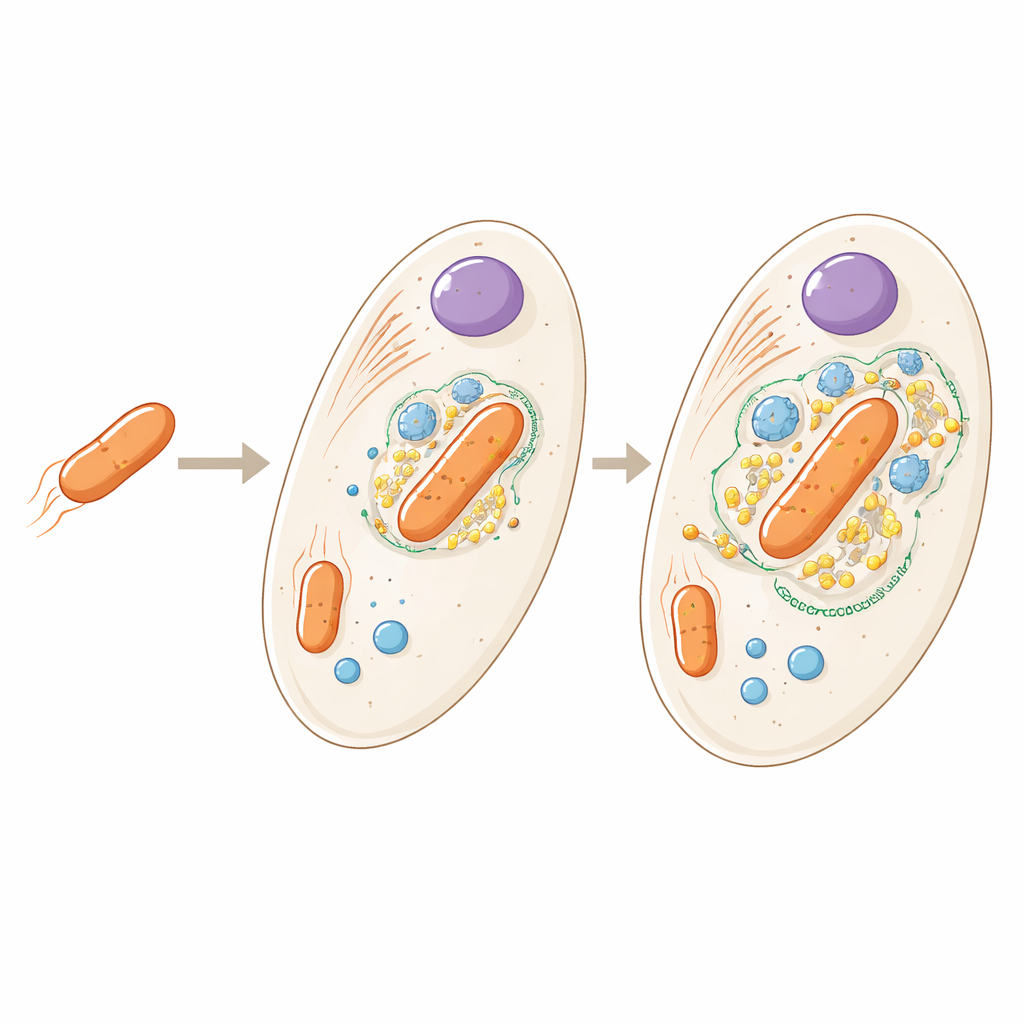
Vom Hausgast zum eingebauten Teil
Das im Inneren von Angomonas deanei lebende Bakterium ist ein entfernter Verwandter frei lebender Bodenmikroben, existiert hier jedoch als einzelne Kopie pro Wirtszelle und kann nicht mehr eigenständig überleben. Frühere Arbeiten zeigten, dass der Wirt spezielle Proteine produziert, die in das Bakterium gelangen und sogar seine Teilung mitsteuern. Die neue Studie stellt eine weiter gefasste Frage: Wenn man die gesamte Zelle betrachtet, wo genau befinden sich alle Wirts- und bakteriellen Proteine, und was sagt das darüber aus, wie eng die beiden Partner integriert sind?
Die Stadtkarte des Zellinneren erstellen
Um das zu beantworten, öffneten die Forschenden große Mengen von Zellen sehr behutsam, sodass die inneren Strukturen weitgehend intakt blieben. Sie trennten diese Komponenten durch Zentrifugation bei unterschiedlichen Geschwindigkeiten und identifizierten in jedem Fraktion Tausende von Proteinen mittels hochauflösender Massenspektrometrie. Durch den Vergleich, wie Proteine über die Fraktionen hinweg gruppierten, und die Gegenprüfung mit bekannten Markern und Fluoreszenzmikroskopie, erstellten sie ein detailliertes „Adressbuch“ der Zelle und ordneten nahezu 3.000 Proteine 21 verschiedenen Bereichen zu, etwa dem Zellkern, Mitochondrium, spezialisierten Speicherorganellen und dem bakteriellen Endosymbionten selbst.
Wirtstools, die auf das im Inneren lebende Bakterium abzielen
Innerhalb dieses Atlas entdeckte das Team eine Reihe wirtsproduzierter Proteine, die konsequent mit dem Endosymbionten mitreisten, wodurch die bekannte Sammlung sogenannter endosymbiontentargetierter Proteine erweitert wurde. Ein neu bestätigtes Beispiel, ETP10 genannt, umhüllt das Bakterium ähnlich wie ein zuvor beschriebeneres Protein, was auf ein Gerüst aus Wirtsfaktoren um den mikrobiellen Partner hindeutet. Eine weitere kleine Proteinengruppe zeigte ein ungewöhnliches physikalisches Verhalten, das sie mit einem bereits bekannten dynaminähnlichen Protein teilt, das das Bakterium bei der Teilung abknipst. Zusammengenommen deuten diese Befunde auf eine spezialisierte, vom Wirt aufgebaute Maschinerie hin, die der Positionierung, Formgebung und Reproduktion des Endosymbionten innerhalb der Zelle gewidmet ist.
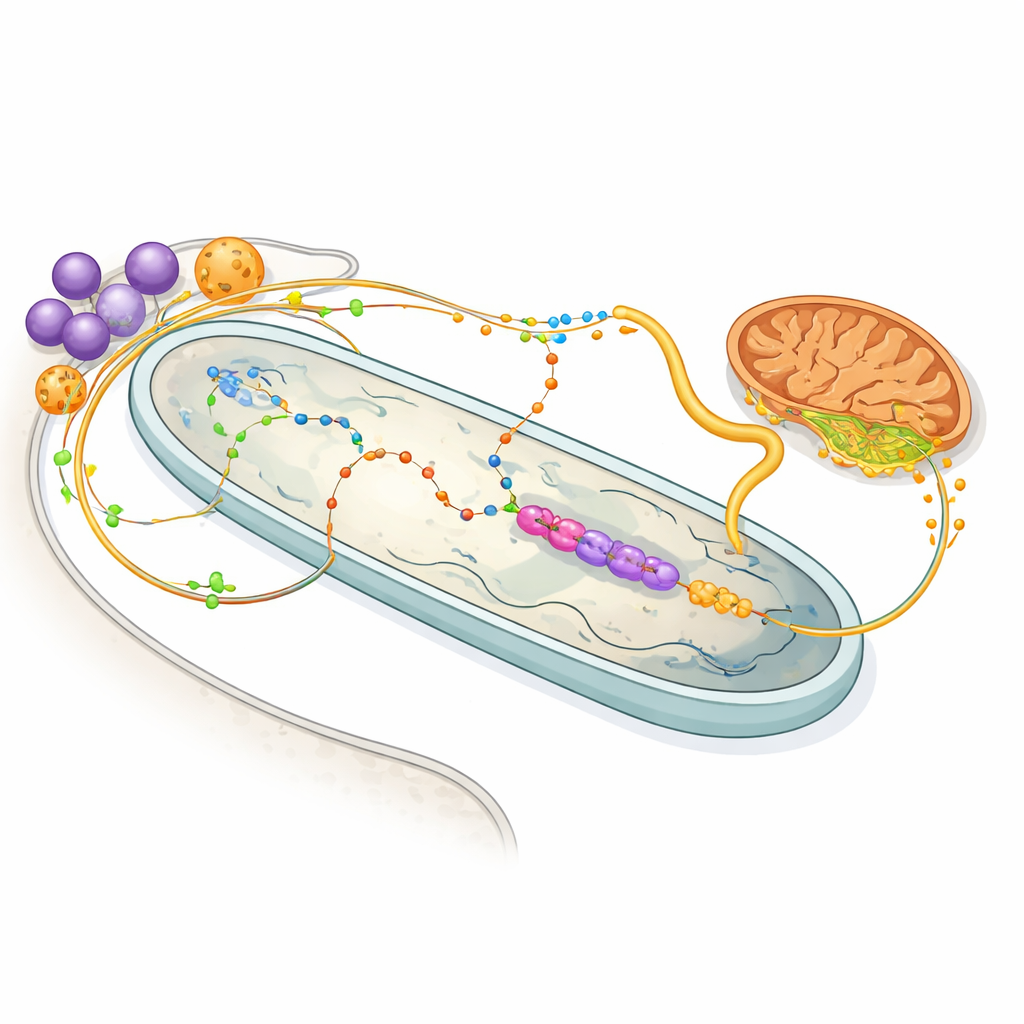
Energieaustausch und chemische Handelswege
Die Proteinkarte beleuchtet außerdem den regen Molekülhandel zwischen Wirt und Bakterium. Enzyme in den Glycosomen des Wirts — Organellen, die Zucker- und Aminosäurestoffwechsel übernehmen — scheinen darauf abgestimmt, das Bakterium mit der Aminosäure Prolin und der Verbindung 2‑Oxoglutarat zu versorgen, beides wertvolle Energiequellen. Im Inneren des Bakteriums nutzt ein reduziertes Enzymset 2‑Oxoglutarat zur Erzeugung von NADH, das eine minimale Atmungskette antreibt, und gibt dann Succinat an das Mitochondrium des Wirts zurück. Andere Wege zeigen, dass das Bakterium die meisten Schritte der Häm-Synthese ausführt — einem für den Wirt lebenswichtigen Pigment — und zugleich entscheidende Bausteine für Nukleotide liefert. Effektiv hat jeder Partner bestimmte Stoffwechselaufgaben an den anderen abgegeben und so ein geteiltes, voneinander abhängiges System geschaffen.
Neue Kommunikationswege innerhalb der Zelle
Über den Stoffwechsel hinaus zeigt die Studie physikalische und wahrscheinlich signalgebende Verknüpfungen zwischen dem Endosymbionten und anderen Organellen. Eine eigene Gruppe von Wirtsproteinen bildet das, was die Autorinnen und Autoren als „Kontaktstellen“-Cluster bezeichnen, angereichert an Komponenten der Kernhülle und des endoplasmatischen Retikulums, die physikalisch mit dem Bakterium ko-sedimentieren. Zwei Typen von Speicherorganellen — Glycosomen und Acidocalcisomen — treten in zwei Populationen auf: Einige bleiben frei im Zytoplasma, andere reisen stets mit dem Bakterium mit. Die Mikroskopie bestätigt, dass Teilmengen dieser Organellen dicht am Endosymbionten anliegen. Acidocalcisomen sind bekannte Calcium- und Phosphatspeicher, sodass ihre enge Lage nahelegt, dass ein wechselseitiger Signal- und Ionenverkehr das Bakterium, diese Speicher und das nahegelegene endoplasmatische Retikulum verbindet.
Ein Bauplan für Leben im Leben
Insgesamt liefert diese Arbeit einen reichen, zellweit gültigen Bauplan dafür, wie ein Bakterium funktionsfähig mit seinem Wirt verschmelzen kann, ohne bereits zu einem vollwertigen Organell wie den Mitochondrien geworden zu sein. Angomonas deanei ist auf seinen Endosymbionten für Schlüsselnährstoffe angewiesen, während das Bakterium seinerseits auf wirtsproduzierte Proteine und energiereiche Moleküle angewiesen ist und an Wirtsorganellen gebunden ist, um Kommunikation und Kontrolle zu ermöglichen. Für Nichtfachleute lautet die Schlussfolgerung, dass die Evolution Kooperationen zwischen sehr unterschiedlichen Lebensformen schrittweise fest verdrahten kann, bis eine Trennung unmöglich wird. Dieses System bietet eine lebendige Momentaufnahme dieses Prozesses in Aktion und hilft Forschenden zu verstehen, wie komplexe Zellen wie unsere eigenen einst aus einfacheren Anfängen entstanden sein könnten.
Zitation: Hammond, M., Chmelová, Ľ., van Geelen-Kuenzel, N.A. et al. Subcellular proteomics reveals a blueprint for endosymbiont integration in trypanosomatid Angomonas deanei. Nat Commun 17, 2241 (2026). https://doi.org/10.1038/s41467-026-70084-0
Schlüsselwörter: Endosymbiose, Zellmetabolismus, Organellenentwicklung, Protistenbiologie, Wirts-Mikroben-Interaktionen