Clear Sky Science · de
Der Lebensstil von Acinetobacter baumannii umfasst Besiedelung von verrottendem Pflanzenmaterial im Boden und luftgetragene Verbreitung
Warum die wilde Seite dieses Krankenhauskeims für Sie wichtig ist
Acinetobacter baumannii ist am bekanntesten als schwer zu beseitigender Krankenhauskeim, der vielen Antibiotika trotzt. Diese Studie zeigt, dass dasselbe Mikrobenleben auch draußen ein reiches Dasein führt – im Boden, in verrottenden Pflanzen, in Tieren und sogar in der Luft. Indem sie aufdeckt, wo es herkommt und wie es sich verbreitet, hilft die Arbeit zu erklären, warum dieses Bakterium so widerstandsfähig ist und warum es immer wieder in Krankenhäusern weltweit auftaucht.

Verstecktes Leben auf Feldern, in Flüssen und Vogelnestern
Die Forschenden begannen mit einem unerwarteten Hinweis: Weißstorchküken in Polen trugen A. baumannii häufig in den oberen Atemwegen, weit entfernt von Krankenhäusern. Indem das Team der Nahrung und Umgebung der Vögel folgte, spürten sie das Bakterium nicht in Insekten oder Fischen, sondern vor allem in Kleinsäugern, Regenwürmern und – am wichtigsten – feuchten Böden mit reichlich verrottendem Pflanzenmaterial entlang von Flüssen und in Komposthaufen nach. Waldböden, selbst entlang von Bächen, beherbergten das Bakterium selten, während Flussufer außerhalb von Wäldern manchmal als „Hotspots“ dienten, an denen viele verschiedene Stämme nebeneinander existierten.
Von verrottenden Pflanzen in die freie Luft
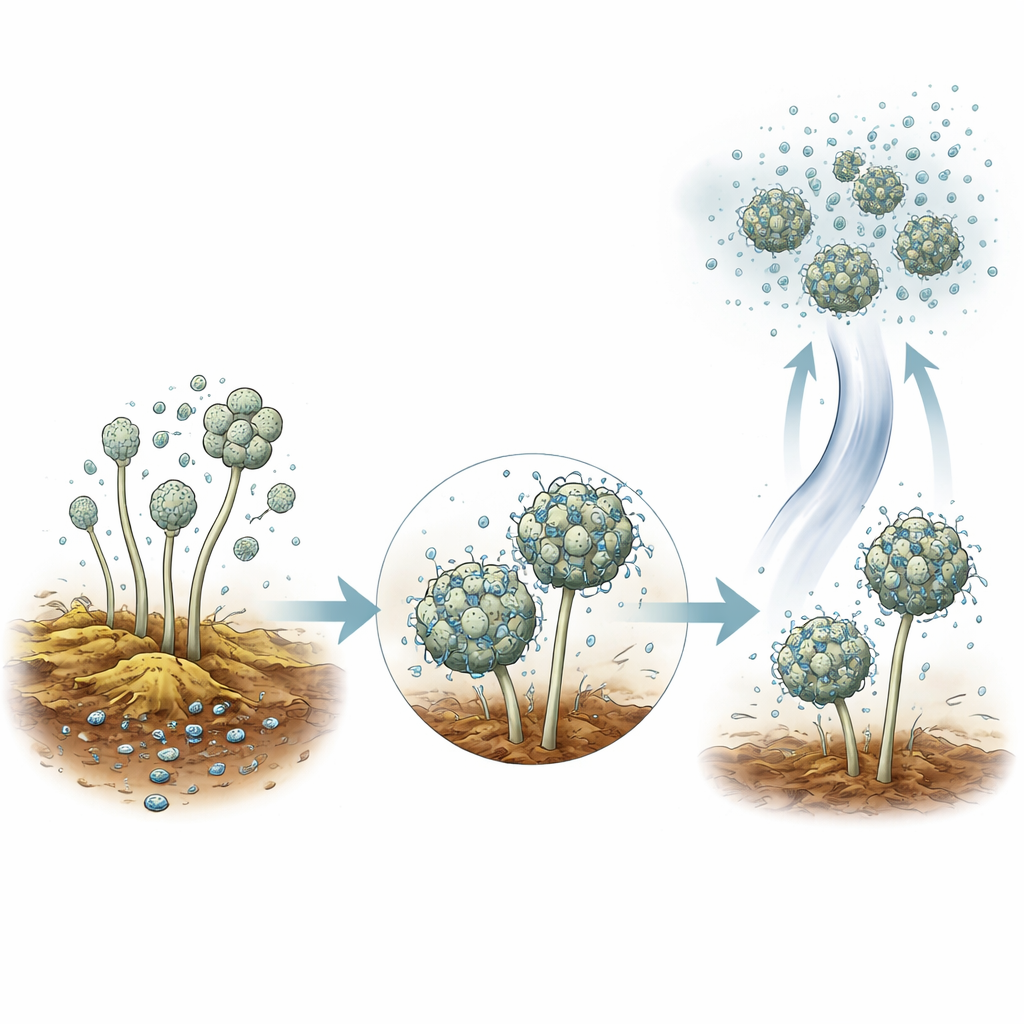
Sorgfältige Feldexperimente zeigten, dass A. baumannii sich zu verrottendem Pflanzenmaterial hingezogen fühlt. Als die Autorinnen und Autoren sterilisierte Pflanzenschnipsel in Gärten auslegten, wurden diese innerhalb weniger Wochen besiedelt – selbst wenn sie über dem Boden aufgehängt und nur über die Luft erreichbar waren. Über aktiven Komposthaufen aufgestellte Lufteinrichtungen sammelten ebenfalls das Bakterium. In Laborversuchen stellte das Team fest, dass sich A. baumannii leicht an Sporen üblicher Schimmelpilze wie Aspergillus und Penicillium heftet. Bakterien überzogen die Sporen allmählich und bremsten sogar deren Keimungsfähigkeit. Da Pilzsporen aus Kompost und Böden leicht in die Luft gelangen, bietet diese enge Partnerschaft einen einfachen Mechanismus, mit dem sich das Bakterium atmosphärisch fortbewegen kann.
Weltreisende mit alten Wurzeln
Um zu sehen, wie diese wilden Stämme zu Krankenhausstämmen in Beziehung stehen, sequenzierte das Team 401 neue Genome aus Proben von Storchennestern, Boden, Pflanzen, Würmern, Nagetieren und anderen Quellen und verglich sie mit Hunderten öffentlich verfügbarer Genome. Der daraus resultierende Stammbaum zeigte eine bemerkenswerte Durchmischung: Umwelt-, Tier- und klinische Humanisolate verteilten sich über dieselben Zweige und unterschieden sich oft nur durch wenige DNA-Veränderungen. Einige nahezu identische Verwandte wurden auf verschiedenen Kontinenten gefunden, was darauf hindeutet, dass dieselben Linien innerhalb weniger Jahrzehnte Ozeane überquert haben. Auf Basis der Rate, mit der Mutationen akkumulieren, schätzen die Autorinnen und Autoren, dass A. baumannii als Art überraschend jung ist – in der Größenordnung von etwa 15.000 Jahren – und sich rapide diversifizierte etwa zu der Zeit, als Menschen großflächige Landwirtschaft betrieben und Wälder rodeten.
Ein gewaltiges Werkzeugset, aber wenig menschlicher Fingerabdruck in der Natur
Durch die Kombination aller Genome schätzten die Forschenden, dass der kombinierte Genbestand der Art – das Pan-Genom – ungefähr 51.000 verschiedene Gensippen enthält, mehr als doppelt so viel wie frühere Schätzungen. Dieser große genetische Werkzeugkasten erklärt vermutlich ihre Fähigkeit, sich an extreme Trockenheit, Strahlung, Desinfektionsmittel und Antibiotika anzupassen. Dennoch trugen die meisten Wildtier- und Bodenisolate nur eine geringe Anzahl bekannter Resistenzgene und wenige mobile DNA-Elemente, im Gegensatz zu Krankenhausstämmen, die voller solcher Merkmale sind. Dieses Muster legt nahe, dass die natürlich vorkommenden Populationen, die hier beprobt wurden, noch relativ unberührt von moderner Antibiotikaanwendung sind und eine „Bezugsbasis“ der Art vor vollständiger Krankenhausanpassung bieten.
Was das für Krankenhäuser und Gesundheitssysteme bedeutet
Die Studie zeichnet A. baumannii nicht als rein vom Menschen gemachtes Problem, sondern als natürlich luftgetragenes, pflanzen- und bodenassoziiertes Bakterium, das erst kürzlich begonnen hat, Krankenhäuser und Viehbetriebe als neue Lebensräume zu nutzen. Seine Partnerschaft mit Pilzen, die Toleranz gegenüber rauen Bedingungen und die enorme genetische Vielfalt machen es gut geeignet für weiträumige atmosphärische Reisen und schnelle Evolution. Für Laien lautet die Quintessenz, dass die Infektionskontrolle nicht nur auf die Übertragung von Patient zu Patient innerhalb von Krankenhäusern fokussieren darf. Saisonale Anstiege, schimmelbelastete Innenräume, Kompostierungsanlagen und breitere Landnutzungsänderungen beeinflussen alle, wann und wie dieser widerstandsfähige Keim in menschliche Umgebungen gelangt – und das Verständnis seines Außenlebensstils ist entscheidend, um künftigen multiresistenten Stämmen einen Schritt voraus zu sein.
Zitation: Wilharm, G., Skiebe, E., Michalska, A. et al. Acinetobacter baumannii’s lifestyle includes soil-dwelling colonization of decaying plant material and airborne spread. Nat Commun 17, 2316 (2026). https://doi.org/10.1038/s41467-026-70072-4
Schlüsselwörter: Acinetobacter baumannii, luftgetragene Bakterien, Bodenmikrobiom, Antibiotikaresistenz, One Health