Clear Sky Science · de
Einzelmoleküldynamik zeigt, dass allein die ATP-Bindung die Substrattranslokation durch einen ABC‑Transporter antreibt
Warum winzige zelluläre Pumpen wichtig sind
Jede Zelle in Ihrem Körper ist auf mikroskopische Maschinen angewiesen, die Moleküle über Membranen transportieren und so alles formen, von der Nährstoffaufnahme bis zur Immunabwehr. Eine wichtige Klasse dieser Maschinen, die sogenannten ABC‑Transporter, nutzt den chemischen Brennstoff ATP der Zelle, um Fracht gegen ein Konzentrationsgefälle zu befördern. Doch Jahrzehnte lang stritten Wissenschaftler über eine grundlegende Frage: reicht der bloße Akt der ATP‑Bindung aus, um den Transportschritt zu treiben, oder wird die Energie erst bei der Zerlegung von ATP freigesetzt? Diese Studie zoomt an einzelnen Transportern Molekül für Molekül heran, um diese Debatte zu klären.
Einen Transporter nach dem anderen beobachten
Anstatt das kombinierte Verhalten von Millionen Molekülen zu messen, bauten die Forschenden eine Anordnung, die es ihnen erlaubt, einzelne Transportereignisse in Echtzeit zu verfolgen. Sie konzentrierten sich auf TmrAB, einen bakteriellen Verwandten des menschlichen TAP‑Transporters, der Immunpeptide für die Präsentation an killerische T‑Zellen lädt. TmrAB sitzt in einer Membran und befördert kurze Proteinstücke (Peptide) von einer Seite zur anderen mithilfe von ATP. Um jeden Transportschritt zu sehen, fingen die Forscher ein einzelnes TmrAB‑Molekül in einer künstlichen Membrantasche (Liposome) ein und platzierten darin ein speziell konstruiertes „Sensor“protein, das seine Fluoreszenz ändert, wenn es ein Peptid einfängt. Mit einem hochsensiblen Mikroskop konnten sie dann als kurzfristige Sprünge im Lichtsignal genau die Momente sehen, in denen ein Peptid nach dem anderen in der Tasche ankam.
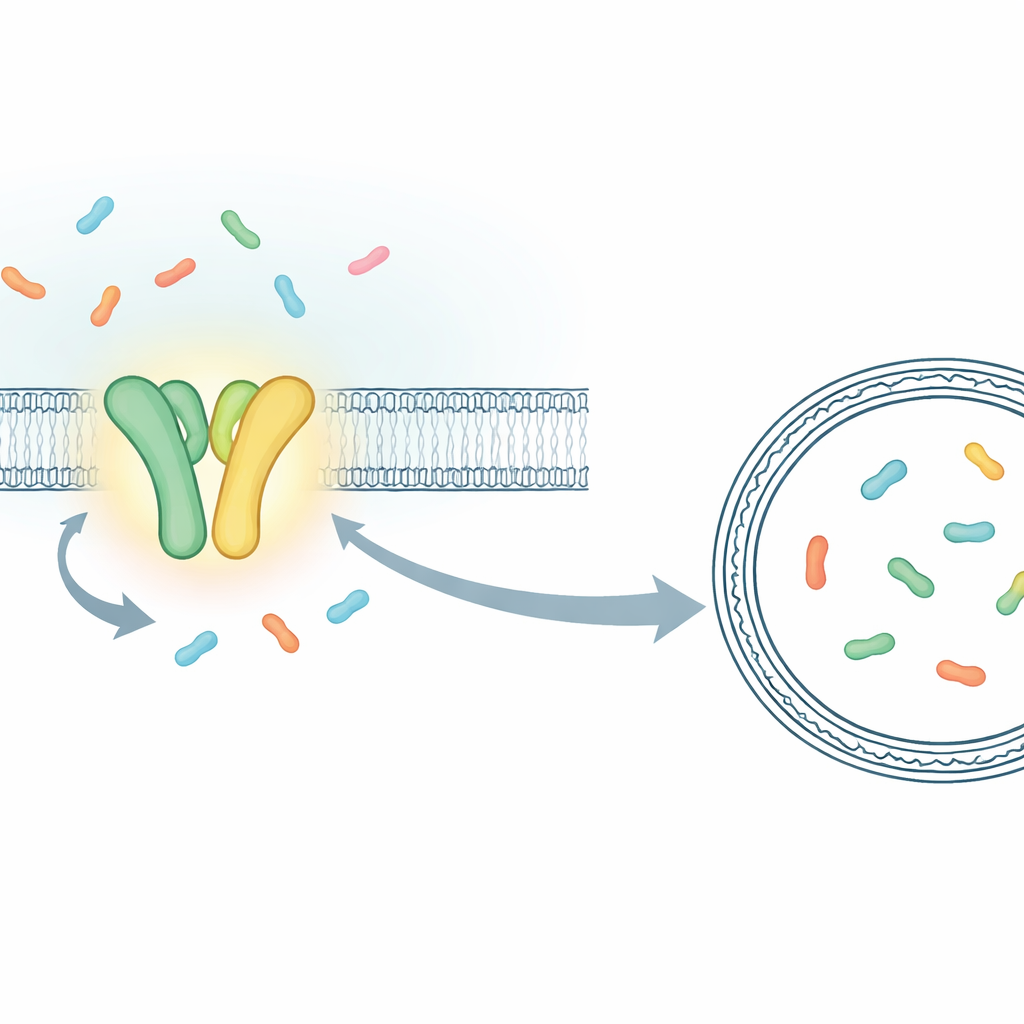
Nachweis: eine ATP‑Bindung befördert ein Peptid
Mit diesem Einzelmolekülassay verglichen die Forschenden normales TmrAB mit einer modifizierten, langsam arbeitenden Variante, deren Zyklen zeitlich gestreckt sind. Die langsame Variante machte es möglich, einzelne Ereignisse zu unterscheiden, die sonst verschwimmen würden. Sie zeigten, dass, wenn ATP und Peptide gemeinsam vorhanden waren, der Sensor im Liposom in diskreten Schritten vom „leer“- in den „beladen“-Zustand wechselte, wobei jeder Schritt mit dem Transport eines einzelnen Peptids übereinstimmte. Durch die Analyse, wie schnell sich der Sensor um die Peptide schloss, und durch Abschätzung des winzigen Volumens in jedem Liposom konnten sie diese Lichtänderungen sogar in ungefähre Peptidkonzentrationen übersetzen. Die Werte stimmten mit dem überein, was man erwarten würde, wenn sich nacheinander ein und dann zwei Peptide in Blasen von etwa 100 Nanometern Durchmesser ansammelten — ein Beleg dafür, dass sie Transportereignisse nun einzeln zählten.
Allein die ATP‑Bindung schaltet den molekularen Mechanismus um
Der zentrale Streit betrifft Magnesiumionen (Mg2+), die in Zellen normalerweise mit ATP assoziiert sind und für eine effiziente ATP‑Hydrolyse erforderlich sind. Manche Modelle schlugen vor, dass Mg2+ auch für die ATP‑Bindung oder für das Schließen des Transporters nötig sein könnte. Um diese Rollen zu trennen, entfernten die Forschenden Mg2+ mittels eines chelatierenden Mittels, versorgten das System jedoch weiterhin mit ATP. Unter diesen Bedingungen konnten sowohl der normale als auch der langsame Transporter genau einen Peptidtransportschritt pro Molekül durchführen und stoppten dann. Dieses Verhalten deutet darauf hin, dass ATP trotzdem binden und den Transporter von einer nach innen geöffneten in eine nach außen geöffnete Konformation zwingen kann und so ein Peptid bewegt, selbst ohne Mg2+. Ohne Mg2+ kann der Transporter jedoch ATP nicht effizient spalten und sich daher nicht für eine weitere Runde zurücksetzen.
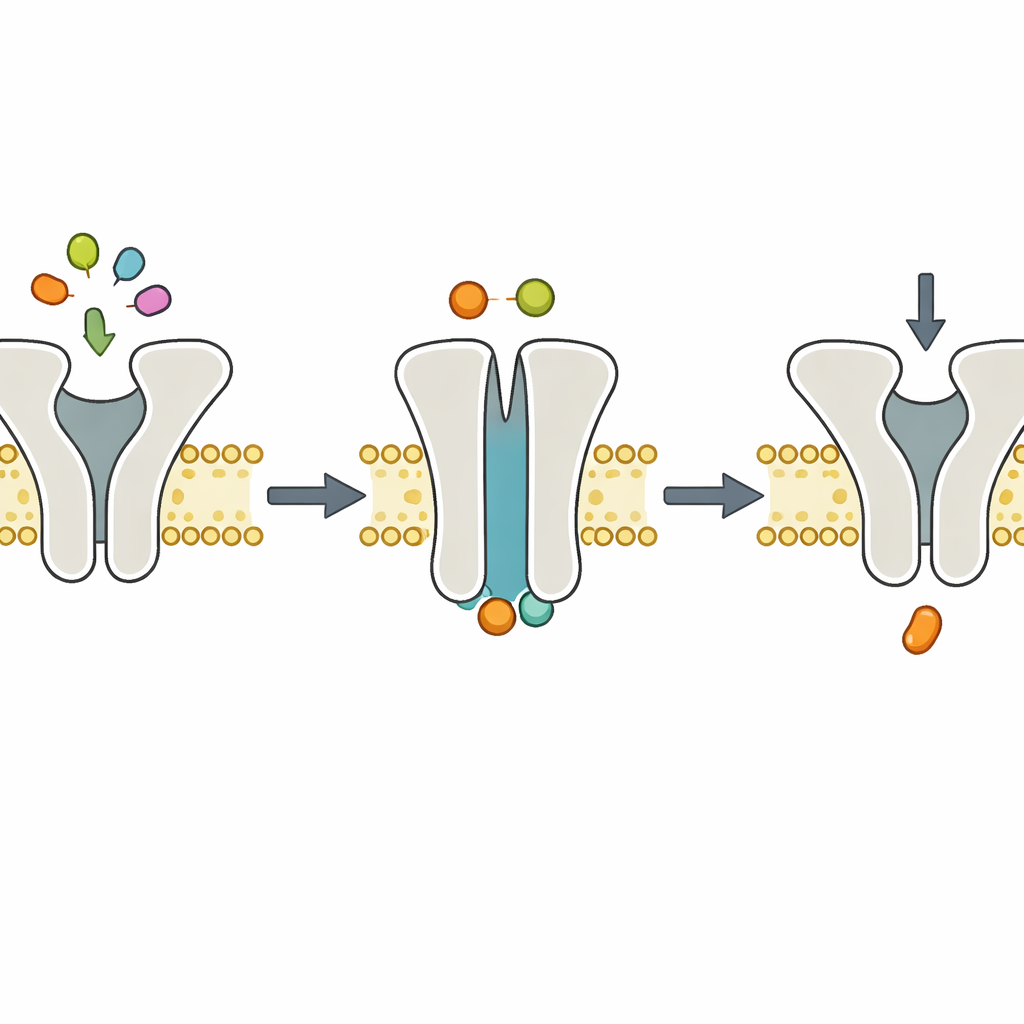
Strukturelle Momentaufnahmen stützen die Dynamik
Um zu sehen, wie die Maschine während dieses Mg2+‑freien Schrittes aussieht, wandte das Team kryo‑Elektronenmikroskopie an, die eingefrorene Moleküle in nahezu atomarer Auflösung abbildet. Sie rekonstituierten TmrAB in Lipid‑Nanodisc‑Systemen, gaben ATP ohne Mg2+ hinzu und froren die Komplexe ein. Die resultierenden Strukturen zeigten TmrAB in einer nach außen gerichteten, „okkudierten“ Konformation mit ATP in beiden internen Bindetaschen, jedoch ohne sichtbares Mg2+. Diese Schnappschüsse unterschieden sich im Wesentlichen nicht von früheren Strukturen, die mit ATP und Mg2+ aufgenommen worden waren. Zusammen mit biochemischen Tests, die zeigten, dass die ATP‑Spaltung ohne Mg2+ vollständig zum Stillstand kommt, stützen die Bilder eine einfache Arbeitsteilung: Die ATP‑Bindung treibt den Konformationswechsel, der das Peptid bewegt, während die Mg2+‑abhängige ATP‑Hydrolyse den Erholungsschritt übernimmt.
Ein klareres Bild davon, wie zelluläre Pumpen funktionieren
Indem sie einzelne Transporter beobachteten und ihre Strukturen lösten, beantwortet diese Arbeit eine langjährige Frage zu ABC‑Transportern: Der mechanische Kraftstoß, der ein Peptid bewegt, wird durch die ATP‑Bindung selbst ausgelöst, nicht durch die spätere chemische Spaltung von ATP. Mg2+ tritt hauptsächlich auf, um die Spaltung von ATP zu ermöglichen, wodurch der Transporter wieder in den Ausgangszustand zurückversetzt werden kann. Über die Klärung eines grundlegenden Teils der Zellbiologie hinaus bietet dieser Einzelmolekülansatz eine Blaupause zum Aufschlüsseln weiterer Membranmachinerien, die Immunität, Medikamentenresistenz und viele Krankheiten steuern — ein Molekül und ein Transportschritt nach dem anderen.
Zitation: Nocker, C., Pečak, M., Nocker, T. et al. Single-molecule dynamics reveal ATP binding alone powers substrate translocation by an ABC transporter. Nat Commun 17, 3038 (2026). https://doi.org/10.1038/s41467-026-70021-1
Schlüsselwörter: ABC‑Transporter, ATP‑Bindung, Einzelmolekül‑FRET, Membrantransport, TAP und TmrAB