Clear Sky Science · de
Preußischblau-Nanopartikel, die mehrere PANoptosom-vermittelte PANoptosen anvisieren, zur Therapie ischämisch-reperfundierter Myokardschäden
Warum Schutz des heilenden Herzens wichtig ist
Wenn eine Person einen Herzinfarkt erleidet, bemühen sich Ärzte, die blockierte Arterie wieder zu öffnen und den Blutfluss wiederherzustellen. Dieser lebenserhaltende Schritt hat jedoch einen verborgenen Preis: die plötzliche Rückkehr von Sauerstoff kann das Herz selbst schädigen, Zellen abtöten und damit den Boden für Herzinsuffizienz bereiten. Diese Studie untersucht eine einfallsreiche Nanomedizin, die das Herz in diesem verletzlichen Zeitraum schützen will, indem sie mehrere verflochtene Wege des Zelltods zugleich blockiert und so potenziell sanftere Erholungen nach Herzinfarkten ermöglicht.
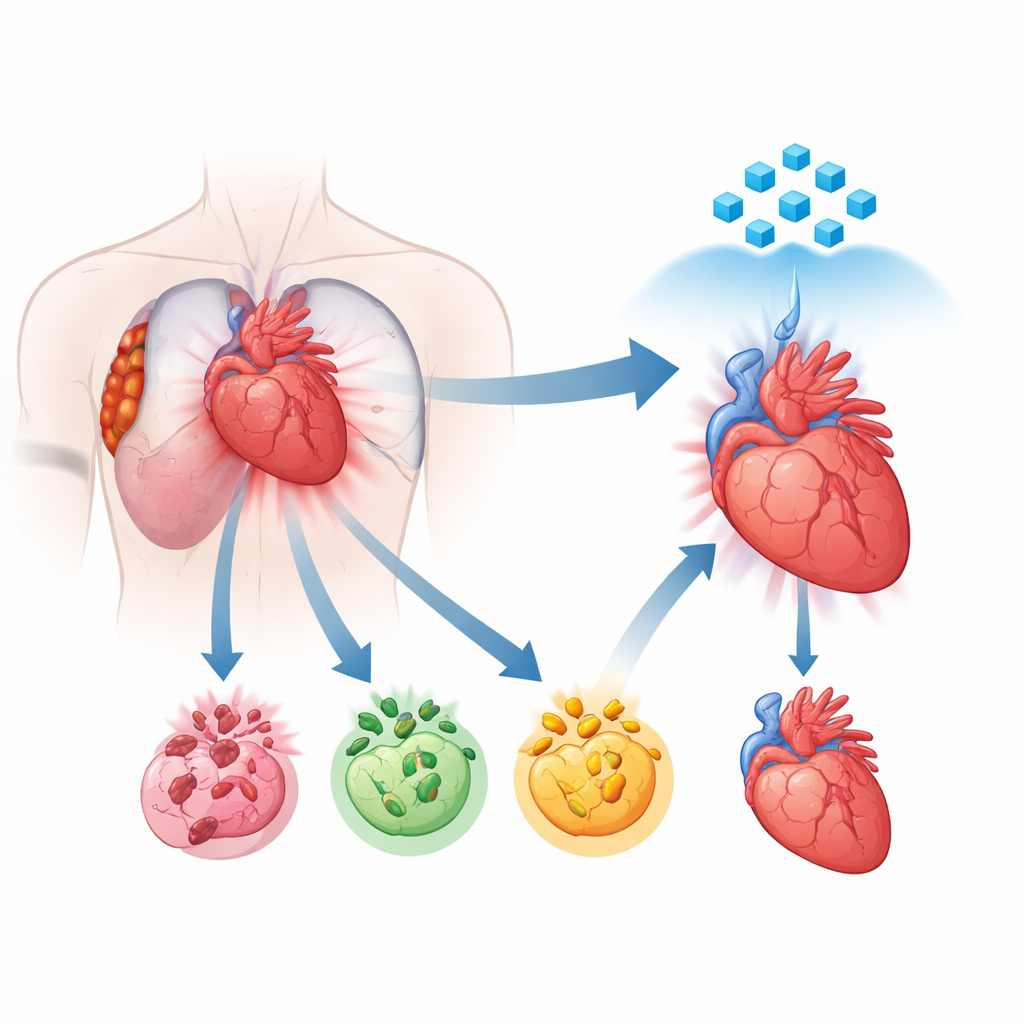
Ein neuer Blick darauf, wie Herzmuskelzellen sterben
Jahrelang wussten Wissenschaftler, dass geschädigte Herzmuskelzellen über verschiedene programmierte Wege sterben können, darunter Apoptose, Nekroptose und Pyroptose. Jeder folgt seinem eigenen molekularen Drehbuch, doch zunehmende Belege zeigen, dass diese Wege nicht isoliert arbeiten. Stattdessen kommunizieren sie miteinander und können sich zu einem kombinierten, außer Kontrolle geratenen Prozess vereinen, der als PANoptose bezeichnet wird. In diesem Zustand feuern mehrere Todesprogramme gleichzeitig ab, weshalb Therapien, die nur einen Weg blockieren, frustrierend schwach sein können. Die Autoren nutzten Einzelkern-RNA-Sequenzierung menschlichen Herzgewebes von Patientinnen und Patienten mit kürzlich erlittenem Herzinfarkt, um zu kartieren, wo und wie stark diese Todesprogramme aktiviert sind. Sie fanden heraus, dass in den am stärksten geschädigten Regionen Herzmuskelzellen eine kräftige Verschiebung hin zu diesem kombinierten Todesmodus zeigten und damit PANoptose als zentralen Treiber der Verletzung kennzeichneten.
Entwicklung eines kleinen Multifunktionswerkzeugs für das verletzte Herz
Um einen so komplexen Prozess anzugehen, wandte sich das Team Preußischblau zu, einer seit langem zugelassenen medizinischen Verbindung, die vor allem als Gegenmittel bei bestimmten Metallvergiftungen bekannt ist. Im Nanomaßstab verhalten sich Preußischblau-Partikel wie winzige katalytische Roboter, die schädliche Moleküle löschen und das Verhalten von Zellen beeinflussen können. Durch Computersimulationen zeigten die Forscher, dass sich diese Nanopartikel direkt an drei zentrale Proteinknoten – RIPK1, ZBP1 und AIM2 – binden können, die beim Aufbau der molekularen Maschinerie der PANoptose helfen. Indem sie sich auf unterschiedliche Weise an diese Knoten anlagern, wurden die Partikel voraussichtlich in der Lage sein, den Zusammenbau der todauslösenden Komplexe zu stören, die die drei Zelltodwege koordinieren.
Nanopartikel gezielt zum geschädigten Herzgewebe führen
Nanopartikel wirken nur, wenn sie den richtigen Ort erreichen, daher umhüllte das Team die Preußischblau-Partikel mit natürlichen Membranen, die von Blutplättchen gewonnen wurden – den Zellen, die verletzte Gefäße ansteuern. Diese Beschichtung schuf PB@PM, einen biomimetischen Träger, der wie eine Blutplättche zirkuliert, aber eine therapeutische Fracht abliefert. Bei Mäusen, die einem kontrollierten Herzinfarkt mit Wiedereröffnung der Arterie unterzogen wurden, zeigte die Bildgebung, dass sich PB@PM deutlich stärker im verletzten Herzbereich anreicherte als unbeschichtete Partikel, während gesunde Organe weitgehend verschont blieben. Wichtig ist, dass die beschichteten Partikel gut verträglich waren: Bluttests und Gewebeuntersuchungen zeigten keine offensichtliche Toxizität, was ihre Eignung für eine weitere Entwicklung stützt.
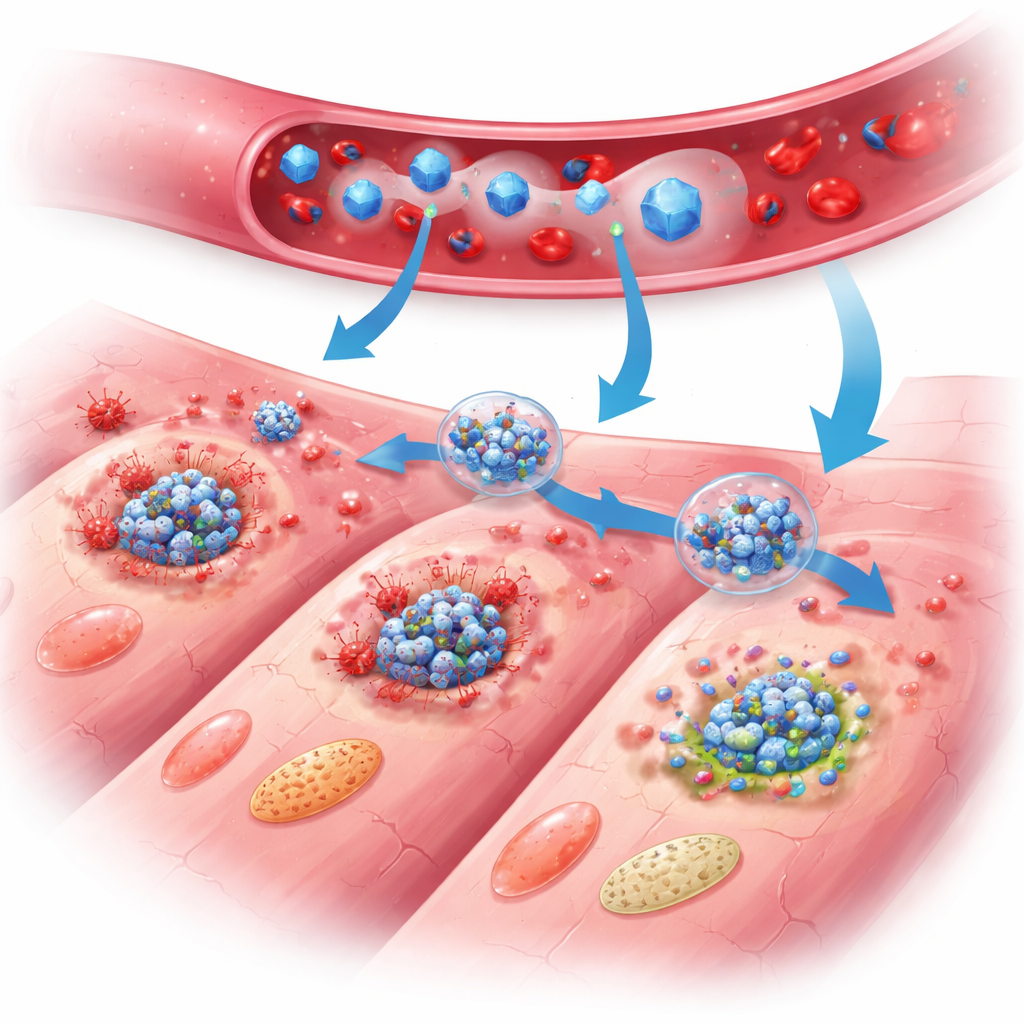
Wie der Nano-Schild das Herz schützt
Bei behandelten Mäusen zeigten sich die Vorteile von PB@PM über Tage und Wochen hinweg. Die Pumpfunktion des Herzens verbesserte sich, die Narbenfläche verringerte sich und die Herzwand wurde im Vergleich zu unbehandelten Tieren weniger dünn. Detaillierte Gewebestudien zeigten weniger sterbende Herzmuskelzellen, ruhiger reagierende Entzündungszellen und besser strukturiertes Reparaturgewebe mit gesünderem Gefäßneubau sowie weniger abnormer Vergrößerung überlebender Zellen. Auf molekularer Ebene zeigte ein breites Genexpressionsprofil und Proteinanalyse, dass PB@PM die drei großen Wege des programmierten Zelltods gleichzeitig dämpfte, den Aufbau der multiproteinären PANoptose-Komplexe störte und die Spiegel von Signalstoffen reduzierte, die Entzündungen antreiben. Die Partikel beseitigten außerdem schädliche reaktive Sauerstoffspezies, stabilisierten die Mitochondrien – die Kraftwerke der Zelle – und stellten einen normaleren Energiestoffwechsel wieder her, womit wichtige Auslöser, die Zellen sonst zur Selbstzerstörung treiben würden, entfernt wurden.
Was das für die künftige Behandlung von Herzinfarkten bedeuten könnte
Einfach ausgedrückt zeigt diese Arbeit, dass ein clever entwickelter Nanopartikel wie ein mehrstrahliger Schild für das Herz wirken kann, indem er ein Geflecht zerstörerischer Todessignale dämpft, statt jeweils nur einem Weg nachzujagen. Durch gezielte Ansteuerung des verletzten Herzgewebes, Bindung an zentrale Kontrollproteine und Milderung von oxidativem und entzündlichem Stress reduzierte PB@PM die Kettenreaktion aus Zellverlust und Vernarbung, die oft auf das Wiederöffnen einer blockierten Arterie folgt, deutlich. Obwohl noch umfangreiche Tests nötig sind, bevor diese Strategie Patienten erreichen könnte, liefert die Studie einen Proof-of-Concept, dass die gezielte Bekämpfung von PANoptose als Ganzes – und dies mit schlauen, biologisch inspirierten Partikeln – ein neues Kapitel im Schutz des Herzens nach Herzinfarkt eröffnen könnte.
Zitation: Xu, L., Jiang, L., Wu, R. et al. Prussian blue nanoparticles targeting multiple PANoptosome-mediated PANoptosis for myocardial ischemia-reperfusion injury therapy. Nat Commun 17, 2329 (2026). https://doi.org/10.1038/s41467-026-70012-2
Schlüsselwörter: Myokardischämie-Reperfusion, Nanopartikeltherapie, programmierter Zelltod, kardiale Entzündung, Mitochondrienschutz