Clear Sky Science · de
RPA stimuliert direkt die Prozessivität der Helikase Mer3, um eine normale Kreuzungsausbildung in der Meiose zu gewährleisten
Wie Zellen DNA durchmischen, um gesunde Eizellen und Spermien zu erzeugen
Jedes Mal, wenn eine Pflanze, ein Tier oder ein Mensch Eizellen oder Spermien bildet, müssen die Zellen die Chromosomen neu durchmischen, damit jeder Nachkomme eine frische Mischung elterlicher DNA erhält. Diese genetische Durchmischung beruht auf sorgfältig positionierten DNA-Austauschen, sogenannten Kreuzungen, zwischen Chromosomenpaaren. Die vorgestellte Studie enthüllt, wie zwei Schlüsseleiweiße, Mer3 und RPA, zusammen als mikroskopische Maschine arbeiten, um sicherzustellen, dass diese Kreuzungen effizient und sicher entstehen — ein Prozess mit Folgen für Fruchtbarkeit, Evolution und möglicherweise auch Krebs.
Ein empfindliches Gleichgewicht in der sexuellen Fortpflanzung
Während der speziellen Zellteilung Meiose treten Chromosomen in passenden Paaren auf, eines von jedem Elternteil. Damit sich diese Paare korrekt trennen, müssen sie an einigen wohlüberlegten Stellen entlang ihrer Länge physisch miteinander verbunden sein. Diese Verbindungen sind die Kreuzungen — Abschnitte, in denen DNA-Stränge eines Chromosoms mit denen des Partners ausgetauscht werden. Zu wenige Kreuzungen erhöhen das Risiko für fehlerhafte Chromosomenverteilung und Unfruchtbarkeit; zu viele oder ungünstig platzierte Kreuzungen können das Genom schädigen. Zellen verlassen sich daher auf spezialisierte Reparaturwege und Helferproteine, um einen gefährlichen DNA-Bruch in eine kontrolliert ausgebildete Kreuzung zu verwandeln.
Treffen Sie Mer3 und RPA, ein DNA-Aufwind-Team
Die Forschenden konzentrierten sich auf Mer3, einen molekularen Motor, der DNA aufwindet und die Kreuzungsbildung fördert. Sein menschliches Äquivalent, HFM1, ist für die Fruchtbarkeit bekannt. Sie entdeckten, dass Mer3 direkt an RPA bindet, einen Proteinkomplex, der üblicherweise freiliegende einzelsträngige DNA umhüllt, um sie zu schützen und andere Reparaturfaktoren zu rekrutieren. Mit biochemischen Tests, Strukturmodellierung und Interaktionsassays kartierten die Forschenden eine spezifische Andockstelle, an der ein kurzer Schwanz von Mer3 in eine Furche einer RPA-Untereinheit passt. Diese Schnittstelle ist von Hefen bis zu Säugetieren konserviert, was darauf hindeutet, dass es sich um eine evolutionär bewährte Lösung handelt, die wiederholt zur Kontrolle der DNA-Reparatur in der Meiose eingesetzt wurde.
Beobachtung eines einzelnen DNA-Motors in Aktion
Um zu sehen, was diese Partnerschaft tatsächlich bewirkt, nutzten die Wissenschaftler Einzelmolekül-Magnetpinzetten — ein Instrument, das einen einzelnen DNA-Haarnadelstrang wie eine winzige Feder hält und misst, wie ein einzelnes Mer3-Molekül ihn im Lauf der Zeit aufwindet. Sie stellten fest, dass Mer3 auch allein mit konstanter Geschwindigkeit die DNA entlangläuft. Unter Bedingungen, die die relativ geringe physikalische Spannung innerhalb von Zellen nachahmen, neigt Mer3 jedoch dazu, die DNA nach dem Aufwinden nur eines kurzen Abschnitts loszulassen. In Anwesenheit einer geringen Menge RPA wird Mer3 plötzlich deutlich ausdauernder: Es kann weitaus längere DNA-Abschnitte aufwinden, ohne abzufallen, besonders wenn die DNA dazu neigt, wieder zusammenzufalten. Eine mutantische Version von Mer3, die so konstruiert wurde, dass der RPA-bindende Schwanz gestört ist, erwirbt diese erhöhte Ausdauer nicht, was zeigt, dass der direkte Kontakt mit RPA Mer3s Prozessivität verstärkt.
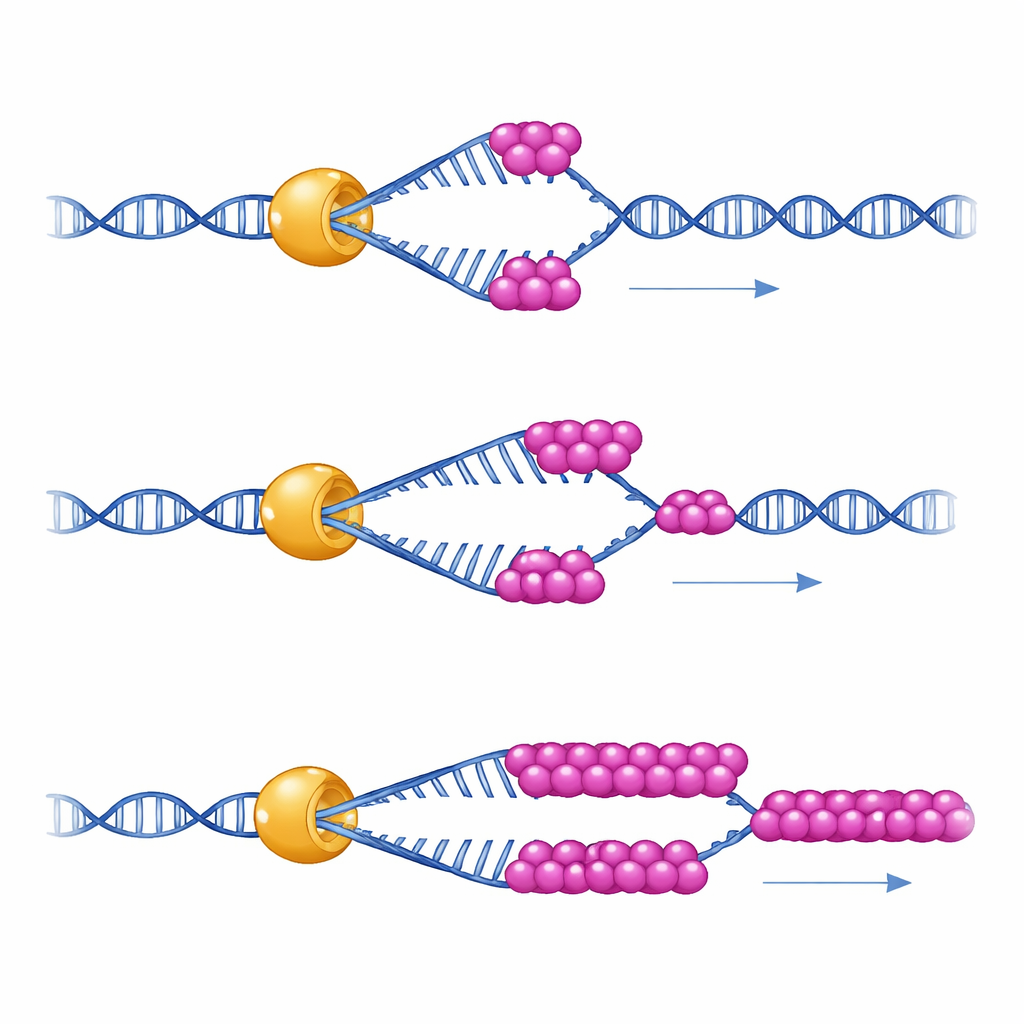
Folgen für Kreuzungen in lebenden Zellen
Das Team untersuchte anschließend, was in echten Hefezellen geschieht, wenn Mer3 RPA nicht richtig greifen kann. Sie ersetzten das normale MER3-Gen durch den RPA-bindenden Mutanten und beobachteten die Meiose. Diese Zellen konnten sich zwar noch teilen und Sporen bilden, doch ihre Fruchtbarkeit sank und die Gesamtanzahl der Kreuzungen in bestimmten Chromosomenregionen verringerte sich. Detaillierte DNA-Analysen zeigten mehr Reparaturereignisse, die als Nicht-Kreuzungen endeten, und eine Anhäufung nicht aufgelöster Rekombinationszwischenprodukte. Genomweite Kartierungen der Mer3-Standorte zeigten, dass das mutierte Protein weniger stabil an Stellen rekrutiert wurde, an denen programmierte DNA-Brüche auftreten, obwohl seine frühe Assoziation mit Chromosomenachsen normal erschien. Anders gesagt: Ohne starke RPA-Bindung verweilt Mer3 nicht lange genug an Bruchstellen, um sie zuverlässig in Richtung Kreuzungsresultate zu treiben.
Was das für Fruchtbarkeit und Genomstabilität bedeutet
Zusammengefasst zeigt die Studie, dass RPA mehr tut, als nur lose DNA zu umhüllen; es justiert direkt das Verhalten einer wichtigen meiotischen Helikase. Durch das Andocken an RPA wird Mer3 zu einem entschlosseneren DNA-Aufwinder, der in der Lage ist, gemeinsame DNA-Strukturen zu verlängern und zu stabilisieren, die zu Kreuzungen heranreifen. Wenn diese Interaktion abgeschwächt ist, neigen Zellen zu sichereren, aber weniger nützlichen Reparaturausgängen und hinterlassen mehr nicht aufgelöste Zwischenprodukte, was die Chromosomenverteilung subtil beeinträchtigt. Da dieselben molekularen Akteure auch beim Menschen vorkommen — und Mutationen in HFM1 mit Unfruchtbarkeit in Verbindung gebracht werden — liefert diese Arbeit einen mechanistischen Rahmen dafür, wie winzige Veränderungen an einer Proteinoberfläche bis hin zu Auswirkungen auf die reproduktive Gesundheit und die genetische Vielfalt künftiger Generationen reichen können.
Zitation: Altmannova, V., Orlić, L., Carrasco, C. et al. RPA directly stimulates Mer3 helicase processivity to ensure normal crossover formation in meiosis. Nat Commun 17, 2621 (2026). https://doi.org/10.1038/s41467-026-69985-x
Schlüsselwörter: Meiose, genetische Rekombination, DNA-Helikase, Fruchtbarkeit, Chromosomenkreuzung