Clear Sky Science · de
Dysregulation der DNA-Schadensantwort durch Phosphorothioat-Antisense-Oligonukleotide
Wenn nützliche Gentherapien die Reparaturmannschaft der Zelle in die Irre führen
Antisense-Oligonukleotide, kurz ASOs, sind eine wachsende Klasse präziser Medikamente, die entwickelt wurden, um einzelne Gene ein- oder auszuschalten. Sie werden bereits zur Behandlung einiger seltener genetischer Erkrankungen eingesetzt und für viele weitere Krankheiten getestet. Diese Studie zeigt eine unerwartete Kehrseite einer gängigen chemischen Modifikation, die diese Arzneimittel stabiler macht: Unter bestimmten Bedingungen kann sie die Zelle dazu verleiten, DNA-Schäden zu vermuten, die Reparaturmaschinerie blockieren und das Genom langfristig schädigen.
Designer-Gen-Schalter und ihr chemisches Upgrade
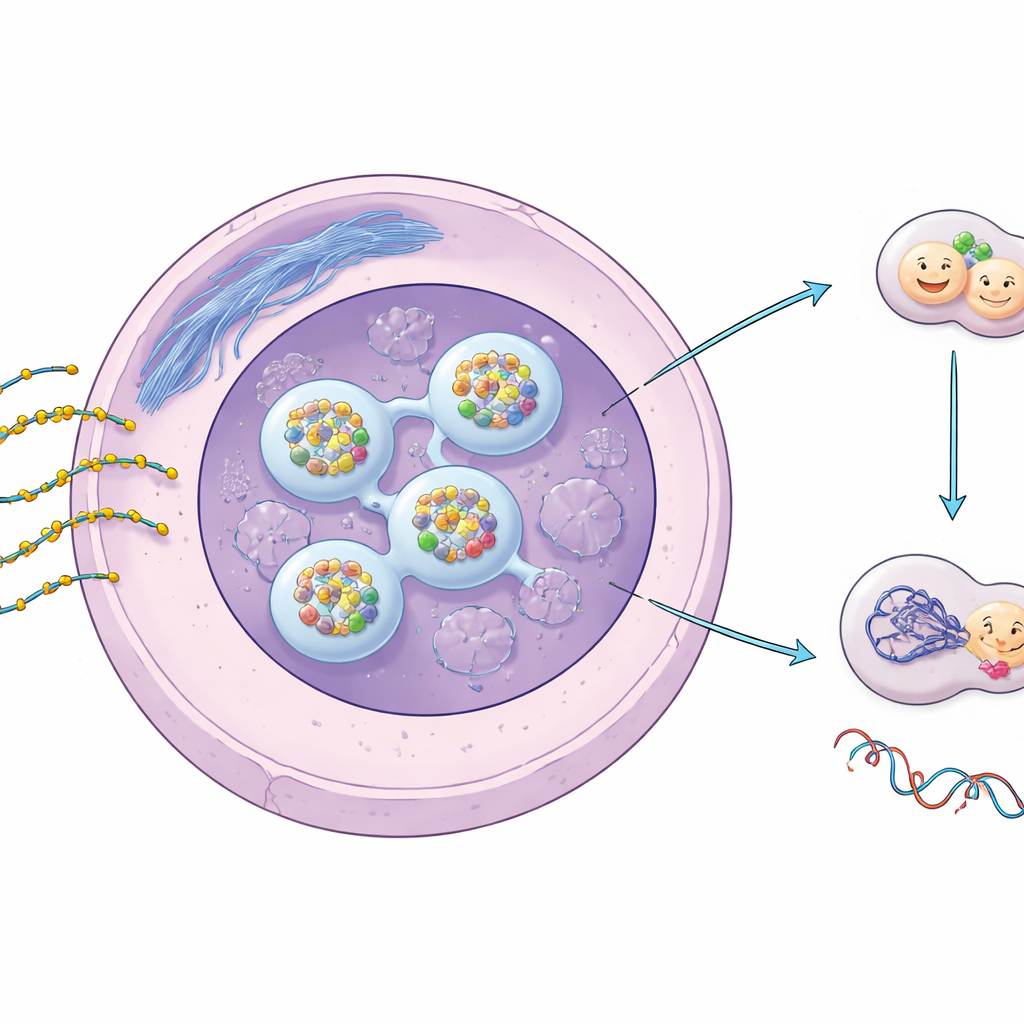
ASOs sind kurze, einzelsträngige Nukleinsäuresequenzen, die so konstruiert sind, dass sie spezifische RNA-Botschaften in unseren Zellen erkennen und binden, um diese stummzuschalten oder zu verändern. Um im Körper zu überleben und effizient in Zellen einzudringen, tragen die meisten therapeutischen ASOs eine Phosphorothioat-(PS-)Modifikation, bei der ein Schwefelatom ein Sauerstoffatom im Rückgrat ersetzt. Diese kleine Veränderung erhöht ihre Stabilität stark und verstärkt ihre Neigung, mit Proteinen zu interagieren. Frühere Arbeiten zeigten, dass sich PS-ASOs in bestimmten Bereichen des Zellkerns ansammeln und bestimmte nukleäre Strukturen belasten können, doch welche Bedeutung das für die DNA-Reparatur und die Langzeitsicherheit hat, war bisher unklar.
Künstliche Tröpfchen, die echte DNA-Reparaturstellen nachahmen
Die Autoren verfolgten fluoreszent markierte PS-ASOs in menschlichen Zellen und stellten fest, dass sich diese bei üblichen experimentellen Dosen schnell im Zellkern anreichern und neue kugelförmige Strukturen bilden, die als PS-Körper bezeichnet werden. Diese Körper entstehen konzentrationsabhängig und verhalten sich wie flüssige Tröpfchen, die verschmelzen, sich auflösen und von schwachen molekularen Kräften abhängen – Kennzeichen einer Flüssig‑Flüssig-Phasentrennung. Entscheidend ist, dass sie nicht dort liegen, wo tatsächliche DNA-Brüche auftreten, und nicht die üblichen Marker gebrochener DNA enthalten. Stattdessen zeigt die Studie, dass wichtige DNA-Reparaturenzyme – darunter DNA‑PKcs, ATM, ATR und PARP1 – direkt an die PS-ASOs binden und in diesen künstlichen Tröpfchen stark angereichert sind, obwohl die zugrunde liegende DNA intakt ist.
Falsche Alarme, die die Schadenssignale der Zelle auslösen
Einmal gebildet, tun die ASO-kernenden Tröpfchen mehr, als Proteine passiv zu fangen: Sie schalten die Reparaturenzyme ein. Innerhalb einer Stunde nach Eindringen der ASOs sind die Enzyme in diesen Tröpfchen aktiviert und beginnen, das benachbarte Chromatin zu modifizieren, indem sie Histonproteine mit chemischen Markierungen versehen, die normalerweise nach echtem DNA-Schaden sichtbar sind. Das löst die volle DNA-Schadensantwort aus – es werden weitere Reparaturfaktoren rekrutiert, Checkpoint-Signale aktiviert und die Aktivität der Zellzyklusmotoren, der CDKs, heruntergeregelt. Infolgedessen verlangsamen oder stoppen Zellen ihren Fortschritt durch wichtige Phasen des Zellzyklus, insbesondere an dem Punkt, an dem normalerweise überprüft wird, ob die DNA vor der Teilung intakt ist. In Mäusegehirnen, die einer klinisch relevanten ASO-Gabe ausgesetzt waren, beobachteten die Forscher ebenfalls vermehrte DNA-Schadenssignale in Regionen mit höherer ASO-Aufnahme, was darauf hinweist, dass diese Effekte nicht auf Zellkulturen beschränkt sind.
Fehlgeleitete Reparatur und eine wachsende Last an DNA-Brüchen
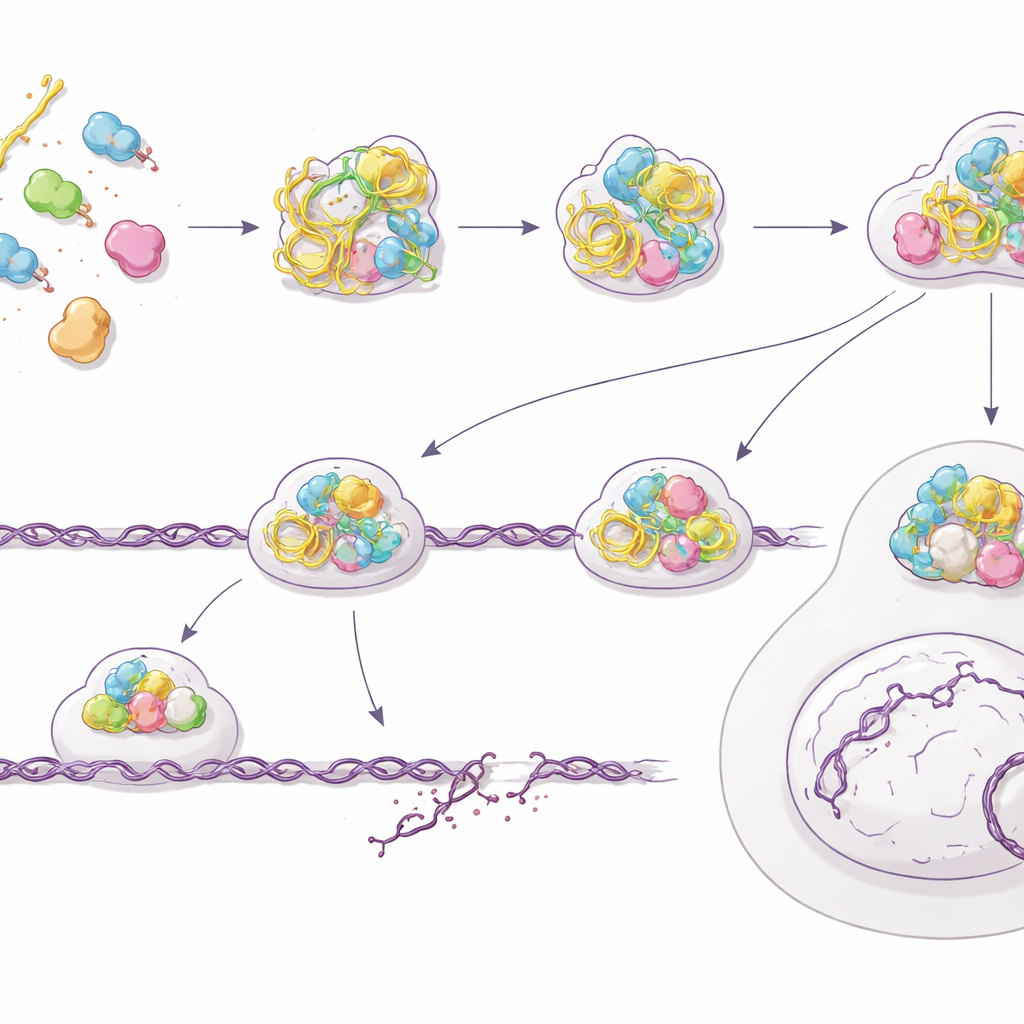
Paradoxerweise verschlechtert sich trotz des lauten Alarmsystems die tatsächliche Fähigkeit der Zelle, gefährliche DNA-Brüche zu reparieren. Das Team zeigte, dass Zellen, die zuvor mit PS-ASOs behandelt wurden, nach Bestrahlung Schwierigkeiten haben, Schäden zu beseitigen, und sogar mehr spontane Brüche akkumulieren, gemessen etwa mit Kometen-Assays und persistierenden Reparaturfoci. Ein genauerer Blick auf einen der präzisesten Reparaturwege der Zelle – die homologe Rekombination – offenbarte das Problem: Schlüsselakteure wie BRCA2 und RAD51 können sich nicht richtig an gebrochenen DNA-Enden zusammenlagern, während frühere Marker der Endverarbeitung weiterhin auftreten. Mithilfe eines genetischen Reporters quantifizierten die Autoren einen Rückgang der Effizienz der homologen Rekombination um etwa 60 % nach PS-ASO-Exposition. Die Zellen werden insgesamt weniger lebensfähig und deutlich strahlungsempfindlicher, was zu einem Bild passt, in dem das Reparatursystem zwar signalisiert, aber nicht korrekt eingesetzt wird.
Was das für die Zukunft genzielter Medikamente bedeutet
Zusammengefasst legt die Studie nahe, dass PS-modifizierte ASOs künstliche flüssigkeitsartige Tröpfchen im Zellkern nucleieren können, die DNA-Reparaturenzyme konzentrieren und aktivieren, selbst wenn es keinen Schaden zu reparieren gibt. Dieser chronische Fehlalarm stört normale Reparaturentscheidungen, insbesondere die präzise homologe Rekombination, und führt zu anhaltenden DNA-Läsionen, Checkpoint-Aktivierung und Zelltod. Während die stärksten Effekte bei hohen nukleären ASO-Spiegeln beobachtet werden, wie sie für Transfektionsversuche typisch sind, ist eine subtile Aktivierung der Schadenssignale selbst bei niedrigeren, arzneimittelähnlichen Dosen nachweisbar. Für Patienten und Wirkstoffentwickler ist die Botschaft klar: Die chemischen Eigenschaften, die ASOs zu wirksamen Medikamenten machen, können in bestimmten Kontexten das grundlegendste Sicherheitsmerkmal der Zelle beeinträchtigen – ihre Fähigkeit, ein stabiles Genom zu erhalten – und unterstreichen die Notwendigkeit, sicherere Rückgrate zu entwickeln und die DNA-Reparaturwege während der Therapie zu überwachen.
Zitation: Hjelmgren, L., Zhou, Q., Schmidli, S. et al. Dysregulation of the DNA damage response by phosphorothioate antisense oligonucleotides. Nat Commun 17, 2111 (2026). https://doi.org/10.1038/s41467-026-69980-2
Schlüsselwörter: Antisense-Oligonukleotide, DNA-Schadensantwort, phasengetrennte Flüssigkeitsbildung, homologe Rekombination, Genomstabilität