Clear Sky Science · de
Chirale Peptidoglykansch mimikriert bakterielle Wandbiosynthese als Angriffspunkt gegen Krankheitserreger
Eine neue Methode, schädliche Keime aufzuspüren
Infektionen mit antibiotikaresistenten Erregern nehmen weltweit zu, dennoch fehlen Ärzten präzise Werkzeuge, die gefährliche Bakterien erkennen und angreifen, ohne unsere eigenen Zellen zu schädigen. Diese Studie stellt einen raffinierten molekularen „Köder“ vor, der einen zentralen Baustein der bakteriellen Zellwand nachahmt. Diese Designer‑Moleküle können Infektionen sowohl für die Bildgebung sichtbar machen als auch Antibiotika direkt zu den Mikroben transportieren und bieten so eine neue Strategie gegen schwer behandelbare Krankheitserreger.
Die Rüstung der Bakterien nachahmen
Bakterien sind von einem robusten Geflecht umgeben, der Zellwand, die aus Zuckern und ungewöhnlichen spiegelbildlichen Aminosäuren aufgebaut ist, die in unseren Zellen kaum vorkommen. Die Forschenden nutzten diesen Unterschied, indem sie lange zuckerbasierte Ketten mit einer spezifischen spiegelbildlichen Form von Alanin dekorierten, einer verbreiteten Aminosäure. Diese Ketten, sogenannte chirale Peptidoglykansch‑Mimics, sind so gestaltet, dass sie den natürlichen Bausteinen der bakteriellen Wand sehr ähnlich sehen, in Säugetiergeweben jedoch fehlen. Durch Feinabstimmung des Anteils an diesem D‑förmigen Alanin erzeugte das Team Varianten, die Bakterien deutlich stärker bevorzugten als menschliche Zellen.
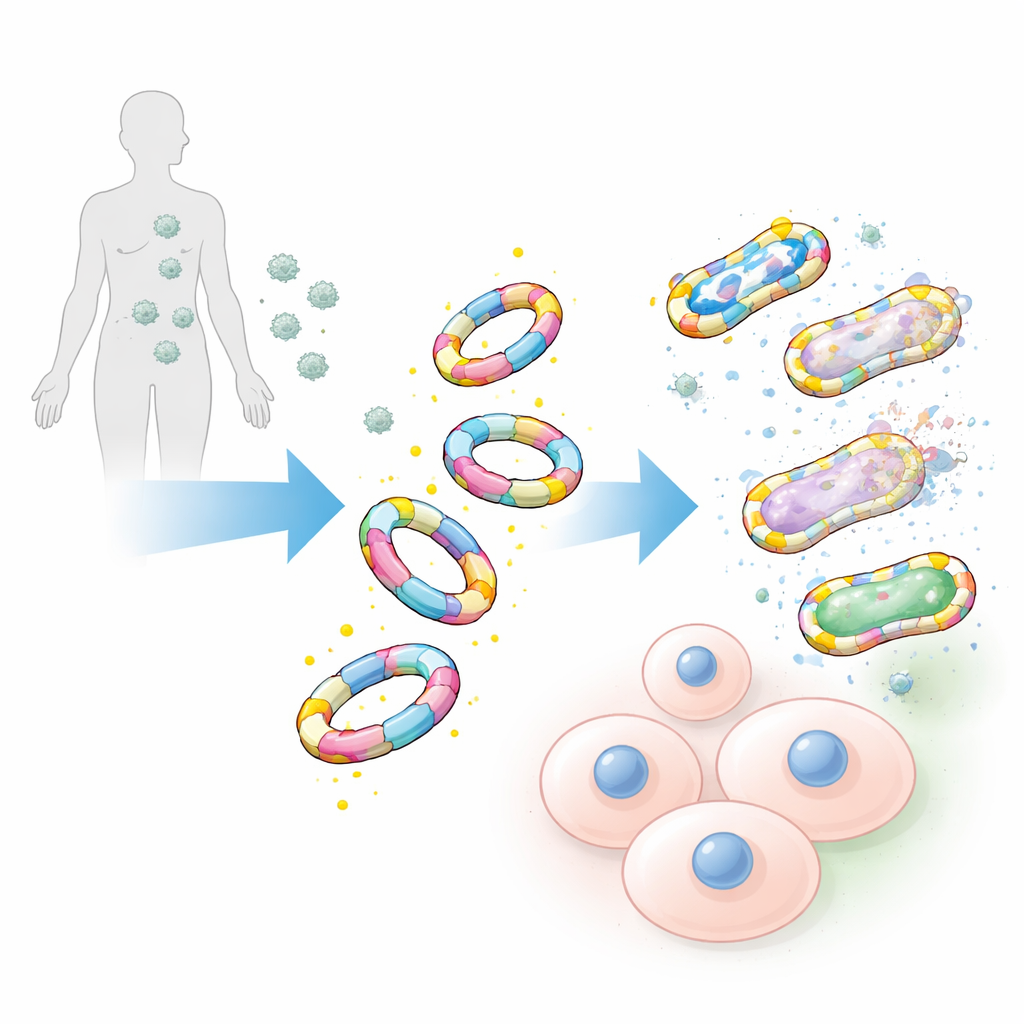
Festhalten an Bakterien, nicht an unseren Zellen
Getestet gegen eine breite Palette von Erregern, darunter gefürchtete Klinikstämme wie Methicillin‑resistenter Staphylococcus aureus und andere ESKAPE‑Bakterien, banden die mit D‑Alaninen versehenen Mimics die bakteriellen Oberflächen mit auffälliger Effizienz. Ihre spiegelbildlichen Gegenstücke aus der L‑Form von Alanin sowie die reinen Zuckerketten zeigten nur schwache oder vernachlässigbare Bindung. Das Team verglich diese großen Mimics außerdem mit herkömmlichen kleinen chemischen Sonden, die auf einzelnen D‑Alanin‑Molekülen basieren. Selbst wenn die kleinen Sonden extrem hell gemacht wurden, markierten sie deutlich weniger Bakterien und lieferten schwächere Signale, was die Überlegenheit des größeren, lebensechteren Designs unterstreicht.
Die Zellwand‑Fertigungsstraße kapern
Um zu verstehen, wie die Erkennung so stark wird, untersuchten die Wissenschaftler, wie die Mimics mit der bakteriellen Wandbau‑Maschinerie interagieren. Sie stellten fest, dass die D‑Alaninhaltigen Ketten nicht nur an der Oberfläche haften; sie werden aufgenommen, als wären sie echte Bausteine, und in dieselben enzymatischen Schritte eingespeist, die normalerweise Wandkomponenten verknüpfen. Chemische Analysen detektierten neue Zwischenprodukte, die nur in Anwesenheit dieser Mimics entstehen, und Computersimulationen zeigten, dass Schlüsselenzyme des Wandaufbaus die Mimics noch fester greifen als die natürlichen Substrate. Über mehrere Wachstumszyklen hinweg reichten die Mimics in der Wand ein und verzerrten ihre Struktur zunehmend, wodurch sie durchlässig wurde.
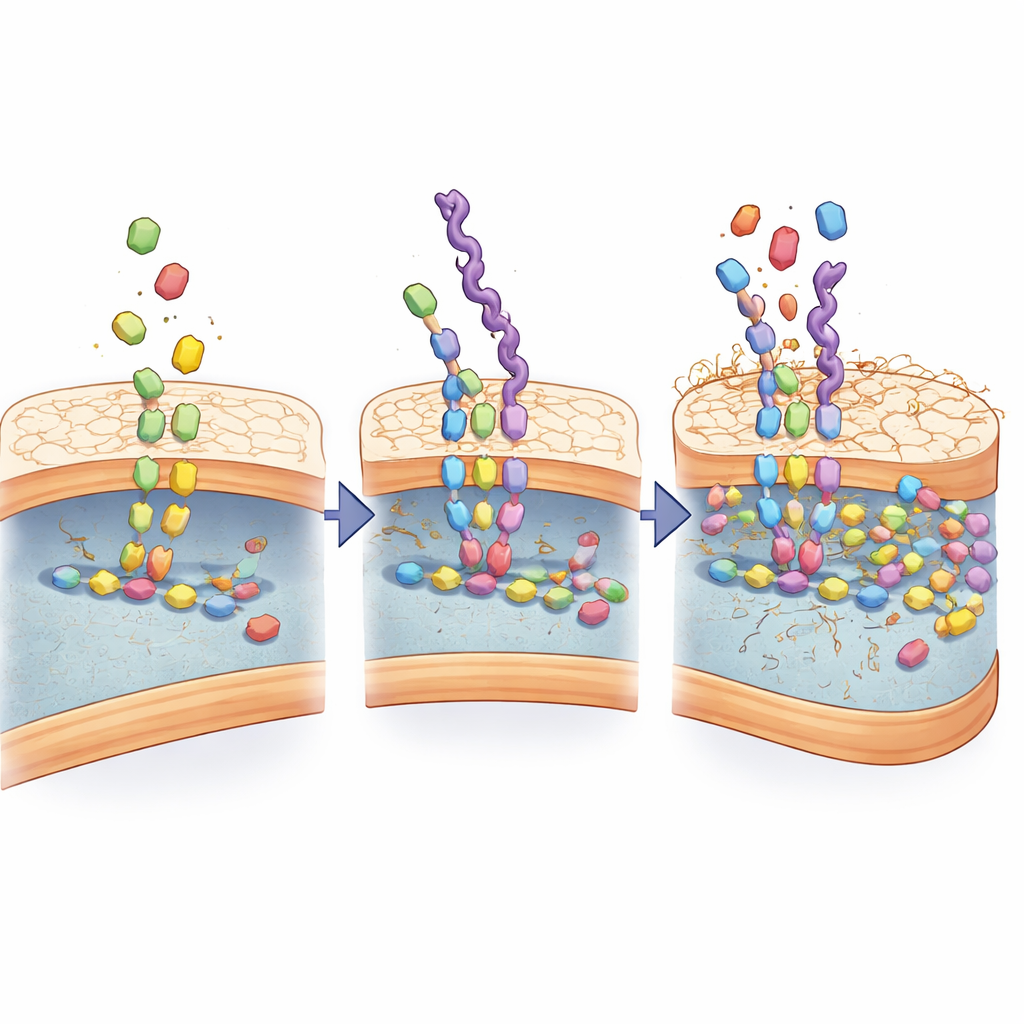
Mimics als intelligente Wirkstoffträger nutzen
Da diese Ketten sich in Wasser naturgemäß zu winzigen Partikeln zusammenlagern und viele chemische Ansatzpunkte bieten, nutzte das Team sie als Gerüst für Bildgebungssonden und Antibiotika. Fluoreszierende Varianten zeichneten Bakterien in Zellkulturen deutlich nach, während sie kaum mit benachbarten Säugetierzellen interagierten. Die Forschenden luden dann das Antibiotikum Tetracyclin in die mimic‑basierten Partikel. In Labortests machte diese Verpackung Tetracyclin mehrfach wirksamer und tötete sogar resistente Stämme bei deutlich niedrigeren Dosen als das freie Medikament. Die Mikroskopie zeigte, dass die antibiotikobeladenen Mimics sich dicht an Bakterien anlagerten, deren Hülle durchdrangen und im Vergleich zu nicht zielgerichteten Formulierungen umfangreichen Zelltod auslösten.
Infektionen im Körper bekämpfen
Die härtesten Prüfungen fanden in Mausmodellen lokal begrenzter Hautwunden und lebensbedrohlicher Bauchfellentzündungen statt. In infizierten Wunden suchten die fluoreszierenden Mimics tief im Gewebe nach Bakterien und beseitigten die Keime, wenn sie Tetracyclin trugen, nahezu vollständig. Das führte zu schnellerer Heilung, dickerer neuer Haut, geordneterer Kollagenablagerung und verstärktem Wachstum kleiner Blutgefäße. In systemischen Infektionsmodellen reichten die Mimics gezielt in infizierte Organe wie Milz und Lunge, wo sie bei Beladung mit Antibiotikum die Bakterienzahlen stark reduzierten. Wichtig ist, dass auch hohe Dosen der Mimics allein eine gute Verträglichkeit zeigten, ohne erkennbare Schäden an wichtigen Organen oder der Blutchemie.
Welche Bedeutung das für künftige Therapien haben könnte
Indem sie ein enges chemisches Ebenbild der natürlichen Bausteine der bakteriellen Zellwand bauen, zeigt diese Arbeit einen neuen Weg, sich in den Stoffwechsel eines Erregers „einzuschleichen“, anstatt ihn nur von außen anzugreifen. Diese chiralen Mimics dienen sowohl als hochpräzise Leuchttürme für die Bildgebung als auch als intelligente Vehikel, die Antibiotika direkt zu ihren mikrobiellen Zielen lenken, einschließlich resistenter Stämme, und dabei Säugetierzellen schonen. Wenn sich diese biomimetischen Plattformen klinisch übersetzen lassen, könnten sie Ärzten helfen, Infektionsherde genau zu lokalisieren und mit geringeren Wirkstoffdosen effektiver zu behandeln — ein vielversprechendes Werkzeug im Kampf gegen die zunehmende Herausforderung der antimikrobiellen Resistenz.
Zitation: Deng, K., Zou, D., Zeng, Z. et al. Chiral peptidoglycan mimics target bacterial wall biosynthesis for pathogen intervention. Nat Commun 17, 3258 (2026). https://doi.org/10.1038/s41467-026-69967-z
Schlüsselwörter: Antibiotikaresistenz, bakterielle Zellwand, gezielte Wirkstofffreisetzung, molekulare Bildgebung, Nanomedizin