Clear Sky Science · de
Vollständige Defluorierung von PFAS durch photokatalytische Reduktion im Wasser
Warum das Aufbrechen von „Forever Chemicals“ endlich möglich erscheint
Seit Jahrzehnten reichert sich eine Gruppe von Schadstoffen, bekannt als PFAS – oft „Forever Chemicals“ genannt – in Trinkwasser, Wildtieren und sogar im menschlichen Blut an, weil sie in der Natur kaum zerfallen. Diese Studie beschreibt ein neues lichtbetriebenes Material, das einige der hartnäckigsten PFAS im Wasser nahezu vollständig von Fluoratomen befreien kann und sie in harmlose kleine Moleküle umwandelt, ohne starke Chemikalien oder teure Energieeinsätze zu benötigen. Das macht es zu einem vielversprechenden Konzept für eine sicherere und praktischere Reinigung kontaminierter Wasserressourcen.
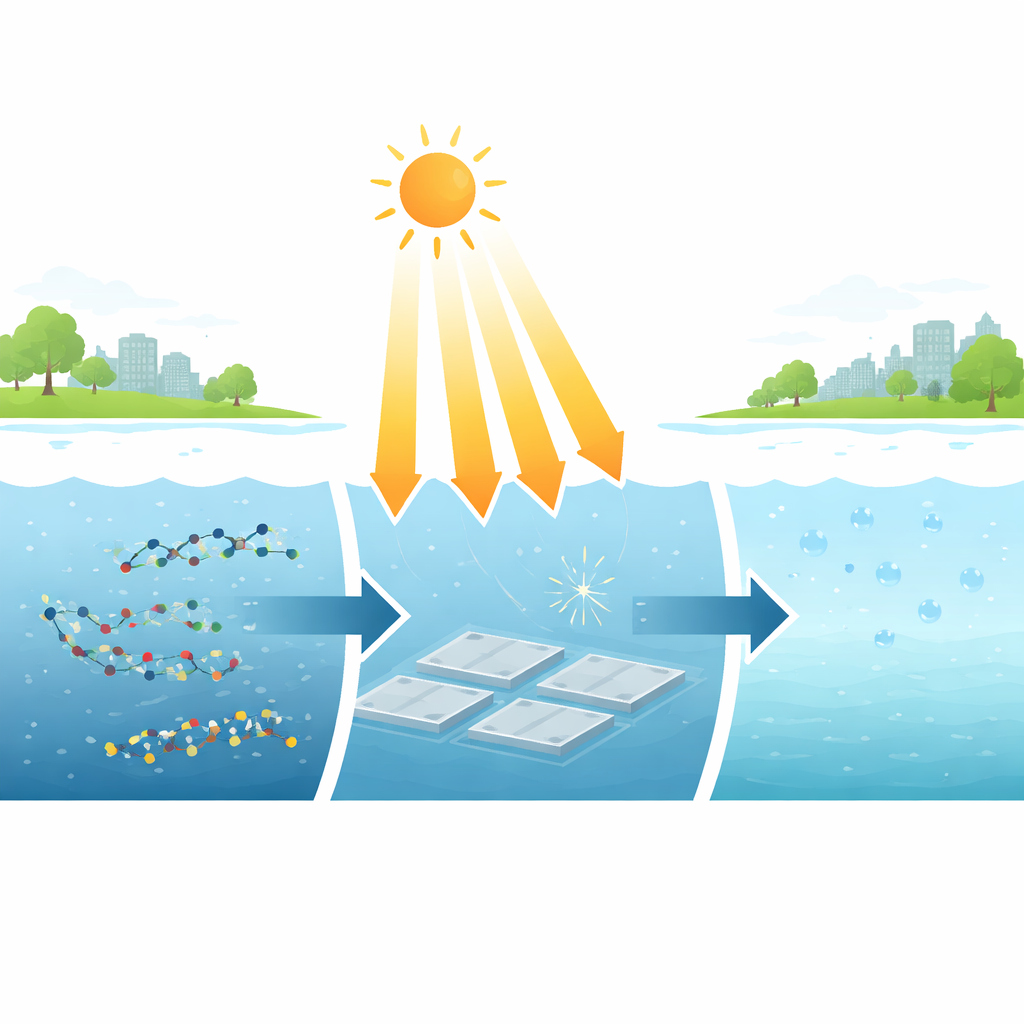
Das Problem mit hartnäckigen fluorierten Schadstoffen
PFAS (per- und polyfluorierte Alkylsubstanzen) werden in Antihaftpfannen, Löschschaum und schmutzabweisenden Beschichtungen verwendet. Ihre Kohlenstoff–Fluor-Bindungen gehören zu den stärksten in der Chemie, weshalb PFAS in der Umwelt verbleiben und sich in Organismen anreichern. Zwei der am weitesten verbreiteten PFAS, PFOA und PFOS, sind inzwischen als krebserzeugend für den Menschen eingestuft, und Länder haben Trinkwassergrenzwerte im Billionstelbereich (parts-per-trillion) festgelegt. Leider funktionieren die meisten bestehenden Methoden, die PFAS wirklich zerstören können – wie intensiver Ultraschall, Hochtemperaturbehandlung oder starke chemische Zusätze – nur bei hohen Konzentrationen und erfordern große Energiemengen, was ihre Skalierung für die Praxis erschwert.
Ein neuer, lichtgetriebener Katalysator für extreme Bindungen
Die Forschenden entwickelten ein spezielles organisches Material namens TAPP, das sich selbst zu geordneten Stapeln flacher Moleküle anordnet. Bei Beleuchtung mit sichtbarem Licht bilden diese Stapel einen langlebigen Radikalzustand – eine Version des Moleküls mit einem ungepaarten Elektron –, der in Luft länger als eine Woche stabil bleibt. Da die elektrische Ladung über das Molekül und seine angehängten Aminogruppen verteilt ist, kann dieses Radikal eine zweite Lichtdosis aufnehmen und Elektronen auf extrem hohe Energien bringen. Diese energetisierten Elektronen sind stark genug, um die ultrastabilen Kohlenstoff–Fluor-Bindungen in PFAS anzugreifen, etwas, das gewöhnliche lichtbasierte Katalysatoren nicht leisten können.
Wie der Katalysator PFAS anzieht und zerlegt
Die TAPP-Partikel sind im Wasser positiv geladen, während PFOS und verwandte PFAS an einem Ende negative Ladungen und am anderen fluorierte Ketten tragen. Dieser Gegensatz zieht die Schadstoffe auf die Katalysatoroberfläche: Die negativ geladenen Kopfgruppen interagieren mit protonierten Aminostellen, und die fluorierte Kette liegt entlang der flachen aromatischen Oberfläche durch schwache Anziehungskräfte. Nach diesem „Vorkonzentrations“-Schritt regt sichtbares Licht TAPP wiederholt an. Seine Radikalform sendet hochenergetische Elektronen direkt in die antibindenden Bereiche der Kohlenstoff–Fluor-Bindungen der PFAS. Dieses zusätzliche Elektron destabilisiert die starre, helikale Struktur der PFAS-Kette, dehnt das Kohlenstoffgerüst und macht einzelne C–F-Bindungen deutlich leichter brechbar.
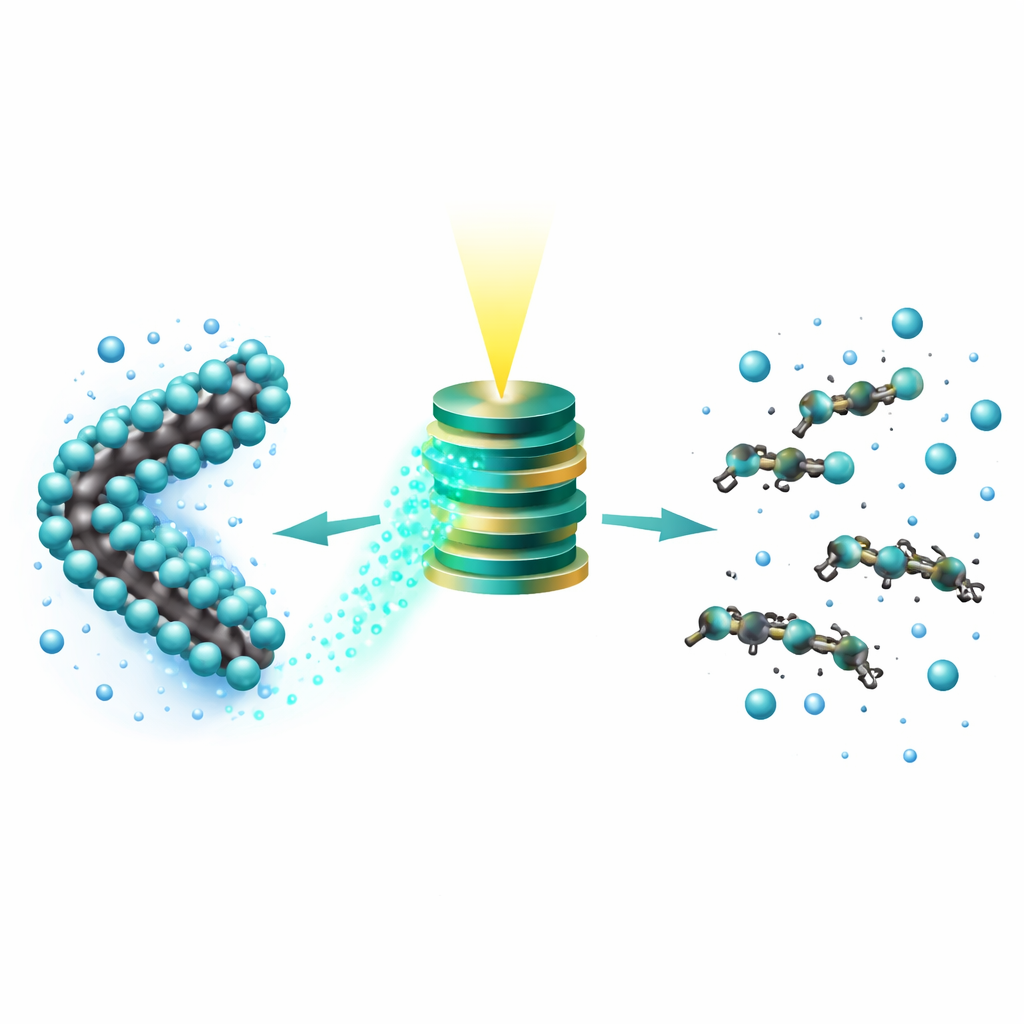
Von tödlichen Ketten zu harmlosen Fragmenten
In sorgfältig kontrollierten Wasserexperimenten mit realistischen Kontaminationsniveaus (etwa 0,1 Teile pro Million) entfernte TAPP PFOS aus der Lösung und wandelte unter Lichteinfluss nahezu all sein Fluor innerhalb von etwa zwei Tagen in freie Fluoridionen um. Detaillierte chemische Analysen zeigten, dass das ursprüngliche PFOS-Signal verschwand und durch einfache organische Säuren wie Formiat, Oxalat und Lactat ersetzt wurde, ohne dass PFOS auf der Katalysatoroberfläche zurückblieb. Früh im Reaktionsverlauf detektierte das Team eine Reihe kürzerer fluorierter Fragmente, was das Bild stützt, dass Elektronen zunächst Fluor aus der Kette entfernen; das dadurch geschwächte Kohlenstoffgerüst zerfällt dann in kleinere Stücke, die weiter zu harmlosen Endprodukten oxidiert werden.
Leistung in realem Wasser und Energieeinsparung
Um die Praktikabilität zu prüfen, bauten die Wissenschaftler eine kleine Außenreaktor-Anlage, die eine Behandlungseinheit einer Kläranlage nachbildet. Mit nur natürlichem Sonnenlicht defluorierte ihr TAPP-basiertes System PFOS-belastetes Wasser in drei Tagen vollständig. Der Katalysator arbeitete gut auch in Gegenwart natürlicher organischer Substanz und häufiger Ionen, obwohl einige Salze den Prozess verlangsamten, weil sie um Bindungsstellen auf der Oberfläche konkurrierten. Im Vergleich zu anderen lichtgetriebenen PFAS-Behandlungen verbrauchte dieser Ansatz etwa 90–98 % weniger Energie pro Wasservolumen und verkam auf giftige Metalle oder zugesetzte Oxidationsmittel. Der Katalysator blieb zudem für mindestens fünf wiederholte Zyklen mit minimalem Effizienzverlust aktiv.
Was das für die Reinigung von „Forever Chemicals“ bedeutet
Diese Arbeit zeigt, dass sorgfältig konstruierte organische Materialien gewöhnliches sichtbares Licht nutzen können, um Elektronen zu erzeugen, die energiereich genug sind, die stärksten Kohlenstoff–Fluor-Bindungen in PFAS aufzubrechen, und das alles in einfachem Wasser ohne Opferchemikalien. Durch die Kombination starker Schadstoffadsorption, eines langlebigen Radikalzustands und mehrstufiger Photoanregung verwandelt der TAPP-Katalysator persistenten PFAS in Fluorid und kleine, harmlose organische Moleküle. Obwohl die Skalierung und die Bewältigung der gesamten Vielfalt von PFAS noch Zeit erfordern, bietet diese Studie einen realistischen Weg zu solarbetriebener, kostengünstiger Zerstörung von „Forever Chemicals“ in Trinkwasser- und Abwassersystemen.
Zitation: Chong, M., Zhou, Q., Xu, J. et al. Complete defluorination of PFASs via photocatalytic reduction in water. Nat Commun 17, 3081 (2026). https://doi.org/10.1038/s41467-026-69933-9
Schlüsselwörter: PFAS-Beseitigung, Photokatalyse, Wasseraufbereitung, Defluorierung, Umweltchemie