Clear Sky Science · de
VAMP7‑abhängige späte endosomale Sekretion von ER‑ und mitochondrialen Proteinen beeinflusst das Tumormikromilieu und die Makrophagen‑Interaktion
Wie gestresste Zellen um Hilfe signalisieren
Krebszellen haben einen harten Alltag. Von Sauerstoff und Nährstoffen entbehrend, häufen sie Schäden in den winzigen Kraftwerken (Mitochondrien) und den Proteinfabriken (endoplasmatisches Retikulum, kurz ER) in ihrem Inneren an. Diese Studie zeigt einen unerwarteten Mechanismus, mit dem belastete Zellen beschädigte Teile dieser inneren Strukturen nach außen abgeben. Bei Hirntumoren, den Glioblastomen, beeinflusst dieses zelluläre „Müllentsorgungssystem“, gesteuert von einem Protein namens VAMP7, wie Immunzellen das Tumorareal wahrnehmen und betreten.
Verborgene Transportwege innerhalb der Zelle
Die meisten Proteine, die eine Zelle verlassen, nutzen einen klassischen Weg: Sie gelangen ins ER, passieren eine zentrale Sortierstelle, den Golgi-Apparat, und werden dann in kleine Bläschen verpackt, die mit der Zelloberfläche verschmelzen. Zellen bedienen sich jedoch auch unkonventioneller Wege, die den Golgi umgehen. Einer dieser Wege nutzt späte Endosomen — interne Säckchen, die mit der Oberfläche verschmelzen und ihren Inhalt nach außen freisetzen können. Die Autoren konzentrieren sich auf ein molekulares „Reißverschluss“-Protein, VAMP7, das bereits dafür bekannt ist, späten Endosomen bei der Fusion mit der Außenmembran zu helfen und kleine extrazelluläre Vesikel freizusetzen, winzige Pakete, die Fracht zwischen Zellen transportieren.
Abgenutzte Teile auf den Weg nach draußen bringen
Anhand gentechnisch veränderter Ratten‑Nieren‑ und Gliomazellen ohne VAMP7 verfolgten die Forschenden, was mit Proteinen geschieht, die normalerweise im ER und in Mitochondrien vorkommen. Sie zeigten, dass Zellen ohne VAMP7 deutlich weniger einer kurzen Form des ER‑gestaltenden Proteins RTN3 und von VDAC, einem Kanal auf der mitochondrialen Oberfläche, freisetzten. Gleichzeitig waren späte Endosomen fehlpositioniert und kleine Vesikel, die reich an dem Marker CD63 sind, wurden schlecht sezerniert. Hochauflösende Bildgebung und Proximity‑Assays zeigten, dass RTN3 und mitochondriales Material physisch mit CD63‑positiven späten Endosomen assoziieren, bevor sie freigesetzt werden, und dass diese Übergabe von VAMP7 und seinen Partner‑Fusionsproteinen abhängt. Diese Befunde stützen ein Modell, in dem gestresstes ER und Mitochondrien kleine Vesikel abschnüren, die mit späten Endosomen fusionieren, welche dann ihre Ladung aus der Zelle exportieren. 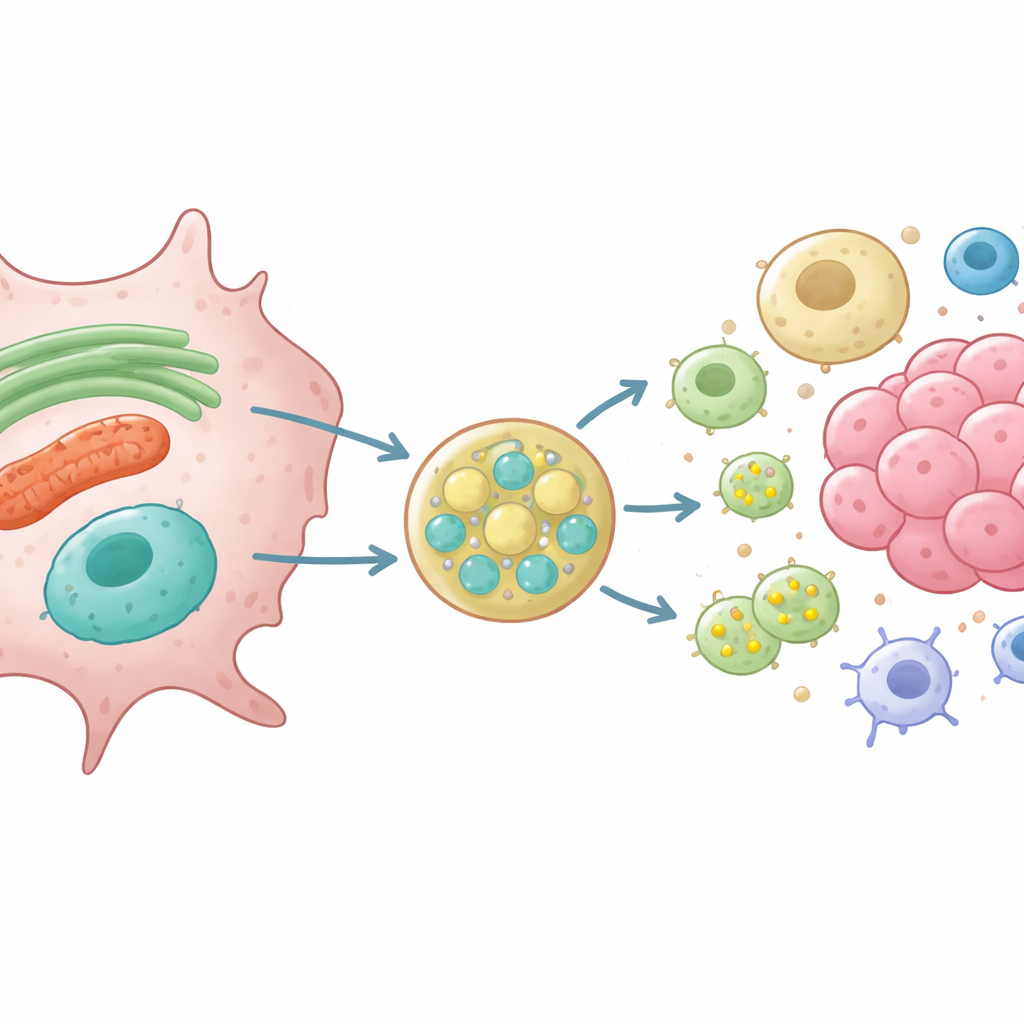
Stressabbau und Qualitätskontrolle
Zellen ohne VAMP7 verloren nicht den allgemeinen Recyclingweg, die Autophagie, zeigten jedoch deutliche Anzeichen von Belastung. Genexpressionsmuster deuteten auf die Aktivierung von Stressantworten im ER und auf Veränderungen in mitochondrienbezogenen Genen hin. Die Mikroskopie enthüllte abnorme „Wirbel“ aus ER‑Membran und übermäßig verschmolzene, verlängerte Mitochondrien — beides Kennzeichen von Organellen, die Schwierigkeiten haben, ihr Gleichgewicht zu halten. Messungen des Sauerstoffverbrauchs zeigten, dass trotz höherer mitochondrialer Masse Zellen ohne VAMP7 oder ohne ein essentielles Autophagieprotein (ATG5) eine schwächere Energieproduktion aufwiesen. Als die Forschenden gezielt ER‑ oder Mitochondrienstress mit Medikamenten auslösten, erhöhten Zellen mit intaktem VAMP7 die Sekretion von RTN3 bzw. VDAC. Dieser Anstieg ging verloren, wenn VAMP7 entfernt wurde, was darauf hindeutet, dass die späte endosomale Sekretion als Druckventil wirkt, um beschädigte Komponenten zu entsorgen und den inneren Zustand der Zelle nach außen zu melden.
Gestaltung der Tumornachbarschaft
Um die Bedeutung dieses Wegs für die Krankheit zu prüfen, verwendete das Team ein Rattenmodell des Glioblastoms, eines hochaggressiven Hirntumors. Sie implantierten normale, VAMP7‑defiziente oder ATG5‑defiziente Gliomazellen in Rattenhirne. Aus VAMP7‑freien Zellen entstehende Tumoren wuchsen groß und enthielten deutlich mehr abgestorbenes Gewebe, wurden jedoch von weniger Makrophagen infiltriert — den Immunzellen, die Trümmer aufnehmen und beeinflussen können, ob ein Tumor wächst oder stoppt. Im Gegensatz dazu waren Tumoren ohne ATG5 insgesamt kleiner, zeigten aber nicht denselben selektiven Rückgang der Makrophageneinwanderung in den Tumorkern. Analysen von menschlichen Hirntumordatensätzen zeigten ferner, dass niedrigere VAMP7‑ (und RTN3‑)Expression mit schlechterem Überleben der Patienten verbunden ist, was darauf hindeutet, dass dieser stress‑verknüpfte Sekretionsweg natürlicherweise das Tumorwachstum durch Gestaltung der Immunlandschaft bremsen könnte. 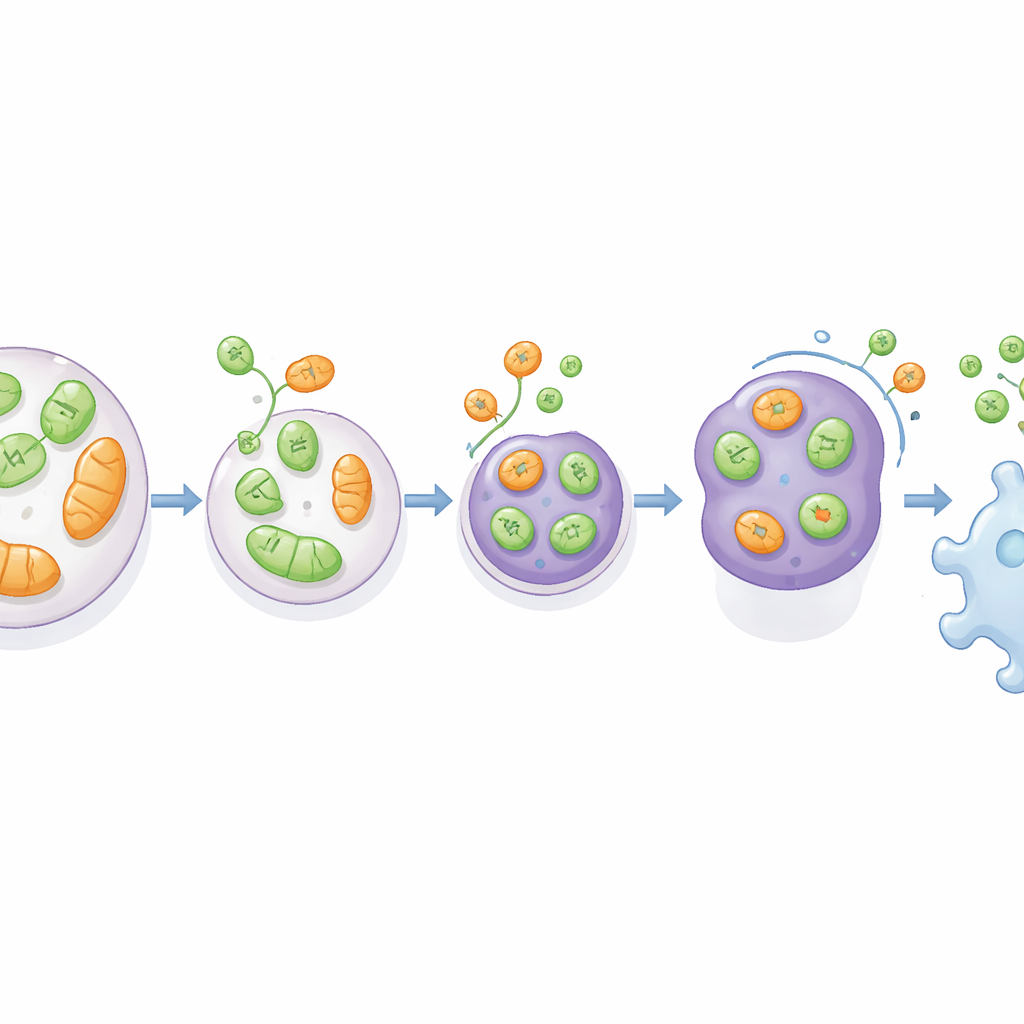
Warum das für Krebs und Immunität wichtig ist
Kurz gesagt schlagen die Autoren vor, dass VAMP7 Zellen dabei hilft, beschädigte Teile ihrer inneren Maschinerie über späte Endosomen zu verpacken und zu exportieren, besonders unter Stress. Beim Glioblastom scheint dieser Ausfluss von ER‑ und mitochondrien‑abgeleitetem Material als Notruf zu dienen, der Makrophagen dazu anregt, in den Tumor einzudringen und Trümmer zu beseitigen, was zu einem tumorhemmenden Milieu beiträgt. Fehlt VAMP7, schwächt das Signal ab, Organellschäden häufen sich, Tumoren werden nekrotischer und die Makrophagenbeteiligung nimmt ab. Das Verständnis und gegebenenfalls die Modulation dieses sekretorischen Qualitätskontrollsystems könnte neue Wege eröffnen, hartnäckige Tumoren für das Immunsystem sichtbarer und empfänglicher zu machen.
Zitation: Vats, S., Dionisio, P., Lemercier, Q. et al. VAMP7-dependent late endosomal secretion of ER and mitochondrial proteins impacts the tumor microenvironment and macrophage engagement. Nat Commun 17, 3012 (2026). https://doi.org/10.1038/s41467-026-69900-4
Schlüsselwörter: unkonventionelle Proteinsekretion, VAMP7, Glioblastom, Tumormikromilieu, extrazelluläre Vesikel