Clear Sky Science · de
Der Eukaryoten-Initiationsfaktor 6 steuert die Plastizität kleinzelliger Lungenkarzinome über die Integrin-FAK-Signalachse
Warum diese Lungenkrebsforschung wichtig ist
Das kleinzellige Lungenkarzinom (SCLC) gehört zu den tödlichsten Formen von Lungenkrebs. Zwar sprechen diese Tumoren anfangs meist gut auf Chemotherapie an, doch fast immer kommt die Erkrankung schnell und aggressiv zurück. Diese Studie stellt eine zentrale Frage: Was erlaubt SCLC‑Zellen, ihre „Persönlichkeit“ zu ändern und medikamentenresistent zu werden, und lässt sich dieses Formwandeln verlangsamen oder blockieren?
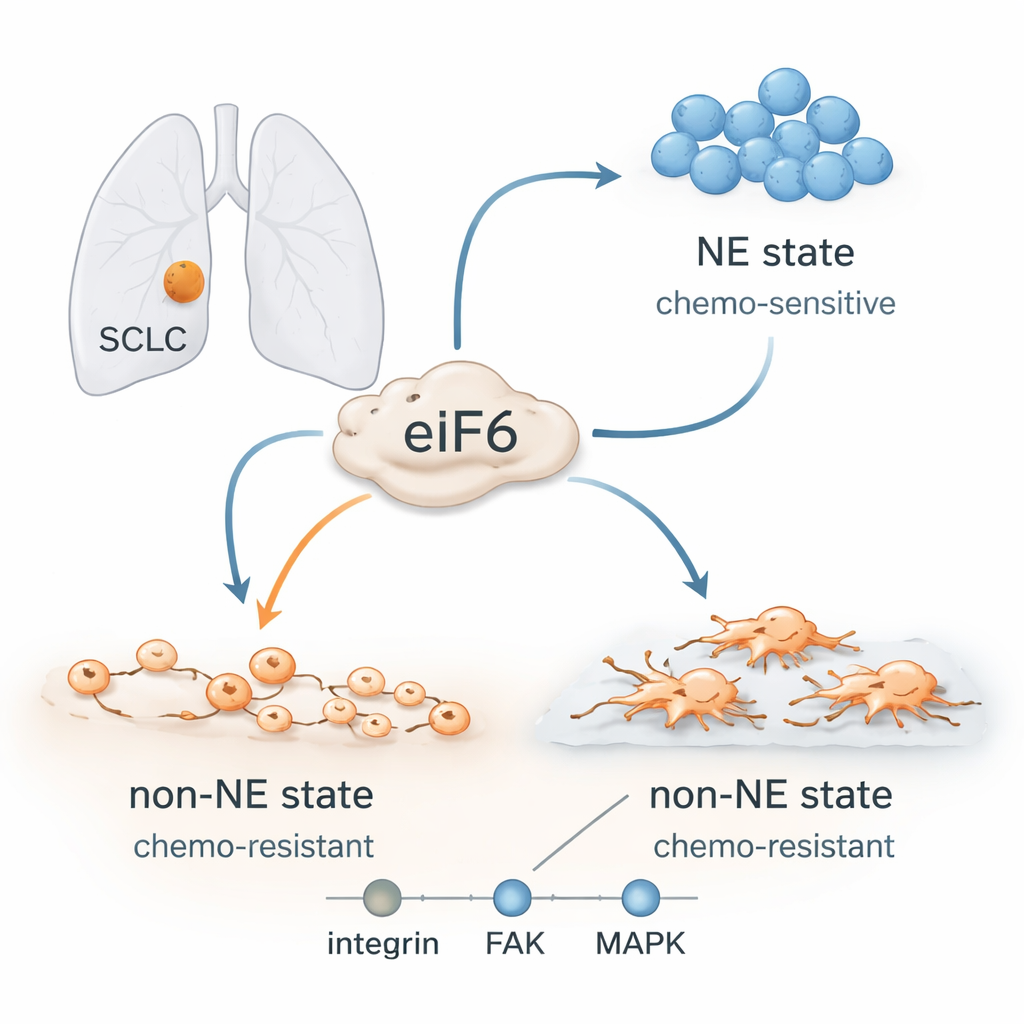
Formwandelnde Krebszellen
Ärzte gingen früher von einer einheitlichen Krankheit aus, doch inzwischen ist klar, dass SCLC‑Tumoren verschiedene Zelltypen enthalten. Einige Zellen haben eine starke „neuroendokrine“ Identität: Sie wachsen in dichten, schwebenden Clustern, sprechen gut auf platinbasierte Chemotherapie an und sind reich an bestimmten nervenähnlichen Proteinen. Andere verlieren diese Identität und nehmen einen „nicht‑neuroendokrinen“ Zustand an: Sie sind ausgebreiteter, haften an umgebendem Gewebe, zeigen Merkmale beweglicher, invasiver Zellen und sind deutlich schwerer mit Medikamenten zu töten. Tumoren von Patientinnen und Patienten wandeln sich während oder nach der Behandlung häufig vom empfindlichen in den resistenten Zustand, obwohl sich ihre DNA kaum verändert. Das spricht dafür, dass flexible Zellprogramme statt neuer Mutationen Rückfälle antreiben.
Ein Translationsfaktor mit Doppelfunktion
Die Autoren konzentrierten sich auf ein Protein namens eIF6, das vor allem für die Zusammenbauhilfe von Ribosomen, den Proteinfabriken der Zelle, bekannt ist. Anhand von Patientenproben, Mausmodellen und mehreren menschlichen SCLC‑Zelllinien stellten sie fest, dass die eIF6‑Spiegel konsequent anstiegen, wenn Zellen in den medikamentenresistenten, nicht‑neuroendokrinen Zustand wechselten. Überraschenderweise ging dieser Anstieg mit einem allgemeinen Rückgang der Gesamtproteinproduktion einher, was darauf hindeutet, dass eIF6 mehr tut als seine Lehrbuchfunktion. Detaillierte Analysen, wie mRNAs an Ribosomen gebunden werden, zeigten, dass sich die grundlegenden Ribosomenbestandteile kaum änderten. Stattdessen wurde die Auswahl und Verarbeitung der Botschaften für die Translation umgestaltet, als die Zellen ihre Identität wechselten.
Abkapseln, um sich in Überlebenssignale einzuklinken
Bei näherer Untersuchung entdeckte das Team, dass sich eIF6 in resistenten Zellen teilweise von Ribosomen löst und sich mit einem an der Zelloberfläche aufgebauten Signalzentrum verbindet, das um Integrine und ein Protein namens focal adhesion kinase (FAK) organisiert ist. Integrine helfen Zellen, ihre Umgebung zu erkennen und sich daran zu verankern; FAK leitet diese Signale nach innen weiter und aktiviert häufig Wege, die Bewegung, Überleben und Medikamententoleranz fördern. Biochemische Pull‑downs und In‑Zell‑Proximity‑Assays zeigten, dass eIF6 physisch mit dem Integrin‑Partner CD104 und mit FAK interagiert und dass diese Komplexe in nicht‑neuroendokrinen Zellen häufiger vorkommen. Diese eIF6–Integrin–FAK‑Assemblierung steigert wiederum die Aktivität des MAPK‑Signalwegs, eines bekannten Treibers von Wachstum und Stressresistenz.
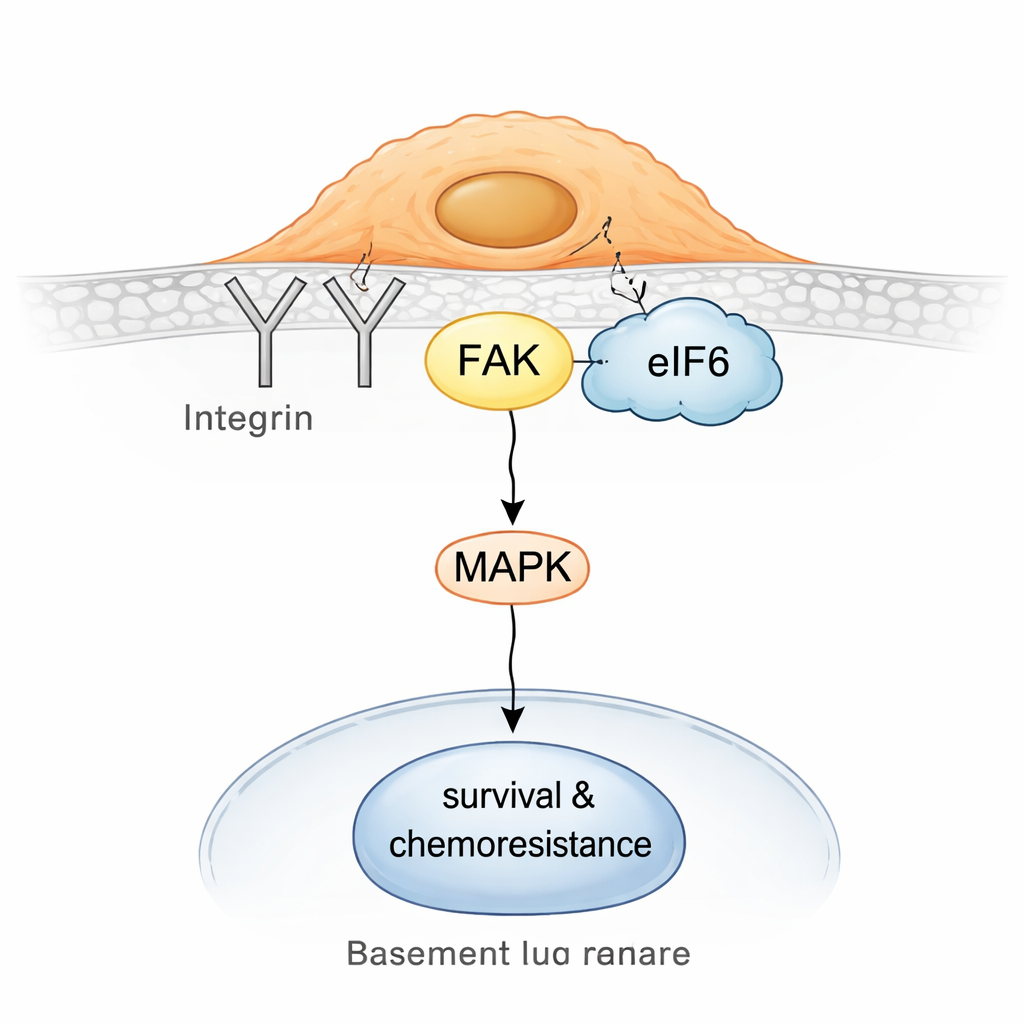
Resistente Tumoren wieder verwundbar machen
Die Forschenden fragten anschließend, ob sich das Verhalten von SCLC durch Eingriffe in eIF6 verändern lässt. Reduzierten sie eIF6 in resistenten Zellen, wurden Gene, die mit einem mobilen, narbenbildenden (epithelial–mesenchymalen) Programm assoziiert sind, herunterreguliert, während klassische neuroendokrine Gene teilweise wiederhergestellt wurden. Diese Veränderungen kehrten den Zustand nicht vollständig um, verlangsamten aber den Übergang in den resistenten Zustand. Wichtig: Zellen mit weniger eIF6 wurden in Kultur und in Maus‑Tumoren empfindlicher gegenüber der Standardchemotherapie Carboplatin–Etoposid, es überlebten weniger Kolonien und die Tumoren schrumpften nachhaltiger. Da für eIF6 bisher keine spezifischen Medikamente existieren, testete das Team FAK‑Inhibitoren, die sich bereits in klinischer Entwicklung befinden. Die Blockade von FAK‑Signalen machte resistente Zellen wieder empfindlich gegenüber Chemotherapie und die Kombinationstherapie erzielte in Mäusen die stärkste Tumorkontrolle.
Vom Laborbefund zu künftigen Patiententools
Schließlich untersuchten die Autoren Tumorproben von Patientinnen und Patienten mit lokal begrenztem SCLC, die operativ behandelt worden waren. Mit einer empfindlichen Färbemethode, die Proteine nur dann sichtbar macht, wenn sie nahe beieinanderliegen, bestimmten sie, wie oft eIF6 in Komplex mit CD104 oder FAK in Tumorzellen vorkommt. Hohe Werte dieser Komplexe — stärker noch als eIF6 allein — korrelierten mit früherem Rückfall und kürzerem Überleben und sind damit vielversprechende prognostische Marker. Insgesamt zeigt diese Arbeit, dass eIF6 abseits der Ribosomen „nebenbei“ tätig werden kann, um Krebszellen in leistungsfähige Überlebensschaltkreise einzubinden. Die Kartierung der eIF6–Integrin–FAK‑Achse legt Ansätze nahe, Patienten mit höherem Rückfallrisiko zu identifizieren und unterstützt den Einsatz von FAK‑Inhibitoren in Kombination mit Chemotherapie, um der gefährlichen Plastizität von SCLC entgegenzuwirken.
Zitation: Peng, H., Wang, Z., Wang, M. et al. Eukaryote initiation factor 6 modulates small-cell lung carcinoma plasticity via the integrin-FAK signaling axis. Nat Commun 17, 2048 (2026). https://doi.org/10.1038/s41467-026-69899-8
Schlüsselwörter: kleinzelliges Lungenkarzinom, Medikamentenresistenz, Zellplastizität, eIF6, Integrin‑FAK‑Signalgebung