Clear Sky Science · de
Kontextabhängige Hemmung der Translation als therapeutisches Konzept gegen Krebs
Die Proteinfabriken gegen Krebs wenden
Krebszellen überleben, indem sie ständig große Mengen kurzlebiger „Treiber“‑Proteine herstellen, die ihr Wachstum und ihre Teilung antreiben. Diese Studie untersucht einen neuen Weg, Krebs zu bekämpfen, indem man die Proteinproduktions‑Maschinen der Zelle — die Ribosomen — fein dosiert blockiert, und zwar nur dann, wenn sie versuchen, ganz bestimmte Proteinsequenzen zu bauen, insbesondere solche, wie sie in schwer angreifbaren Onkogenen wie MYC vorkommen. Diese selektive Störung könnte Tumorzellen abtöten, während ein Großteil der normalen Proteinsynthese verschont bleibt.
Wie Zellen Proteine herstellen — und wo etwas schiefgehen kann
Jede Zelle ist auf Ribosomen angewiesen, winzige molekulare Fabriken, die genetische Botschaften (mRNAs) lesen und Aminosäuren zu Proteinen aneinandersetzen. Die meisten vorhandenen Medikamente, die Ribosomen angreifen — etwa Antibiotika oder ältere Krebsmedikamente — wirken wie grobe Werkzeuge: sie schalten die Proteinsynthese breit herunter, was gesunde Zellen schädigen und schwere Nebenwirkungen verursachen kann. Die Autor:innen überlegten, dass jede entstehende Proteinkette eine eigene Sequenz und chemische Eigenart hat, sodass es möglich sein könnte, kleine Moleküle zu entwickeln, die das Ribosom nur dann blockieren, wenn eine bestimmte Sequenz in der Maschine liegt, und die übrige Proteinsynthese größtenteils unberührt lassen.
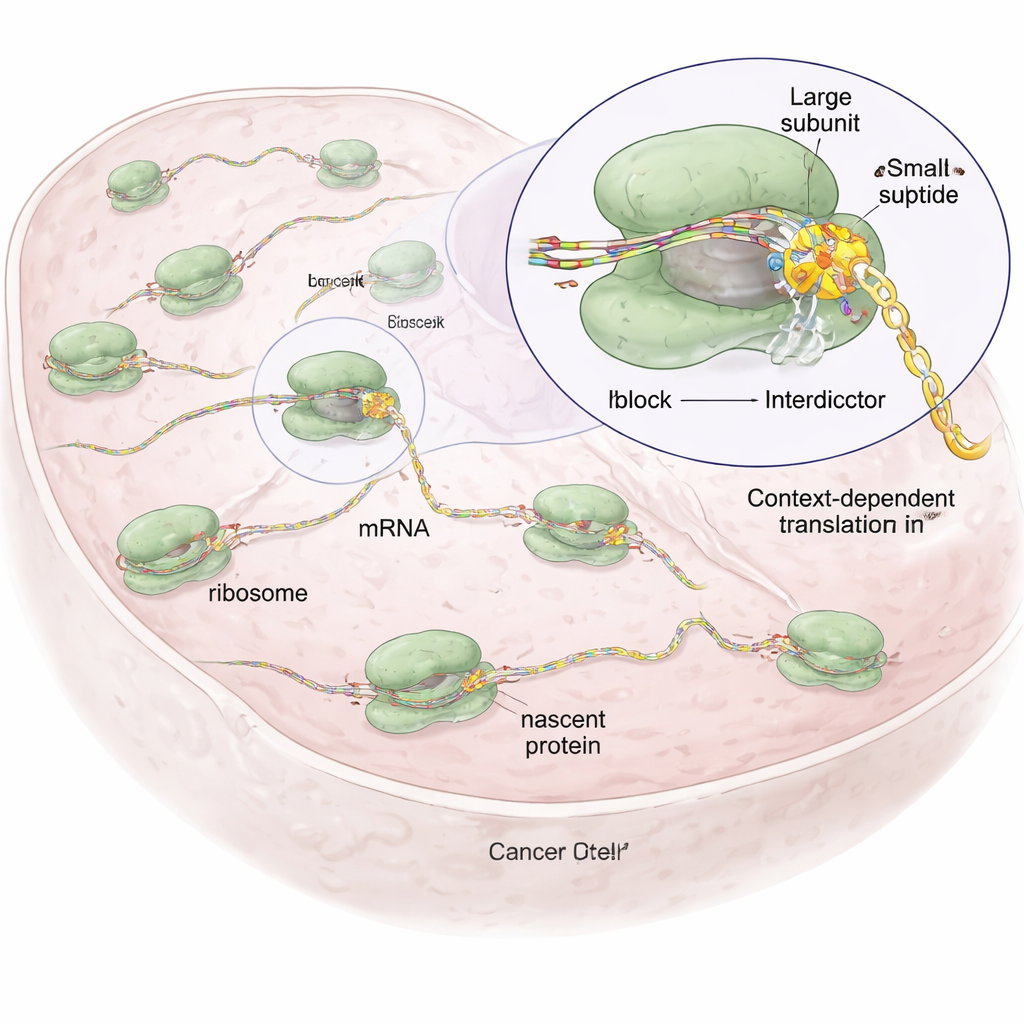
Entwickler‑Moleküle, die nur bestimmte Proteinsequenzen ins Stocken bringen
Aufbauend auf einer natürlichen Verbindung namens Anisomycin, die an das katalytische Zentrum des Ribosoms bindet, wo Peptidbindungen entstehen, erzeugten die Forschenden eine Familie synthetischer Moleküle, die sie „Interdictors“ nennen. Alle teilen ein zentrales Gerüst, das sie im Ribosom verankert, unterscheiden sich jedoch in Seitenketten, die in Richtung der wachsenden Proteinkette zeigen. Diese Seitenketten sind so abgestimmt, dass sie bestimmte Aminosäuretypen bevorzugen — etwa zieht ein Interdictor (IDB‑001) negativ geladene Reste an, während ein anderer (IDB‑002) kleine, fettliebende (hydrophobe) Reste bevorzugt. Mithilfe von Ribosomen‑Profiling, einer Technik, die global abbildet, wo Ribosomen auf mRNAs in Zellen pausieren, zeigte das Team, dass jede Verbindung Stillstände an charakteristischen kurzen Motiven in der entstehenden Kette verursacht, oft an der vorletzten (−1) Aminosäure, was eine sequenzabhängige Wirkung statt einer indiscriminaten Abschaltung belegt.
Das Treffen von Wirkstoff und Ribosom atomgenau beobachten
Um zu verstehen, wie diese Selektivität physikalisch entsteht, frierten die Autor:innen menschliche Ribosomen beim Übersetzen entworfener Peptidsequenzen ein und bildeten sie mittels kryogener Elektronenmikroskopie in nahezu atomarer Auflösung ab. Sie beobachteten den Interdictor im aktiven Zentrum des Ribosoms, wo er präzise Kontakte zu den letzten Aminosäuren der entstehenden Kette knüpft. In einer Struktur liegt eine hydrophobe Seitenkette von IDB‑002 eingebettet zwischen kleinen, nicht sperrigen Resten im Peptid, was erklärt, warum größere Seitenketten dort ungünstig sind. In einer anderen Struktur bildet eine saure Seitenkette eines MYC‑abgeleiteten Restes eine Salzbrücke mit einer positiv geladenen Gruppe von IDB‑001. Die Anwesenheit des Wirkstoffs veranlasst außerdem benachbarte Basen der ribosomalen RNA, neue Positionen einzunehmen, die das aktive Zentrum verengen und den Eintritt der nächsten tRNA teilweise blockieren, wodurch die Elongation an diesen bevorzugten Sequenzen eingefroren wird.
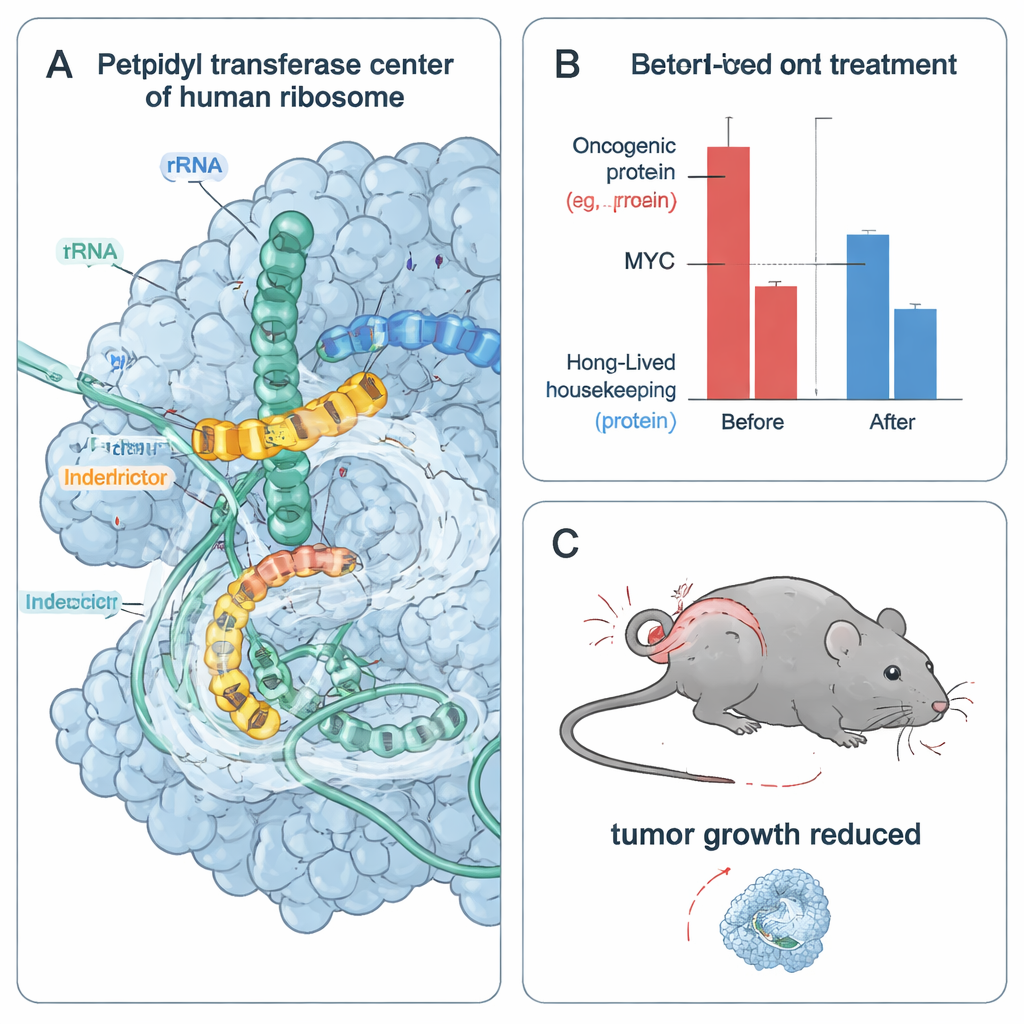
Von gestoppten Ribosomen zu gestressten und sterbenden Tumorzellen
Da sich schnell teilende Krebszellen stark auf kurzlebige onkogene Proteine wie MYC und CCND1 stützen, prüfte das Team, wie sich Interdictors auf das Überleben von Tumorzellen auswirken. In mehreren MYC‑abhängigen Krebszelllinien reduzierten IDB‑001 und IDB‑002 die Zellviabilität in nanomolaren bis niedrigen Mikromolar‑Bereichen. Ein weiter optimiertes Analogon, IDB‑003, war noch wirksamer und für die orale Gabe geeignet. In Zellen entleerten diese Verbindungen rasch MYC und andere schnell turnovernde Onkoproteine, während länger lebende Haushaltsproteine im gleichen Zeitfenster relativ stabil blieben. Die Wirkstoffe lösten zudem zelluläre Stressreaktionen aus, die mit kollidierenden Ribosomen in Verbindung stehen; das Blockieren dieser Stresssignalwege beseitigte jedoch nicht den Verlust der Lebensfähigkeit, was darauf hindeutet, dass die direkte Entziehung essentieller onkogener Proteine ein Haupttreiber des Tumorzelltods ist.
Proof of Concept in einem schwierigen Brustkrebsmodell
Um zu testen, ob dieser Ansatz auch in Tieren funktioniert, behandelten die Autor:innen Mäuse mit humanen triple‑negativen Brustkrebstumoren oral mit IDB‑003. Über 28 Tage wuchsen die behandelten Tumoren deutlich langsamer als die der Kontrolltiere, mit bis zu 80 % Tumorwachstumshemmung bei höheren Dosen und ohne in dieser Studie berichtete schwere Toxizität. Die Genexpressionsanalyse der Tumoren zeigte eine starke Herunterregulierung von MYC‑Zielgenen, was mit verminderter MYC‑Aktivität in vivo übereinstimmt. Zusammengenommen deuten diese Ergebnisse darauf hin, dass das selektive Stillsetzen von Ribosomen an bestimmten Proteinsequenzen Tumoren schwächen kann, die von instabilen onkogenen Treibern abhängig sind, und zugleich die breite Toxizität klassischer Translationshemmer möglicherweise vermeidet.
Warum das für zukünftige Krebstherapien wichtig ist
Diese Arbeit stellt eine neue Art kleiner Moleküle vor: solche, die nicht durch Bindung an ein fertiges Protein wirken, sondern es abfangen, während es entsteht — und nur, wenn eine kurze „Adress‑Tag“‑Sequenz vorhanden ist. Weil viele krebsfördernde Proteine flexibel, kurzlebig oder ohne offensichtliche Taschen für konventionelle Medikamente sind, könnte das direkte Anvisieren ihrer Synthese am Ribosom einen Weg öffnen, Tumoren zu behandeln, die von derzeit „nicht ansprechbaren“ Genen wie MYC getrieben werden. Die Studie legt außerdem nahe, dass sich durch Feinabstimmung der Chemie von Interdictors künftige Medikamente so designen lassen könnten, dass sie auf verschiedene Sequenzmotive und Krankheitssignale abziel en — und diese Strategie über die Onkologie hinaus auf andere Erkrankungen ausweiten, bei denen das Herunterregeln bestimmter Proteine die Gesundheit wiederherstellen könnte.
Zitation: Diamond, P.D., Sauer, P.V., Holm, M. et al. Context-dependent translation inhibition as a cancer therapeutic modality. Nat Commun 17, 1963 (2026). https://doi.org/10.1038/s41467-026-69891-2
Schlüsselwörter: Ribosom‑gerichtete Krebstherapie, Hemmung der Translation, MYC‑getriebene Tumoren, kontextabhängige kleine Moleküle, triple-negativer Brustkrebs