Clear Sky Science · de
Identifizierung von ephrin-A1–EphA2-Signalgebung als potenzielles Ziel zur Frakturprävention
Warum der Schutz brüchiger Knochen wichtig ist
Mit zunehmendem Alter können Knochen dünn und brüchig werden, sodass bereits alltägliche Missgeschicke wie das Stolpern über einen Teppich zu schweren Brüchen führen. Diese osteoporotischen Frakturen sind nicht nur schmerzhaft, sondern auch teuer für Gesundheitssysteme und rauben Jahre gesunder Lebenszeit. Bestehende Medikamente helfen zwar, werden aber meist erst bei manifester Osteoporose eingesetzt und können seltene, aber ernste Nebenwirkungen haben. Diese Studie stellt eine vorausschauende Frage: Können wir mithilfe von Genetik und Proteinmessungen in großen Bevölkerungsgruppen völlig neue Wege finden, Knochen zu stärken und Frakturen zu verhindern, bevor sie auftreten?
Auf der Suche nach Frakturhinweisen im Blut
Die Forschenden starteten, indem sie die zirkulierenden Proteine des Körpers als großes Hinweisbuch betrachteten. Viele Medikamente wirken bereits, indem sie Blutproteine ansteuern; Proteine zu finden, die wirklich das Frakturrisiko beeinflussen, könnte direkt auf neue Therapien hinweisen. Anhand von Proben aus der UK Biobank untersuchten sie genetische Varianten, die die Konzentration von 1.615 verschiedenen Blutproteinen erhöhen oder senken. Diese genetischen „Protein-Fingerabdrücke“ verknüpften sie dann mit Daten aus einer großen genetischen Studie zu über 50.000 Unterarmfrakturen. Eine statistische Methode namens Mendelianische Randomisierung half ihnen zu klären: Wenn Menschen von Geburt an Gene haben, die den Spiegel eines Proteins nach oben oder unten treiben, verändert sich ihr lebenslanges Frakturrisiko in einer konsistenten Weise?
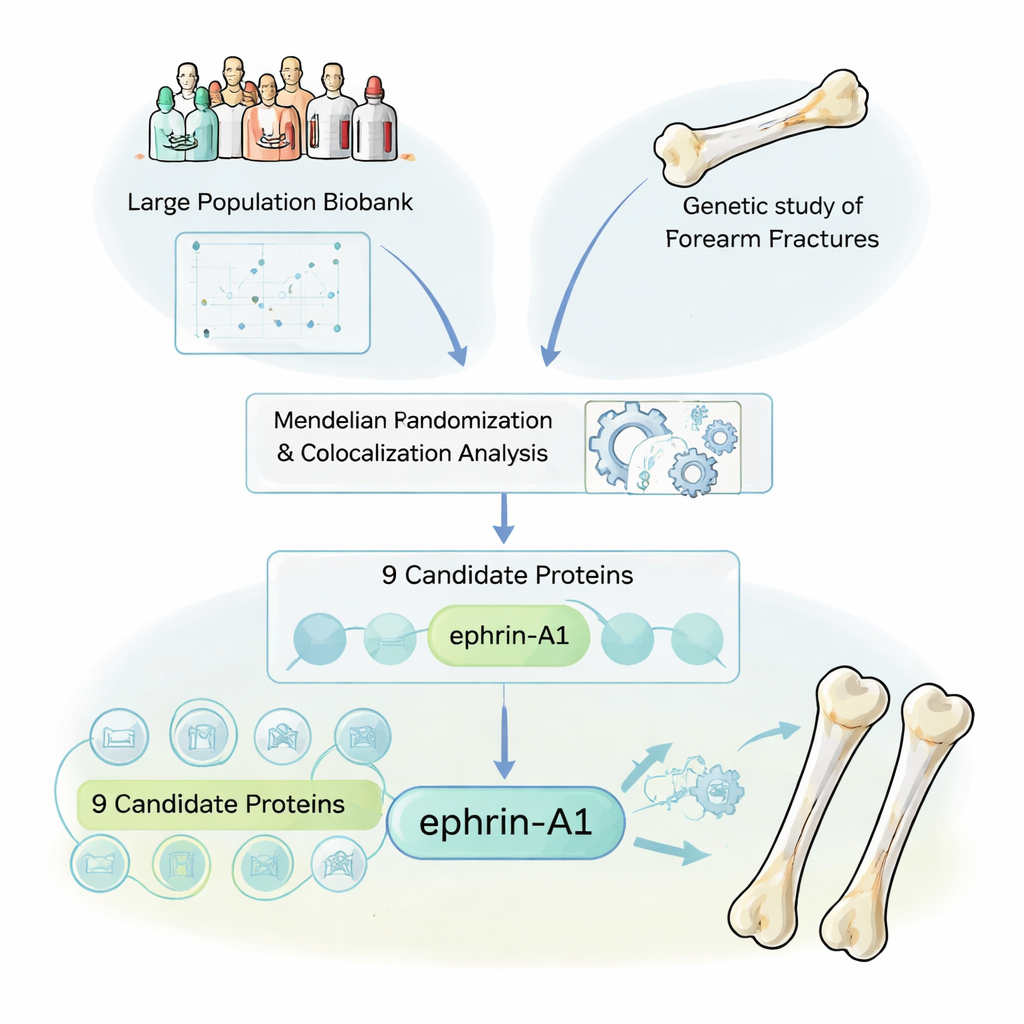
Reale Signale von genetischem Rauschen trennen
Weil benachbarte Gene oft gemeinsam weitergegeben werden, nutzte das Team eine zweite Analyseebene, die Kolokalisierung genannt wird, um sicherzustellen, dass sie kausale Zusammenhänge und nicht irreführende genetische Nachbarn beobachteten. Von den 1.615 Proteinen stachen neun hervor, die kausal mit Unterarmfrakturen verbunden waren. Wichtig ist, dass mehrere davon bereits bekannte Knochenakteure waren: Sclerostin und Osteoprotegerin, die von bestehenden Osteoporosemitteln ins Visier genommen werden, sowie andere Proteine, die lange mit der Knochenmineraldichte verknüpft sind. Ihre Wiederentdeckung lieferte eine entscheidende Qualitätskontrolle und zeigte, dass die Pipeline bewährte Arzneimittelziele zuverlässig wiederfinden kann, während sie zugleich neue Kandidaten ins Blickfeld rückt.
Ein überraschender neuer Schutzfaktor: ephrin-A1
Unter den neu hervorgehobenen Proteinen zog eines besonders die Aufmerksamkeit auf sich: ephrin-A1. Menschen, die genetisch zu höheren Blutspiegeln von ephrin-A1 veranlagt waren, hatten dichtere Knochen und weniger Unterarmfrakturen. Ephrin-A1 ist normalerweise an Zelloberflächen gebunden und kann ins Blut abgeschert werden. Es bindet an einen Rezeptor namens EphA2, der nach Ansicht des Teams stark auf knochenbildenden Zellen, den Osteoblasten, exprimiert wird. Durch die Untersuchung menschlicher und muriner Gewebe mit Einzelzellsequenzierung, in situ-RNA-Bildgebung und einer fortschrittlichen 3D-„DeepBone“-Clearing-Technik beobachteten sie ein konsistentes Muster: ephrin-A1 sitzt auf den Auskleidezellen von Blutgefäßen im Inneren des Knochens, während EphA2 auf Osteoblasten an der Knochenoberfläche lokalisiert ist, oft nur wenige Zell-Durchmesser entfernt. Diese Anordnung macht direkte Zell‑zu‑Zell-Kommunikation zwischen Gefäßzellen und knochenbildenden Zellen nicht nur möglich, sondern wahrscheinlich.
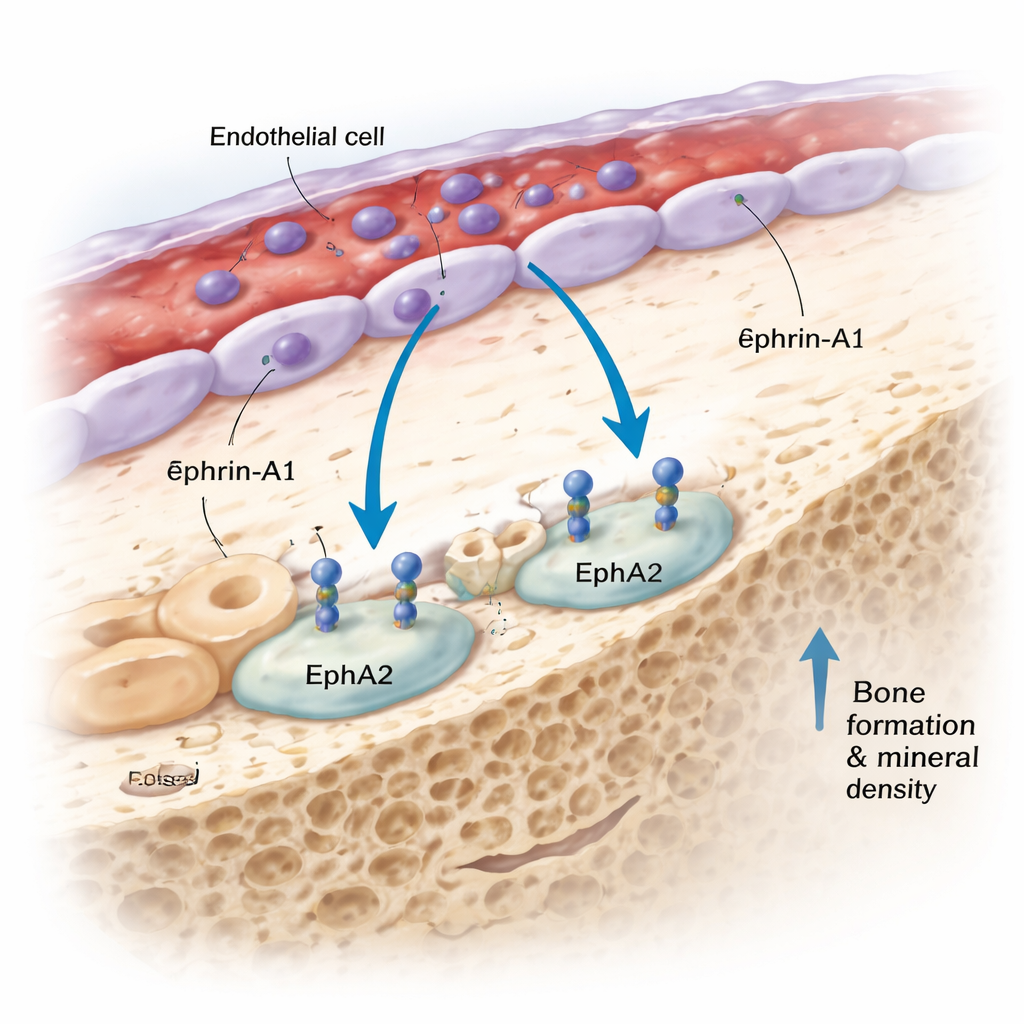
Das Signal in lebenden Knochen testen
Um herauszufinden, ob dieses ephrin-A1–EphA2-Gespräch tatsächlich für die Knochengesundheit relevant ist, wandten sich die Forschenden der Mausgenetik zu. Mäuse, denen entweder ephrin-A1 oder sein Rezeptor EphA2 fehlten, hatten eine deutlich geringere gesamte Körper-Knochenmineraldichte als ihre normalen Wurfgeschwister, in beiden Geschlechtern. Das Team untersuchte dann, wie sich dieses Signalkpaar in verschiedenen Mausmodellen verhält, die menschlichen Knochenverlust bzw. -zuwachs nachahmen. Entzündungen, Alterung und hohe Dosen von Vitamin A — jeweils bekannt dafür, Knochen zu schwächen — waren alle mit einer verringerten Expression von ephrin-A1 und/oder EphA2 im Knochengewebe verbunden. Im Gegensatz dazu steigerte mechanische Belastung, die den günstigen Effekt von belastungsorientierter Bewegung nachahmt, die ephrin-A1-Expression. Bemerkenswerterweise spiegelten sich diese Veränderungen nicht in den Mustern wider, die bei aktuellen Osteoporosemedikamenten beobachtet werden, was darauf hindeutet, dass ephrin-A1–EphA2 über einen eigenen Weg wirkt, der bestehende Therapien ergänzen könnte.
Was das für die zukünftige Frakturprävention bedeutet
Insgesamt zeigt die Studie, dass ein ausgefeilter Genetik-plus-Protein-Ansatz bekannte Wirkziele für Knochentherapien wiederfinden und neue aufdecken kann. Sie weist darauf hin, dass die Interaktion von ephrin-A1 mit EphA2 auf Osteoblasten ein wichtiges Signal ist, das hilft, Knochen dicht und belastbar zu halten. Für eine allgemeine Leserschaft lautet die Kernbotschaft: Unser Blut und unsere Gene enthalten detaillierte Blaupausen dafür, wie Knochen stark bleiben — und ephrin-A1 ist jetzt ein vielversprechender neuer Schalter in dieser Blaupause. Wenn künftige Arbeiten diesen Schalter sicher hochsetzen können, etwa mit Medikamenten, die ephrin-A1–EphA2-Signalgebung verstärken, könnte das einen neuen, potenziell sichereren Weg zur Frakturprävention eröffnen, besonders für die vielen Menschen, die derzeit unbehandelt bleiben.
Zitation: Movérare-Skrtic, S., Nethander, M., Li, L. et al. Identification of ephrin-A1–EphA2 signalling as a potential target for fracture prevention. Nat Commun 17, 1988 (2026). https://doi.org/10.1038/s41467-026-69863-6
Schlüsselwörter: Osteoporose, Knochenmineraldichte, Frakturprävention, ephrin-A1 EphA2, Mendelianische Randomisierung