Clear Sky Science · de
TRIM13 In-situ-Engineering erhöht die entzündungsdämpfende Kapazität von CAR-Ms für die Therapie von Leberfibrose
Umprogrammierung der Aufräumtruppe der Leber
Leberfibrose, ein Vernarbungsprozess, der zu Zirrhose und Leberversagen führen kann, betrifft Millionen Menschen und hat derzeit nur wenige wirksame Behandlungen. Diese Studie untersucht einen Ansatz, die körpereigenen Immunzellen der Leber so zu nutzen und umzuprogrammieren, dass sie nicht nur narbenbildende Zellen entfernen, sondern auch schädliche Entzündungen dämpfen — was möglicherweise eine sicherere und stärkere Therapie für chronische Lebererkrankungen bieten könnte.
Warum Lebernarbe so schwer zu stoppen ist
Wird die Leber wiederholt verletzt — durch Viren, Alkohol oder Stoffwechselerkrankungen — versucht sie zu heilen, indem sie Narbengewebe bildet. Spezialisierte Zellen, die hepatischen Sternzellen, schalten in einen „aktivierten“ Zustand und produzieren zähe Fasern, ähnlich wie Bauarbeiter, die Beton gießen. Mit der Zeit verformt diese Vernarbung, die als Fibrose bezeichnet wird, das Organ und beeinträchtigt seine Funktion. Immunzellen, die Makrophagen genannt werden, stehen im Zentrum dieses Prozesses. In einer geschädigten Leber können sie wie ein zweischneidiges Schwert wirken: In einem Modus fördern sie Entzündung und aktivieren Sternzellen, in einem anderen, heilungsfördernden Modus helfen sie, Narben abzubauen und das Gleichgewicht wiederherzustellen.
Schädliche Signale in nützliche verwandeln
Die Forscher konzentrierten sich auf ein wichtiges Gefahrensignal in geschädigten Lebern: mitochondriale DNA, die aus verletzten Zellen entweicht. Makrophagen erkennen diese DNA über einen Signalweg, der als cGAS‑STING bekannt ist und sie in einen proinflammatorischen, narbenfördernden Zustand treibt. Ein Protein namens TRIM13 hilft normalerweise, STING zu dämpfen, indem es dessen Abbau markiert. Das Team argumentierte, dass eine Verstärkung von TRIM13 in Lebermakrophagen diese zurück in einen beruhigenden, gewebereparierenden Zustand versetzen könnte. Gleichzeitig sollten diese Zellen gezielt die narbenbildenden Sternzellen aufspüren und entfernen. Dafür nutzten sie das Konzept des chimären Antigenrezeptors (CAR) aus der Krebstherapie: einen synthetischen Rezeptor, der Immunzellen erlaubt, ein gewähltes Ziel zu erkennen — in diesem Fall ein Protein namens FAP, das auf aktivierten Sternzellen reichlich vorhanden ist.
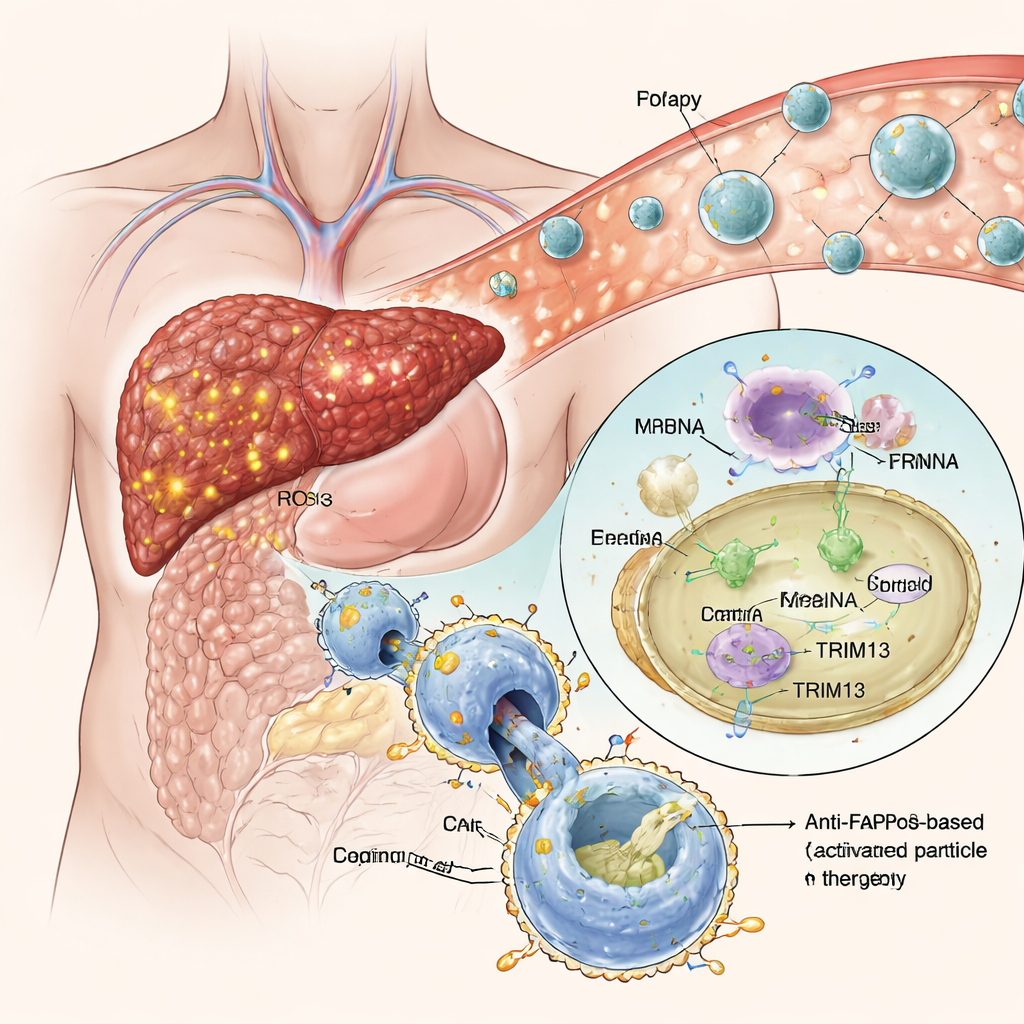
Intelligente Nanopartikel, die erkranktes Gewebe ansteuern
Anstatt Makrophagen außerhalb des Körpers zu verändern, entwickelten die Forscher „efferocytose‑gezündete“ Lipidnanopartikel — winzige, fettbasierte Kugeln, die genetische Anweisungen als Boten‑RNA (mRNA) transportieren. Diese Partikel sind mit einer getarnten Form von Phosphatidylserin beschichtet, einem natürlichen „Iss‑mich“-Signal, das sterbende Zellen zeigen, um Makrophagen anzulocken. In der stark oxidativen Umgebung fibrotischen Lebergewebes wird die Tarnung entfernt und das Signal freigelegt, wodurch nahegelegene Makrophagen die Nanopartikel aufnehmen. Einmal im Inneren wird die mRNA freigesetzt und von der Zelle gelesen, was zur Produktion von sowohl TRIM13 als auch des anti‑FAP‑CAR führt. In Zellkulturen brachte dieser Ansatz Makrophagen erfolgreich in einen entzündungshemmenden Zustand und verlieh ihnen gleichzeitig eine starke, selektive Vorliebe für FAP‑positive narbenbildende Zellen, ohne ihre normale Fähigkeit zur Beseitigung anderer Trümmer zu stören.
Von kranken zu regenerierenden Lebern bei Mäusen
Das Team testete die Strategie anschließend in Mausmodellen der Leberfibrose, die entweder durch ein toxisches Chemikalium oder durch eine fettreiche, nährstoffarme Diät verursacht wurde. Systemisch injizierte Nanopartikel erreichten effizient die Leber und wurden besonders in fibrotischen Tieren überwiegend von Makrophagen aufgenommen. Dort zeigten die veränderten Zellen eine reduzierte Aktivität des STING‑Signalwegs und eine geringere Produktion entzündlicher Moleküle sowie eine verstärkte Abtötung aktivierter Sternzellen. Gewebeanalysen offenbarten markante Rückgänge von Kollagen und anderen Narbenmarkern, eine feingliedrigere und normalere Struktur der extrazellulären Matrix sowie verbesserte Blutwerte der Leberfunktion. Die Lebern behandelter Mäuse wiesen mehr proliferierende Zellen und eine wiedergewonnene gesündere Architektur auf, was auf echte Organreparatur und nicht nur auf eine vorübergehende Dämpfung der Entzündung hindeutet.
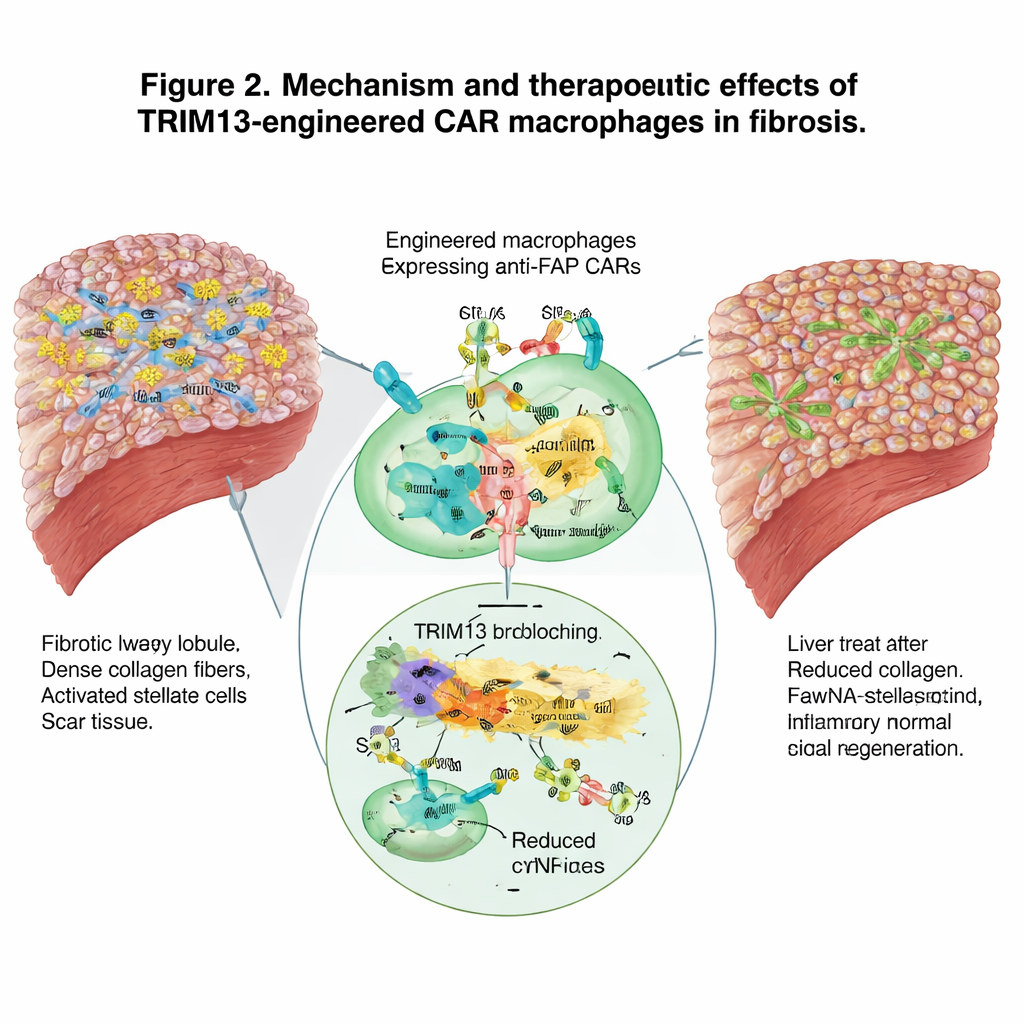
Das breitere Immunsystem einbinden
Über die direkte Narbenentfernung hinaus veränderten die programmierten Makrophagen die weitere Immunlandschaft. Sie gingen von einem aggressiven, schädigungsfördernden Profil zu einem eher auflösenden, heilenden Profil über und reduzierten entzündliche Signale im Blut. Gleichzeitig schienen sie durch das Verschlingen narbenbildender Zellen als Lehrmeister für das adaptive Immunsystem zu fungieren, indem sie Neutrophile, dendritische Zellen und T‑Zellen anlockten und eine koordinierte Reaktion gegen das fibröse Gewebe förderten. Einzelzell‑RNA‑Sequenzierungen von Leber‑Immunzellen bestätigten die Verschiebung weg von proinflammatorischen Genprogrammen hin zu einer erhöhten Fähigkeit, schädliche Zellen und Trümmer zu umschließen und zu entfernen.
Was das für Patientinnen und Patienten bedeuten könnte
Für nichtfachliche Leser lässt sich festhalten: Die Arbeit weist auf eine Möglichkeit hin, die eigenenen Müllentsorger der Leber so „umzuschulen“, dass sie sowohl Narbengewebe abbauen als auch die chronischen Alarmzeichen ausschalten, die die Schädigung am Laufen halten. Durch die Verwendung kurzlebiger mRNA‑Anweisungen in intelligenten Nanopartikeln vermeidet die Therapie dauerhafte Veränderungen der Zellen und begrenzt die Aktivität auf erkrankte Regionen, was Nebenwirkungen verringern könnte. Obwohl vor einer Anwendung am Menschen noch deutlich mehr Tests nötig sind, skizziert diese Strategie ein vielversprechendes Konzept zur Behandlung von Leberfibrose — und möglicherweise auch anderer fibrotischer Erkrankungen — indem das Immunsystem des Körpers vom Treiber der Vernarbung zu einem aktiven Partner der Heilung gemacht wird.
Zitation: Gao, J., Yang, Z., Song, Y. et al. TRIM13 in situ engineering boosts anti-inflammatory capacity of CAR-Ms for liver fibrosis therapy. Nat Commun 17, 2077 (2026). https://doi.org/10.1038/s41467-026-69858-3
Schlüsselwörter: Leberfibrose, Makrophagen-Therapie, Nanopartikel-mRNA-Transfer, chimärer Antigenrezeptor, TRIM13 STING-Signalweg