Clear Sky Science · de
Maximierung der Energienutzung und Effizienz der Lithiumauslaugung durch sequentielle elektrochemische Doppeloxidation und Einweich‑Relaxation
Warum alte Autobatterien immer noch wichtig sind
Lithium‑Ionen‑Batterien treiben unsere Telefone, Laptops und zunehmend auch unsere Autos an. Wenn jedoch Millionen von Traktionsbatterien das Ende ihrer Lebensdauer erreichen, entsteht eine neue Art von Abfall – und eine neue Chance. Das in verbrauchten Batterien enthaltene Lithium und andere Metalle sind wertvoll, ihre Rückgewinnung aber energieintensiv. Diese Studie untersucht einen schlaueren Weg, Lithium mit Hilfe von Strom effizienter zurückzugewinnen, die Kosten und die Umweltbelastung zu senken und gleichzeitig mit der weltweit wachsenden Nachfrage nach Batteriematerialien Schritt zu halten.
Altbatterien in eine Ressource verwandeln
Heute beruht die industrielle Aufarbeitung von Lithium‑Ionen‑Batterien meist auf aggressiven Chemikalien oder Hochtemperaturofen. Diese Methoden können Metalle zurückgewinnen, verschwenden jedoch häufig Energie und erschweren die saubere Trennung von Lithium von Nickel, Kobalt und Mangan in den sogenannten NCM‑Batterien. Die Forschenden konzentrierten sich auf einen neueren, saubereren Ansatz: den Einsatz eines elektrischen Stroms in salzhaltigem Wasser, um Lithium aus dem verbrauchten Kathodenmaterial zu lösen. Sie stellten eine einfache, aber entscheidende Frage: Können wir Zeitpunkt und Art der Stromnutzung so umstrukturieren, dass fast jedes Watt zur Entfernung von Lithium beiträgt, statt in Nebenreaktionen verloren zu gehen?
Ein zweistufiger Tanz: Kraft, dann Ruhe
Das Team entwickelte einen zweistufigen Prozess, der ein aktives „Schieben“ mit einem ruhigen „Einweichen“ kombiniert. In der ersten Stufe, der elektrochemischen Doppeloxidation, wird über eine Zelle mit einer verbrauchten NCM‑Kathode und einer Natriumchlorid‑Lösung eine konstante Spannung angelegt. Der Strom zieht Lithium‑Ionen aus dem Feststoff in die Flüssigkeit und erzeugt zugleich starke oxidierende Spezies in der Lösung. Die Forschenden stellten fest, dass die meiste nutzbare Arbeit in der ersten Stunde geschieht: Lithium verlässt die Kristallstruktur anfangs schnell, später wird ein Großteil der Energie auf Nebenreaktionen wie Sauerstoffentwicklung verschwendet.
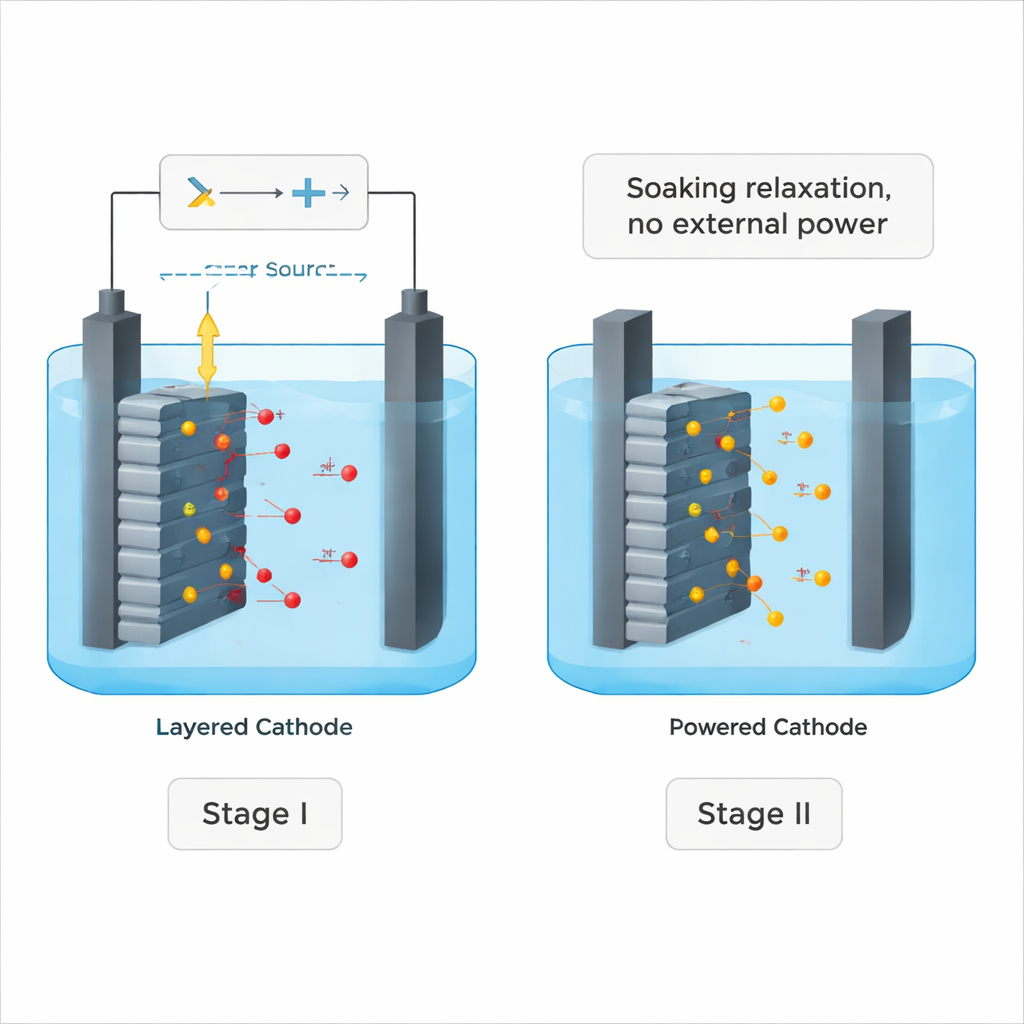
Die Chemie die Arbeit beenden lassen
Anstatt die Stromzufuhr immer länger fortzusetzen, schalteten die Forschenden die Spannung einfach ab und ließen die Elektrode in der nun oxidierenden Salzlösung einweichen. Überraschenderweise setzte die Auslaugung von Lithium fort, bis fast alles entfernt war – etwa 99 % Rückgewinnung bei frischem NCM‑Material und rund 98 % bei realen verbrauchten Kathoden. Detaillierte Messungen zeigten, dass Sauerstoffatome innerhalb des Kristalls, die in der geladenen Phase vorübergehend in einen reaktiveren Zustand versetzt worden waren, in der zweiten, ruhigen Phase zum verborgenen Treiber wurden. Diese „aktivierten“ Sauerstoffspezies förderten einen langsamen Tausch: Lithium‑Ionen diffundierten in die Lösung, während Natrium‑ (oder Kalium‑)Ionen aus der Lösung in die entstehenden Leerstellen einsprangen – ganz ohne weitere elektrische Zufuhr.
Wie sich die Kristallstruktur umordnet
Mithilfe von Elektronenmikroskopen, Röntgenbeugung und Spektroskopie beobachtete das Team, wie die Kathodenpartikel rissen, dünner wurden und ihre interne Stapelung veränderten, während Lithium entwich. Das Material durchlief mehrere bekannte geschichtete Anordnungen, während es von lithiumreich zu lithiumarm wurde und schließlich in einer natriumreichen Form endete, die die Struktur zusammenhielt, aber kaum noch Lithium enthielt. Während dieses Prozesses änderten Nickel‑ und Kobalt‑Atome ihre Ladungszustände, um das elektrische Gleichgewicht des Materials zu wahren, während Mangan weitgehend unverändert blieb und so das Gerüst stabilisierte. Die Forschenden zeigten außerdem, dass Kaliumionen, die ihre Wassermoleküle leichter ablegen als Natrium, den Ionentauschschritt weiter beschleunigen können.
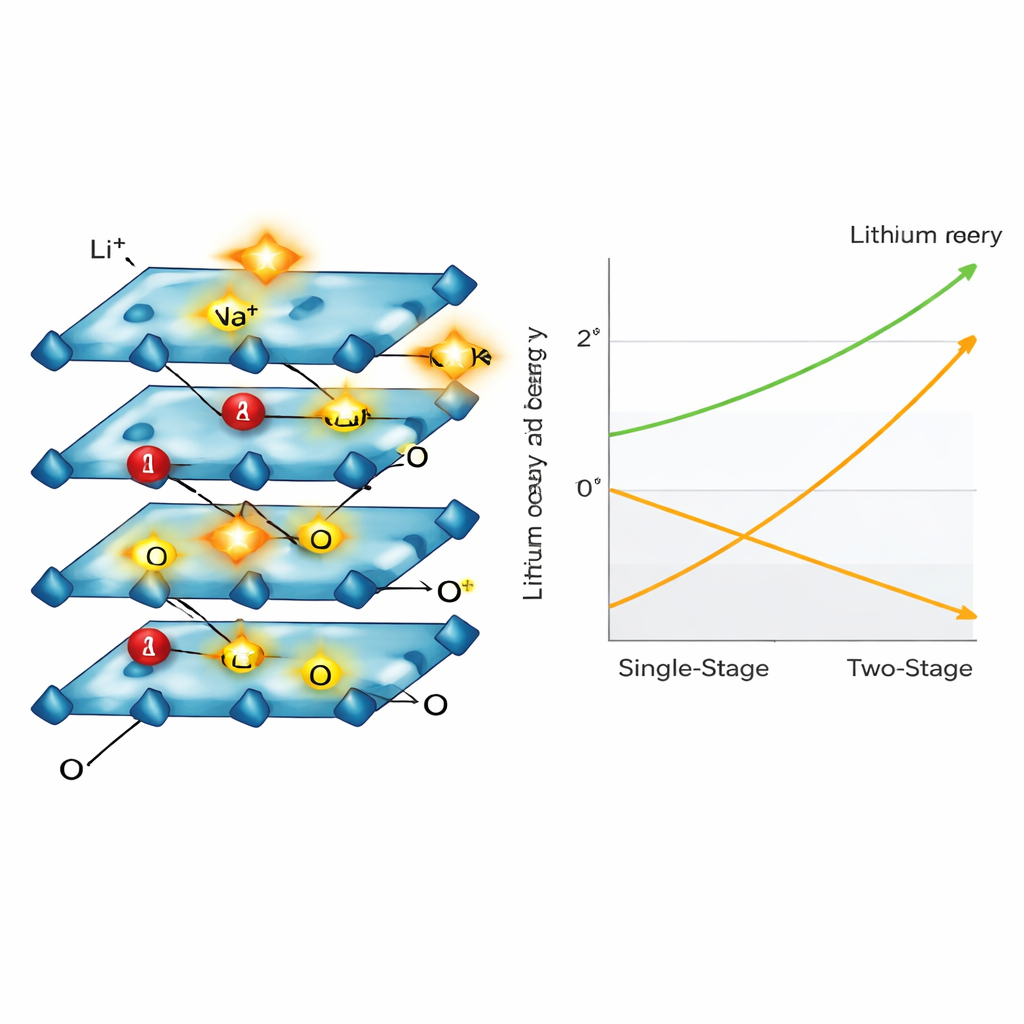
Vom Labor auf die Fabrikhalle
Um zu prüfen, ob die Idee außerhalb des Labors funktionieren kann, bauten die Forschenden ein Pilot‑System, das pro Charge eine halbe Kilogramm echten Batterieabfall behandeln kann. Mit ihrer zweistufigen Methode gewannen sie über 98 % des Lithiums als hochreines Lithiumcarbonat zurück, geeignet für die Herstellung neuer Batterien. Entscheidend war, dass mit dem Ausschalten der Stromzufuhr, sobald die „intelligente Chemie“ in Gang gesetzt war, der Prozess etwa halb so viel elektrische Energie verbrauchte wie ein standardisiertes einstufiges elektrochemisches Verfahren und damit mehr als ein Fünftel des betrieblichen Gewinns pro Tonne recyceltem Kathodenmaterial einspart.
Was das für zukünftige Batterien bedeutet
Einfach ausgedrückt zeigt die Studie, dass es nicht immer nötig ist, kontinuierlich Strom zuzuführen, um wertvolle Materialien aus alten Batterien zurückzugewinnen. Ein gut getimter Energieschub kann Material und Lösung so vorbereiten, dass der Rest der Arbeit von selbst geschieht, angetrieben durch innere chemische Kräfte. Wird dieser zweistufige Ansatz in großem Maßstab übernommen, könnte das Recycling von Lithium aus verbrauchten NCM‑Batterien kostengünstiger, sauberer und für die Industrie attraktiver werden, den Lebenszyklus von Batterien schließen und den Druck auf den Abbau neuen Lithiums verringern.
Zitation: Zhong, W., Gu, X., Feng, X. et al. Maximizing energy utilization and lithium leaching efficiency via sequential electrochemical dual-oxidation and soaking-relaxation. Nat Commun 17, 2050 (2026). https://doi.org/10.1038/s41467-026-69834-x
Schlüsselwörter: Lithiumrecycling, Akkuabfall, energieeffiziente Auslaugung, NCM‑Kathoden, elektrochemische Rückgewinnung