Clear Sky Science · de
Überleben von Cyanobakterien und Abschwächung der toxischen Effekte von Fe(II) in einem silica-reichen archäischen Ozean
Uralte Meere und die Luft, die wir atmen
Milliarden Jahre bevor Tiere oder Pflanzen existierten, begannen winzige photosynthetische Mikroben, so genannte Cyanobakterien, Sauerstoff in die Ozeane der Erde freizusetzen. Dennoch dauerte es hunderte Millionen Jahre, bis sich Sauerstoff schließlich in der Atmosphäre anhäufte. Diese Studie fragt, warum diese Verzögerung so lange dauerte und ob die Chemie der frühen Meere — reich an gelöstem Eisen und Siliziumdioxid — den Mikroben, die unsere Atmosphäre letztlich atembar machten, geholfen oder geschadet hat.

Eisenreiche Ozeane und eine toxische Nebenwirkung
Die frühen Ozeane enthielten große Mengen gelösten Eisens, besonders in Küstenregionen, in denen tiefes Wasser an die Oberfläche aufstieg. Wenn dieses Eisen auf den von Cyanobakterien abgegebenen Sauerstoff traf, oxidierte es und bildete Eisenminerale, die später zu den banded iron formations (geschichteten Eisenerzen) wurden — gestreifte Gesteine, die zu den ältesten geologischen Archiven gehören. Die gleichen Reaktionen können jedoch auch „reaktive Sauerstoffspezies“ erzeugen, hochreaktive Formen von Sauerstoff, die DNA, Proteine und Zellmembranen schädigen können. Frühere Arbeiten legten nahe, dass diese eisengetriebene chemische Gegenreaktion Cyanobakterien vergiftet und so ihre Ausbreitung verlangsamt und den Anstieg von Sauerstoff in der Luft verzögert haben könnte.
Siliziumdioxid als unerwarteter Beschützer
Die Autoren konzentrierten sich auf eine weitere häufige Komponente des urzeitlichen Meerwassers: gelöstes Siliziumdioxid, das gleiche Grundmaterial wie Glas. Geologische Befunde deuten darauf hin, dass die frühen Ozeane deutlich höhere Silicakonzentrationen als heute aufwiesen. In Laborversuchen kultivierten sie ein marines Cyanobakterium (Synechococcus sp. PCC 7002) unter kontrollierten Bedingungen mit unterschiedlichen Mengen an gelöstem Eisen und Siliciumdioxid. Sie verfolgten, wie schnell die Zellen wuchsen, wie viel Sauerstoff sie produzierten, wie schnell Eisen oxidierte und wie viele reaktive Sauerstoffspezies sich bildeten. Bei niedrigen Eisengehalten gediehen die Zellen unabhängig von Silica. Bei sehr hohen Eisengehalten — vergleichbar mit den Bedingungen, die in einigen archäischen Küstengewässern erwartet werden — litten jedoch Kulturen ohne zugesetztes Silica, während solche mit hohem Silicagehalt aktiv blieben, mehr Sauerstoff produzierten und höhere Zellzahlen erreichten.
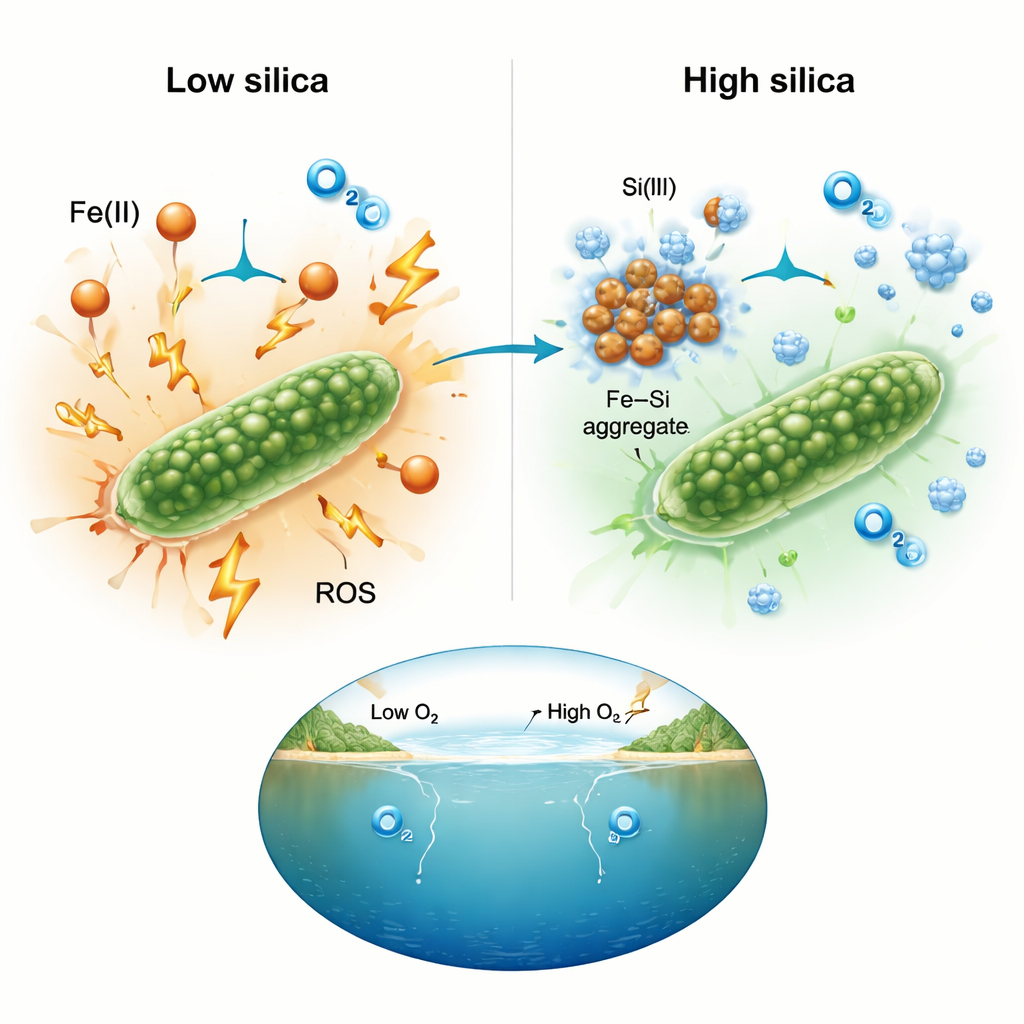
Chemische Zusammenarbeit, die schädliche Reaktionen zügelt
Um zu verstehen, warum Silica einen so großen Unterschied machte, maßen die Forscher reaktive Sauerstoffspezies direkt mit fluoreszierenden Farbstoffen. Bei hohen Eisengehalten zeigten kulturen ohne Silica starke Signale reaktiver Sauerstoffspezies, was mit belastender Chemie rund um die Zellen übereinstimmt. In silica-reichen Versuchsreihen blieben diese Signale nahe dem Hintergrundniveau, selbst bei extremen Eisenkonzentrationen. Die Forscher interpretieren dies so, dass Silica an gelöstes Eisen bindet und Eisen–Silica-Aggregate bildet. Sobald das Eisen in solchen Klumpen gebunden ist, steht es weniger zur Verfügung, um die Kettenreaktionen anzutreiben, die schädliche Oxidantien erzeugen. Die Nettowirkung ist eine Abschwächung der chemischen Umgebung, sodass Cyanobakterien weiter photosynthetisieren können, anstatt durch oxidativen Stress gelähmt zu werden.
Tag–Nacht-Rhythmen und Auswirkungen auf Ozean-Skala
Die Experimente liefen zudem unter realistischen Tag–Nacht-Lichtzyklen statt unter konstanter Beleuchtung. Unter diesen wechselnden Bedingungen oxidierten Cyanobakterien Eisen schneller und tolerierten eisenreiche Gewässer besser, was darauf hindeutet, dass nächtliche „Erholungs“-Phasen den Langzeitstress verringern. Ausgehend von den im Labor gemessenen Sauerstoffproduktionsraten entwickelten die Autoren dann ein einfaches numerisches Modell einer archäischen Wassersäule. Für plausible Cyanobakterienzahlen und realistische Auftriebsraten tieferer Wasserschichten stellten sie fest, dass Oberflächengewässer sauerstoffreich werden konnten, während tiefere Schichten eisenbeladen blieben. In vielen Szenarien erreichten die Sauerstoffkonzentrationen in der belichteten Zone Werte, die mit oder über der Sättigung moderner Meerwasserwerte lagen, was darauf hindeutet, dass lokale Sauerstoff‑„Oasen“ über eisenreichen Tiefen häufig gewesen sein könnten.
Neu denken, warum Sauerstoff so lange brauchte
Insgesamt sprechen die Ergebnisse dafür, dass reaktiver Sauerstoff, der durch Eisen und Sauerstoff entstand, für frühe Cyanobakterien wahrscheinlich kein unüberwindbares Problem war, vorausgesetzt, Silica war reichlich vorhanden und natürliche Tag–Nacht‑Zyklen herrschten vor. Anstatt chronisch vergiftet zu sein, fanden diese Mikroben vermutlich viele Küstenorte, an denen Silica die schädlichen Nebenwirkungen von Eisen abpufferte, was ihnen erlaubte zu wachsen, große Mengen Eisen zu oxidieren und überschüssigen Sauerstoff in die Atmosphäre zu entweichen. Das verbleibende Rätsel, warum die Erdatmosphäre so spät oxygenierte, muss daher eher in großskaligen Faktoren liegen — etwa wie schnell Sauerstoff durch vulkanische Gase und Gesteine verbraucht wurde — als in der lokalen Chemie um einzelne mikrobielle Zellen.
Zitation: Dreher, C.L., Cirpka, O.A., Schad, M. et al. Survival of cyanobacteria and mitigation of Fe(II) toxicity effects in a silica-rich Archean ocean. Nat Commun 17, 1987 (2026). https://doi.org/10.1038/s41467-026-69826-x
Schlüsselwörter: frühes Erdatmosphäre-Sauerstoff, Cyanobakterien, gegliederte Eisenerze, reaktive Sauerstoffspezies, silicareiche Ozeane