Clear Sky Science · de
Cholecystokinin aus Beta-Zellen fördert bei Adipositas die Entwicklung von Pankreasadenokarzinomen
Wenn Übergewicht mit dem Pankreas spricht
Es ist bekannt, dass Adipositas das Risiko für Pankreaskrebs — eine der tödlichsten Krebsarten — erhöht, doch die biologische „Konversation“, die überschüssiges Körperfett mit Tumoren verbindet, war lange unklar. Diese Studie fördert einen unerwarteten Botenstoff zutage: das Verdauungshormon Cholecystokinin (CCK), das innerhalb der insulinproduzierenden Zellen des Pankreas hergestellt wird. Indem die Autorinnen und Autoren verfolgen, wie sich diese Zellen unter metabolischem Stress verändern, zeigen sie, wie ein Hormon, das dem Körper helfen soll, stattdessen Krebs befeuern kann, und sie deuten neue Wege an, die Krankheit abzufangen, bevor sie Fuß fasst.
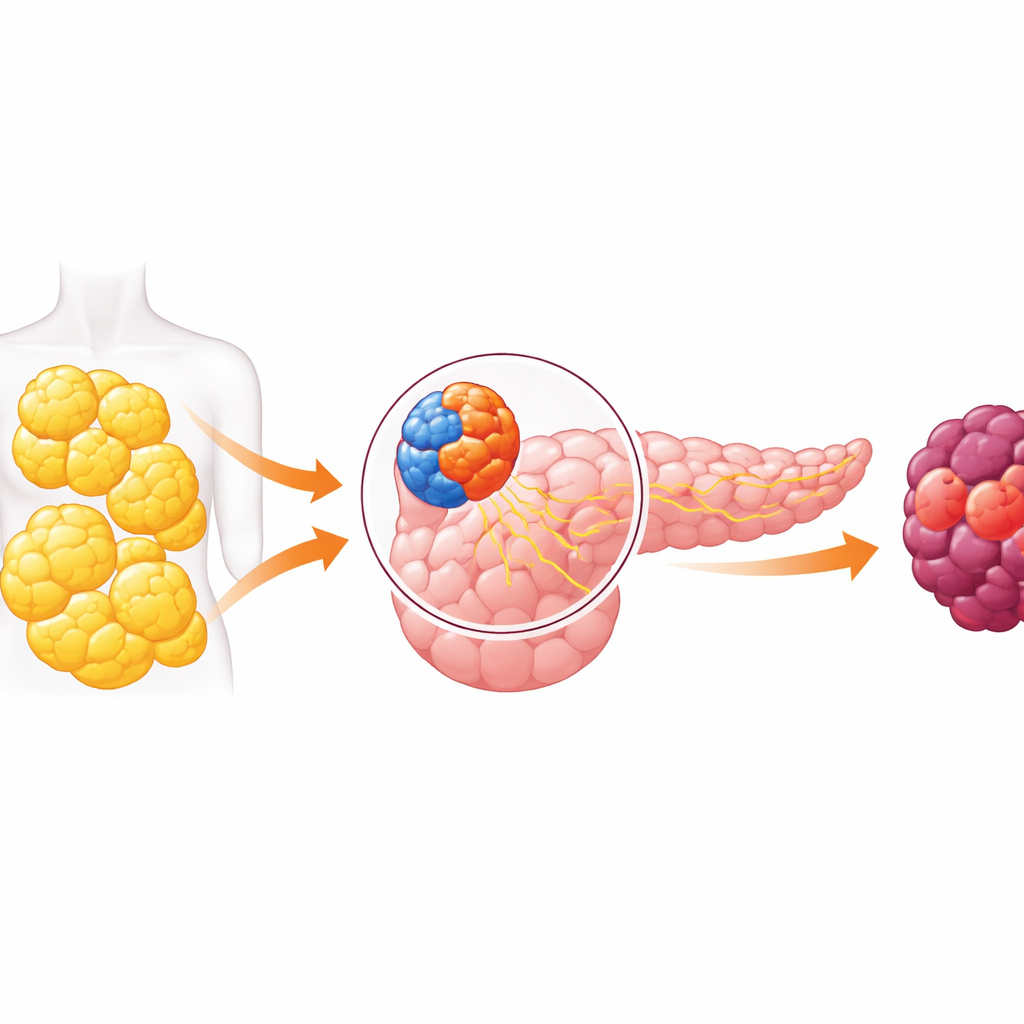
Ein Organ mit zwei Seiten und ein gefährlicher Dialog
Das Pankreas hat zwei Hauptaufgaben. Die eine Seite, der endokrine Teil, enthält winzige Inseln von Zellen, die Hormone wie Insulin zur Kontrolle des Blutzuckers freisetzen. Der andere, der exokrine Teil, produziert Verdauungssäfte und umfasst die Zellen, aus denen am häufigsten Pankreaskrebs entsteht. Jahrelang gingen Forschende davon aus, dass diese Kompartimente weitgehend getrennt arbeiten. Jüngere Arbeiten haben diese Vorstellung widerlegt und gezeigt, dass Signale aus hormonproduzierenden Zellen die benachbarten Verdauungszellen beeinflussen können. Dieses Papier geht auf diesen Austausch ein und zeigt, dass er bei Adipositas die exokrine Seite des Pankreas in Richtung Krebs treiben kann.
Stress in Hormonzellen löst ein neues Signal aus
Bei Adipositas stehen insulinproduzierende Beta-Zellen unter dauerhaftem Druck, dem steigenden Insulinbedarf gerecht zu werden. Mithilfe von Einzelzell-RNA-Sequenzierung und fortgeschrittenen Rechenmethoden verfolgten die Forschenden einzelne Beta-Zellen, während Mäuse von schlank über übergewichtig bis hin zu stark adipös wurden. Sie fanden, dass sich eine Untergruppe unreifer Beta-Zellen vermehrte und nach und nach ihre spezialisierte Insulin-Identität verlor. Während diese Zellen gestresst wurden, stiegen Marker für Protein-Faltungsstress und Zellschädigung an, während die Insulinproduktion zurückging. Gleichzeitig begannen diese Zellen, hohe Mengen an CCK zu produzieren — ein Hormon, das sonst mit dem Darm assoziiert wird und das Wachstum und Veränderungen von Verdauungszellen stimulieren kann.
Vom hilfreichen Hormon zur Krebsantriebskraft
Um zu prüfen, ob das neu produzierte CCK nur ein Stressnebenprodukt oder ein aktiver Krankheitsverursacher war, erzeugte das Team Mäuse, deren Beta-Zellen zusätzliches CCK produzierten, selbst ohne Adipositas. Diese Tiere entwickelten pankreatische Präkanzerosen und invasive Tumore in ähnlichem Ausmaß wie adipöse Mäuse, obwohl sie normales Gewicht und normalen Blutzucker hatten. Im Gegensatz dazu sank bei Entfernen von CCK ausschließlich im Pankreas adipöser Mäuse die Tumorlast stark, obwohl die Tiere weiter schwer und hyperinsulinäm waren. In mehreren Mausmodellen korrelierte die CCK-Menge im Pankreas eng mit dem Tumorumfang, während Insulinwerte tendenziell in die entgegengesetzte Richtung gingen. Das deutet darauf hin, dass in diesen Systemen CCK — nicht Insulin — das vorherrschende Hormon ist, das Adipositas mit Pankreaskrebs verbindet.
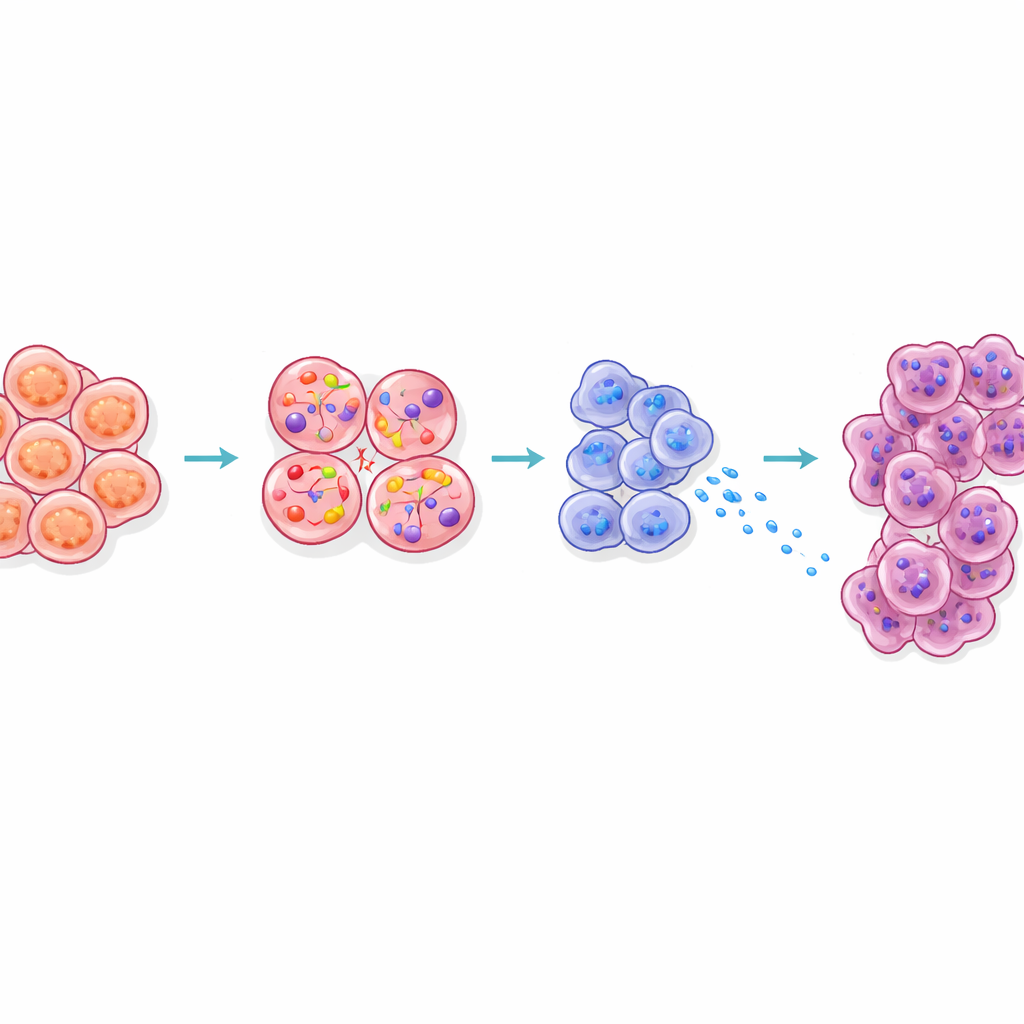
Wie das Signal benachbarte Zellen erreicht und vorbereitet
Die Studie untersuchte auch, wie CCK aus Beta-Zellen das umliegende Gewebe umgestaltet. Azinuszellen, die normalerweise Verdauungsenzyme ausschütten, liegen unmittelbar neben den Inseln im Pankreas. Bei adipösen Mäusen zeigten Azinuszellen in Inselnähe ein Stress-Signaturmuster, produzierten mehr Verdauungsenzyme und Reg-Proteine und wechselten in Zustände, die bekanntermaßen leichter in Krebs überführbar sind. Das Blockieren der CCK-Signalgebung bei adipösen Mäusen reduzierte diese Reg-Signale. Dreidimensionale Bildgebung zeigte außerdem, dass frühe präkanzeröse Läsionen bei adipösen Tieren ungewöhnlich dicht an Inseln entstanden. Zusammengenommen legen diese Ergebnisse nahe, dass von gestressten Beta-Zellen diffundierendes CCK eine „Hot-Zone“ um Inseln schafft, in der Verdauungszellen darauf vorbereitet werden, Tumore zu bilden.
Gemeinsame Muster mit menschlichem Diabetes und ein zentraler Schalter
Beim Vergleich der Mausdaten mit menschlichem Pankreasgewebe von Personen mit und ohne Typ‑2‑Diabetes fanden die Autorinnen und Autoren auffällige Parallelen: Beta-Zellen aus diabetischen Spendern ordneten sich denselben gestressten, weniger ausgereiften Zuständen zu, wie sie bei adipösen Mäusen beobachtet wurden. Anschließend führten sie eine regulatorische Analyse durch, um zu klären, was CCK in Beta-Zellen einschaltet, und identifizierten einen stress-reaktiven Signalweg um das Protein cJun. Als sie den upstream JNK–cJun‑Weg in adipösen Mäusen oder in beta‑ähnlichen Zellen in der Kultur blockierten, sanken die CCK-Spiegel, und cJun zeigte Bindung in der Nähe einer regulatorischen Region des CCK-Gens. Das legt nahe, dass chronischer Stress JNK–cJun aktiviert, wodurch Beta-Zellen in einen CCK-produzierenden Modus umgeschaltet werden.
Was das für gefährdete Menschen bedeutet
Für eine nichtfachliche Leserschaft ist die zentrale Botschaft: Unter Belastung durch Adipositas und Diabetes versagen die Insulinzellen des Pankreas nicht nur — sie passen sich so an, dass sie unbeabsichtigt benachbarte Zellen zur Krebsbildung anregen. Sie tun dies, indem sie CCK hochregulieren, ein Hormon, das als Wachstums- und Stresssignal für benachbarte Verdauungszellen wirkt und so einen fruchtbaren Boden für Tumore schafft. Da pankreasspezifisches CCK nicht wesentlich für die Aufrechterhaltung der Blutzuckerkontrolle ist, könnte das gezielte Anvisieren dieser Hormonquelle oder ihres stressaktivierten Schalters prinzipiell das Risiko für Pankreaskrebs bei Menschen mit Adipositas oder Typ‑2‑Diabetes senken, ohne das gesamte Hormongleichgewicht zu stören. Die Arbeit stellt Pankreaskrebs als Krankheit fehlgeleiteter Kommunikation zwischen den beiden Seiten des Organs dar und weist neue Wege zur frühen Prävention auf.
Zitation: Garcia, C.C., Venkat, A., McQuaid, D.C. et al. Beta cell-derived cholecystokinin drives obesity-associated pancreatic adenocarcinoma development. Nat Commun 17, 3292 (2026). https://doi.org/10.1038/s41467-026-69821-2
Schlüsselwörter: Pankreaskrebs, Adipositas, Beta-Zellen, Cholecystokinin, Typ-2-Diabetes