Clear Sky Science · de
Die Bildung einer zusammengesetzten SMG5‑SMG6‑PIN‑Domäne ist für NMD essenziell
Wie sich Zellen vor fehlerhaften Nachrichten schützen
Unsere Zellen lesen ständig genetische Botschaften (mRNAs), um Proteine herzustellen. Diese Botschaften enthalten jedoch manchmal vorzeitige Stoppzeichen, die verkürzte und potenziell schädliche Proteine produzieren würden. Der Prozess, der solche fehlerhaften Nachrichten zerstört, heißt nonsense‑vermittelter mRNA‑Abbau (NMD). Diese Studie zeigt, wie zwei Schlüsselproteine, SMG5 und SMG6, physisch zusammenarbeiten, um defekte Nachrichten zu zerschneiden, und erklärt damit ein lange bestehendes Rätsel der zellulären Qualitätskontrolle.
Die verborgene Partnerschaft entdecken
Jahrelang wussten Forscher, dass SMG6 RNA direkt spalten kann, während SMG5 als „katalytisch tot“ galt und hauptsächlich als Helfer oder Gerüst fungiert. Zelluläre Experimente zeigten jedoch ein widersprüchliches Bild: SMG6 funktionierte nicht richtig ohne SMG5, und NMD brach zusammen, wenn eines der beiden fehlte. Die Autoren nutzten moderne Strukturvorhersage (AlphaFold), biochemische Tests mit gereinigten Proteinen und genetische Versuche in menschlichen Zelllinien, um diesen Widerspruch zu klären. Ihre Modelle sagten voraus, dass die C‑Enden von SMG5 und SMG6, sogenannte PIN‑Domänen, nebeneinander andocken und eine gemeinsame Struktur bilden. Diese zusammengesetzte Einheit — als „cPIN“ bezeichnet — wurde als die eigentliche Schneidemaschine in der NMD vorgeschlagen. 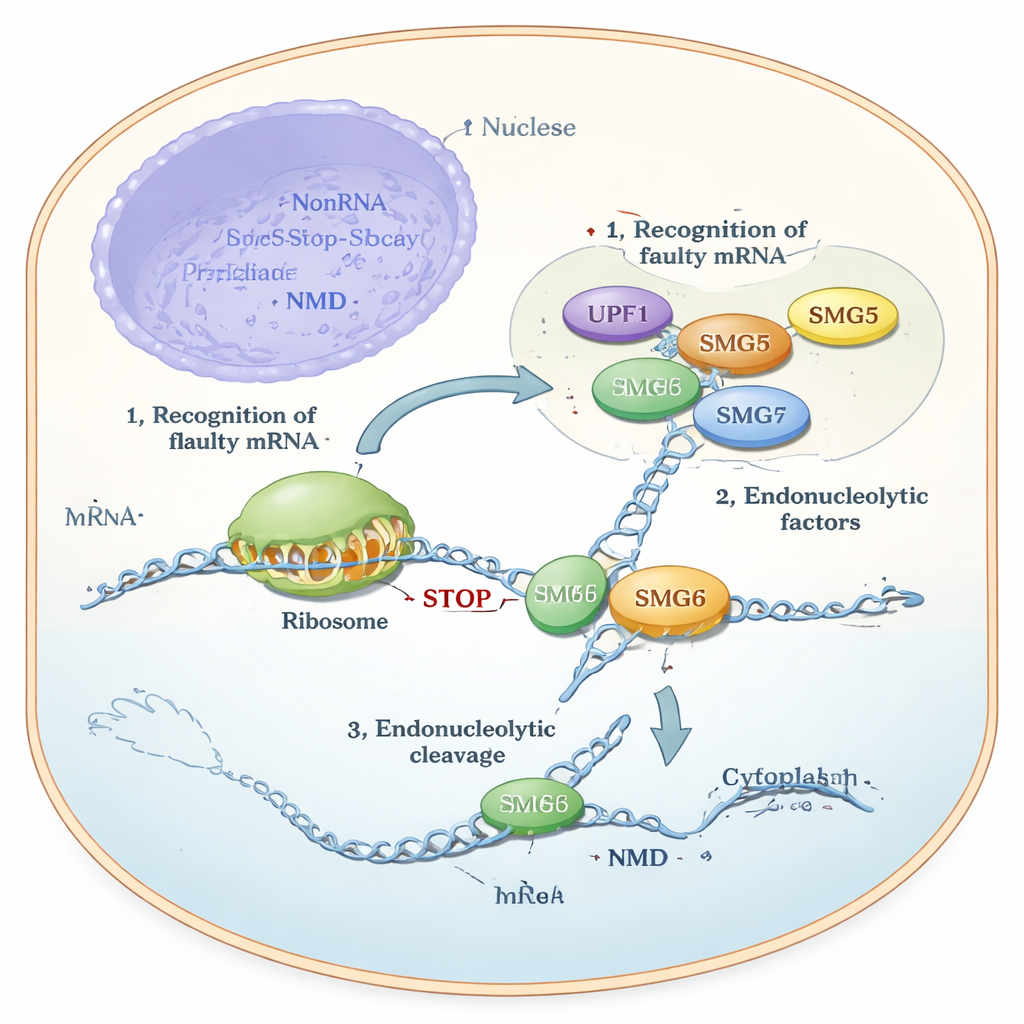
Die molekularen Scheren im Reagenzglas nachbauen
Um die Vorhersage zu testen, stellten die Forscher Fragmente menschlicher SMG5‑ und SMG6‑Proteine in Bakterien her und reinigten sie. Allein zeigte SMG6 nur eine schwache Fähigkeit, ein entworfenes RNA‑Substrat zu schneiden, und SMG5 allein zeigte praktisch keine Aktivität. Wenn die beiden Fragmente jedoch gemischt wurden, stieg die Spaltaktivität deutlich an — auch unter Bedingungen, bei denen Verunreinigungsenzyme kaum eine Rolle spielen konnten. Derselbe Effekt trat sowohl bei linearen als auch bei zirkulären RNA‑Testmolekülen auf, was darauf hindeutet, dass die verstärkte Spaltung tatsächlich vom SMG5–SMG6‑Paar stammt. Chemische Quervernetzung und Massenspektrometrie zeigten zudem, dass die beiden Proteine in engen Kontakt kommen, was die Idee einer direkten, wenn auch transienten, Partnerschaft stützt.
Die Schneidekante vervollständigen
Die Strukturmodelle erklärten genau, wie SMG5 SMG6 stärkt. SMG6 liefert vier saure Aminosäuren, die Metallionen im Zentrum der Spaltstelle binden, wie es für diese Enzymfamilie typisch ist. Überraschenderweise platzieren die Modelle noch eine zusätzliche saure Seitekette von SMG5 direkt daneben und erweitern damit effektiv die katalytische Tasche. Weitere positiv geladene Reste auf SMG5 wurden vorhergesagt, den RNA‑Rückgrat zu greifen und so die Positionierung für die Spaltung zu unterstützen. Wenn die Forscher diese kritischen Reste in SMG5 oder SMG6 mutierten, verlor der zusammengesetzte Komplex in vitro einen Großteil seiner Spaltkraft. Dieselben Mutationen konnten auch in gentechnisch veränderten menschlichen Zellen, aus denen das normale Protein entfernt worden war, NMD nicht wiederherstellen — ein enger Zusammenhang zwischen Strukturmodell und zellulärer Funktion.
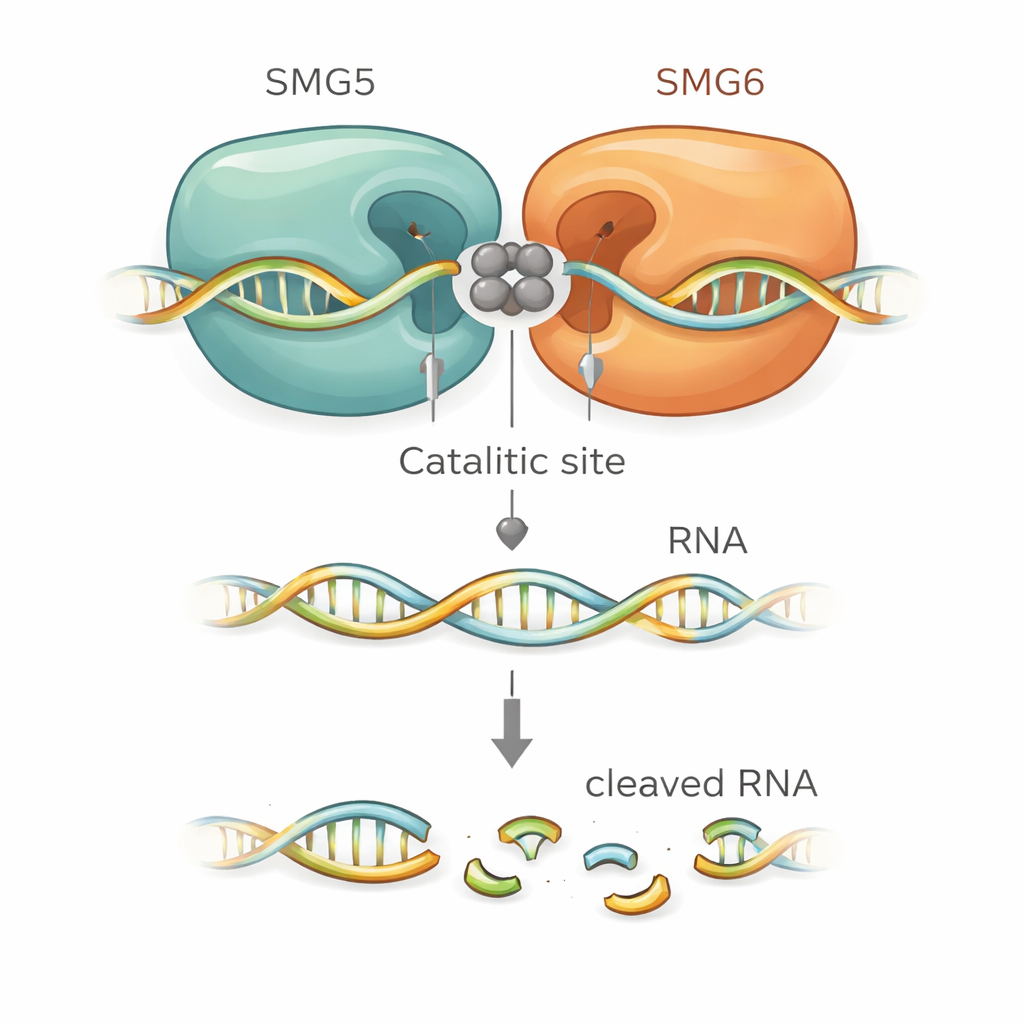
Nachweis, dass beide Partner in Zellen unverzichtbar sind
Da das vollständige Entfernen von SMG5 oder SMG6 Zellen tötet, verwendete das Team ein „Degron“-System, mit dem sich jedes Protein so markieren lässt, dass es schnell durch ein kleines Molekül zerstört werden kann. Die Kombination dieses schnellen Abbaus mit RNA‑Interferenz ermöglichte die nahezu vollständige Entfernung von SMG5, SMG6 oder eines zentralen Regulators namens UPF1. Eine genomweite RNA‑Sequenzierung enthüllte anschließend, was mit NMD geschieht, wenn jeder Faktor verloren geht. Die Depletion von SMG5 oder UPF1 führte zu nahezu identischen Veränderungen in zellulären RNAs, wobei fehlerhafte, NMD‑sensible Transkripte stark akkumulierten. Die Entfernung von SMG6 zeigte ein sehr ähnliches, wenn auch leicht abgeschwächtes Bild. Diese Daten belegen, dass SMG5 und SMG6 keine optionalen, parallelen Zweige des Weges sind; vielmehr wirken sie gemeinsam mit UPF1 als Kernkomponenten eines Hauptabbauswegs.
Warum das für die Zellgesundheit wichtig ist
Kurz gefasst zeigt die Studie, dass SMG5 und SMG6 zusammenkommen, um ein einziges, leistungsfähiges molekulares Scherenpaar zu bilden, das defekte genetische Botschaften durchtrennt. SMG6 stellt den Großteil der Klinge bereit, SMG5 liefert jedoch eine fehlende Schneidekante und hilft, die RNA an Ort und Stelle zu halten, wodurch aus einem schwachen Schnitter ein effizienter wird. Diese zusammengesetzte „cPIN“ erklärt, warum Zellen beide Proteine unbedingt benötigen, um ihre RNA‑Botschaften sauber zu halten. Indem die Arbeit klärt, wie der entscheidende Spalt‑Schritt der NMD nur dann aktiviert wird, wenn fehlerhafte Nachrichten erkannt sind, liefert sie ein klareres Bild davon, wie Zellen die Ansammlung toxischer, verkürzter Proteine verhindern und die Genexpression fein regulieren.
Zitation: Kurscheidt, K., Theunissen, S., Pasquali, N. et al. Composite SMG5-SMG6 PIN domain formation is essential for NMD. Nat Commun 17, 1934 (2026). https://doi.org/10.1038/s41467-026-69819-w
Schlüsselwörter: nonsense‑vermittelte mRNA‑Abbau, RNA‑Qualitätskontrolle, SMG5 SMG6, mRNA‑Überwachung, Genexpressionsregulation