Clear Sky Science · de
Tumorzell‑Dörfer definieren die Ko‑Abhängigkeit von Tumor und Mikroumgebung bei Leberkrebs
Warum winzige „Dörfer“ innerhalb von Tumoren wichtig sind
Krebs wird oft als Ansammlung entarteter Zellen beschrieben, doch diese Studie zu Leberkrebs zeichnet ein weitaus geordneteres Bild. Innerhalb von Tumoren ordnen sich Zellen zu winzigen „Dörfern“ an, die mit benachbarten Stütz‑, Gefäß‑ und Immunzellen zusammenarbeiten. Zu verstehen, wie diese Mini‑Gemeinschaften entstehen und funktionieren, könnte erklären, warum manche Tumoren aggressiver sind als andere, und neue Ansätze liefern, um sie zu stören.
Tumoren Zelle für Zelle in ihrer natürlichen Umgebung betrachten
Die meisten modernen Krebsstudien isolieren Zellen aus dem Tumor und messen ihre Genaktivität in Reagenzgläsern, wodurch entscheidende Informationen darüber verloren gehen, wo jede Zelle lag und wer ihre Nachbarn waren. In dieser Arbeit kombinierten Forschende zwei leistungsfähige Ansätze an Proben von sieben Patient:innen mit primärem Leberkrebs. Sie nutzten eine hochauflösende Bildgebungsplattform, um RNA‑Moleküle direkt in Schnitten des Tumorgewebes zu messen und über 2,3 Millionen Zellen in situ zu kartieren, und kombinierten dies mit Einzelzell‑RNA‑Sequenzierung aus denselben Tumoren. So konnten sie nicht nur sehen, was jede Zelle tat, sondern auch, wo sie sich im Tumor befand und welche Zelltypen sie umgaben. 
Unterscheidbare „Persönlichkeiten“ von Krebszellen entdecken
Durch die Analyse von Genaktivitätsmustern identifizierte das Team rund ein Dutzend verschiedener „Zustände“ maligner Leberkrebszellen. Einige konzentrierten sich auf schnelle Teilung, andere auf Stress‑Reparatur, Reaktion auf Immunangriffe, Bewegung und Invasion des umliegenden Gewebes oder die Nachahmung normaler Leber‑ oder Gallengangszellen. Diese Zustände stimmten eng mit Mustern überein, die in anderen Krebsarten beobachtet wurden, was auf gemeinsame Themen über Tumorarten hinweg hinweist, jedoch mit einer leberspezifischen Ausprägung. Normale, nicht‑krebsartige epithelialen Zellen in denselben Proben zeigten ein deutlich engeres Zustands‑Spektrum, was die ungewöhnliche Vielfalt der Tumorzellen hervorhebt.
Die Nachbarschaft bestimmt, was aus Krebszellen wird
Die Forschenden fragten sich dann, wie das lokale Umfeld diese Krebszellzustände beeinflusst. Für jede maligne Zelle katalogisierten sie alle Nachbarzellen in einem Bereich von etwa der Breite eines menschlichen Haares und gruppierten ähnliche Nachbarschaften in sogenannte Spatial Dynamics Networks. Manche Nachbarschaften waren dicht von Blutgefäßen durchzogen, andere wurden von Tumorzellen dominiert, wieder andere waren reich an Immunzellen oder Fibroblasten (Zellen, die Bindegewebe aufbauen). Krebszellen in einem bestimmten Zustand tauchten nicht zufällig auf. Zum Beispiel saßen Zellen, die einen Formwandelprozess mit Invasion verbinden, tendenziell in der Nähe dichter Gefäßnetze, während stark teilende Zellen in tumorlastigen Regionen mit wenigen Nicht‑Tumorzellen gehäuft vorkamen. Dieses nicht‑zufällige Muster zeigt, dass Mikroumgebung und Tumorzellverhalten eng verflochten sind.
Tumor‑„Dörfer“ als kooperative Ökosysteme
Um über einzelne Zellen hinauszugehen, nutzte das Team eine Art Deep‑Learning‑Modell, das jeden Tumor als Graphen verbundener Zellen behandelt. Das Modell lernte sowohl aus dem internen Zustand jeder malignen Zelle als auch aus der Art der Nachbarschaft, die sie bewohnte. Das Clustern dieser gelernten Repräsentationen offenbarte acht wiederkehrende Tumor‑„Dörfer“. Jedes Dorf kombinierte bestimmte Krebszellzustände mit charakteristischen Umgebungen — etwa blutgefäßreiche Bereiche mit invasiven Zellen oder „Keimzentren“ schnell teilender Tumorzellen. Als die Wissenschaftler:innen Hunderte zusätzlicher Leberkrebs‑Patient:innen in anderen Datensätzen untersuchten, stellten sie fest, dass Patient:innen, deren Tumoren von bestimmten Dörfern (bezeichnet 3–8) dominiert waren, tendenziell eine schlechtere Überlebensprognose hatten als solche mit Anreicherung für Dörfer 1 und 2. Das legt nahe, dass die Zusammensetzung der Dörfer aussagt, wie gefährlich das Ökosystem eines Tumors ist. 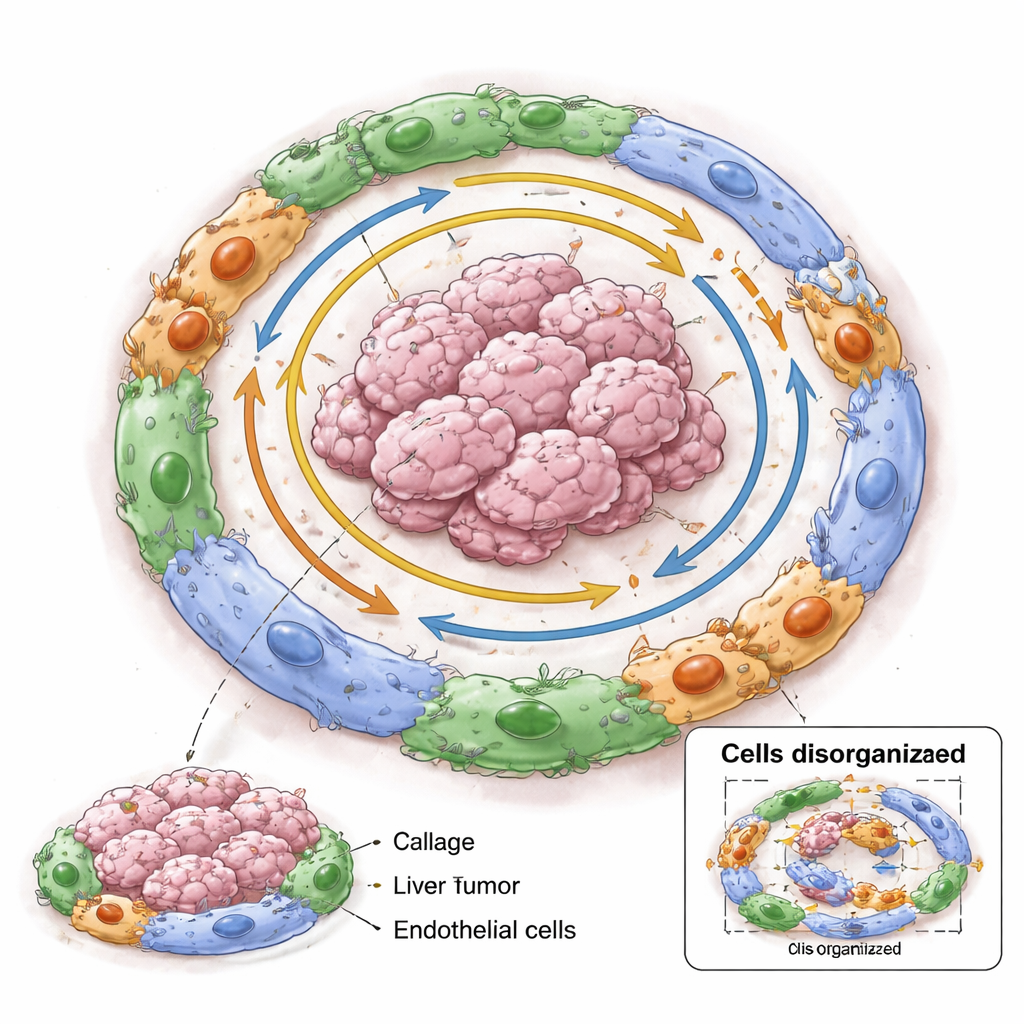
Molekulare Absprachen zwischen Krebszellen und ihren Nachbarn
Innerhalb jedes Dorfes suchten die Forschenden nach Genpaaren — eines aktiv in Tumorzellen, eines in benachbarten Nicht‑Tumorzellen — die räumlich zusammen an‑ und abnahmen. Diese „ko‑abhängigen“ Paare variierten von Dorf zu Dorf und schwächten sich mit zunehmendem Abstand zwischen den Zellen ab, was auf hochlokale molekulare Beziehungen hinweist. Ein auffälliges Beispiel betraf ein von Tumorzellen produziertes Protein namens SPINK1 und kollagenproduzierende Fibroblasten, bekannt als matrix‑assoziierte Krebs‑Fibroblasten. SPINK1‑positive Tumorzellen fanden sich häufig neben diesen Fibroblasten, und die Signalübertragung zwischen ihnen — wahrscheinlich über einen bekannten Rezeptor namens EGFR — wurde mit Merkmalen der Metastasierung in Verbindung gebracht. Als die Forschenden in ihren Modellen die Nachbarn von Tumorzellen „durchmischten“, fiel die Fähigkeit, Dörfer korrekt zu erkennen, ab, besonders in solchen Dörfern mit vielen SPINK1‑verknüpften Interaktionen. Das legt nahe, dass diese molekularen Absprachen die Dorfstruktur mittragen.
Was das für Patient:innen bedeutet
Für eine allgemeine Leserschaft ist die Kernbotschaft: Lebertumoren sind keine zufälligen Zellhaufen. Sie organisieren sich selbst in kleine Gemeinschaften — Dörfer — in denen Krebszellen und umgebende Stütz‑ und Immunzellen wechselseitig voneinander abhängig sind, um zu wachsen, zu streuen und Therapien zu widerstehen. Manche Dorftypen sind mit besserer, andere mit schlechterer Überlebensprognose verbunden, und jedes birgt seine eigenen molekularen Abhängigkeiten. Künftige Therapien könnten darauf abzielen, nicht nur einzelne Krebszellen zu töten, sondern bestimmte Dörfer zu zersetzen oder zu „verhungern“, indem die Beziehungen zwischen Tumorzellen und ihren Nachbarn gezielt gestört werden — womit der gesamte Tumor verwundbarer würde.
Zitation: Liu, M., Hernandez, M.O., Castven, D. et al. Tumor cell villages define the co-dependency of tumor and microenvironment in liver cancer. Nat Commun 17, 1986 (2026). https://doi.org/10.1038/s41467-026-69797-z
Schlüsselwörter: Leberkrebs, tumorale Mikroumgebung, räumliche Transkriptomik, intratumorale Heterogenität, Tumorzellzustände