Clear Sky Science · de
Das S‑nitrosoglutathion‑Reduktase GSNOR treibt altersbedingte Fettleibigkeit voran, indem es Fettgewebe durch De‑nitrosierung von Beclin‑1 weißer macht
Warum Gewichtszunahme in der Lebensmitte wichtig ist
Viele Menschen bemerken, dass es in den 40er‑ und 50er‑Jahren schwieriger wird, schlank zu bleiben, selbst wenn sie nicht mehr essen oder sich weniger bewegen. Diese Gewichtszunahme in der Lebensmitte erhöht das Risiko für Diabetes, Herzkrankheiten und andere Erkrankungen, doch ihre biologischen Ursachen werden erst allmählich aufgeklärt. Diese Studie deckt einen bislang verborgenen Schuldigen im Fettgewebe selbst auf: ein Enzym namens GSNOR, das verändert, wie Fettzellen mit Energie umgehen, wenn wir altern, und sie dazu bringt, mehr zu speichern und weniger zu verbrennen.
Wärme erzeugendes Fett versus Speichermetabolismus
Unser Körper enthält mehr als eine Art von Fett. Klassisches weißes Fett ist der bekannte Energiespeicher, bestehend aus großen, blassen Zellen mit einem einzelnen großen Tropfen. Beiges und braunes Fett dagegen sind mit vielen kleinen Tropfen und zahlreichen Mitochondrien ausgestattet, den „Öfen“ der Zelle, die Brennstoff verbrennen, um Wärme zu produzieren. In jungen Jahren hilft ein höherer Anteil beigen Fettes, Gewicht und Blutzucker zu kontrollieren. Mit dem Alter neigt dieses beige Fett jedoch dazu, „weiß zu werden“: Die Mitochondrien werden abgebaut, die Zellen schwellen durch gespeichertes Fett an und der Gesamtstoffwechsel verlangsamt sich.
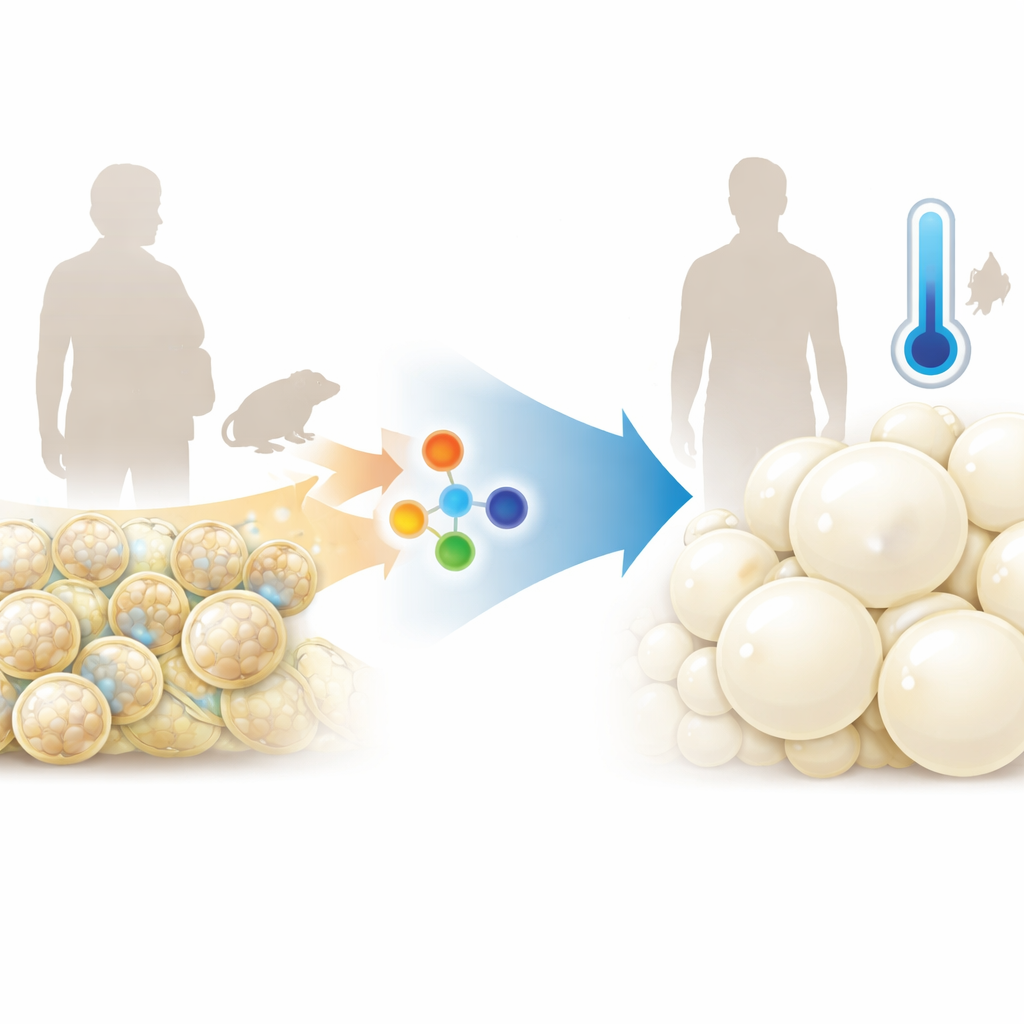
Ein altersabhängiger Schalter im Fettgewebe
Die Forschenden fanden heraus, dass die GSNOR‑Spiegel speziell im subkutanen weißen Fett mittelalterlicher Mäuse und Männer ansteigen, jedoch nicht in allen Fettdepots. GSNOR steuert ein auf Stickstoffmonoxid beruhendes chemisches Signal, das viele Proteine modifiziert. Als das Team das GSNOR‑Gen bei Mäusen entfernte, blieben diese Tiere weitgehend gegen altersbedingte Gewichtszunahme gefeit. Sie trugen weniger Fett, mehr fettfreie Masse, hatten eine bessere Blutzuckerregulation und verbrannten mehr Energie, ohne weniger zu fressen oder sich mehr zu bewegen als normale Mäuse. Ihre inguinalen Fettpolster enthielten kleinere Zellen und mehr beige‑artige Merkmale, mit höheren mitochondrialen Markern und stärkerer wärmeproduzierender Aktivität.
Ein höherer GSNOR‑Spiegel fördert Weißfärbung und Fettleibigkeit
Um die Gegenrichtung zu testen, erhöhten die Forschenden GSNOR gezielt nur in Fettzellen, entweder durch virale Übertragung in ein Fettdepot oder durch Erzeugen einer Knock‑in‑Maus, die das Enzym im Fettgewebe überexprimierte. In beiden Fällen wurden die Fettzellen größer und blasser, mitochondriale Marker fielen und Gene, die mit beigem Fett und Wärmeproduktion verknüpft sind, wurden unterdrückt. Die Knock‑in‑Mäuse waren deutlich fettleibig, weniger fähig, die Körpertemperatur bei Kälte zu halten, und zeigten geringere Sauerstoffaufnahme und Energieverbrauch. Wichtig ist, dass diese Veränderung nicht von erhöhter Nahrungsaufnahme oder reduziertem Fettabbau herrührte, sondern auf eine Umprogrammierung der Fettzellidentität hin zu Energiespeicherung hindeutete.
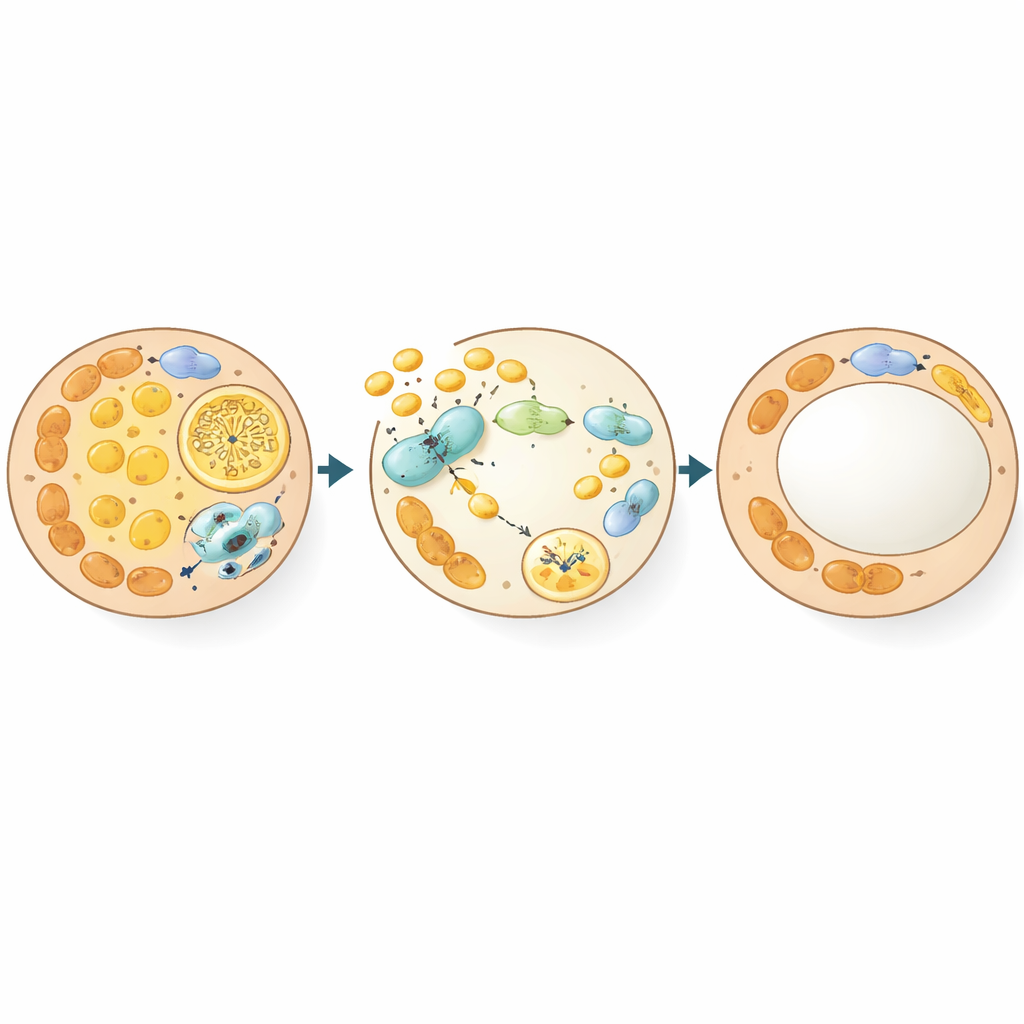
Eine verborgene Bremse für zelluläres Recycling
Bei genauerer Betrachtung fragten die Forschenden, wie GSNOR Fettzellen auf molekularer Ebene umgestaltet. Mit sensitiven proteomischen Methoden kartierten sie Proteine, deren Stickstoffmonoxid‑basierte Modifikation sich änderte, wenn GSNOR hoch war. Ein zentrales Ziel tauchte auf: Beclin‑1, ein Schlüsselorganisator der Autophagie, des Prozesses, mit dem Zellen Komponenten, einschließlich Mitochondrien, recyceln. Normalerweise kann sich Stickstoffmonoxid an Beclin‑1 an einem spezifischen Cysteinrest anheften und so die Autophagie bremsen. Wenn die GSNOR‑Spiegel steigen, wird diese Modifikation entfernt, Beclin‑1 bindet stärker an seinen Partner ATG14 und die Autophagie wird hochgefahren. In Fettzellen löscht dieses verstärkte Recycling bevorzugt Mitochondrien aus, wodurch beige Zellen wieder in den weißeren, speicherorientierten Zustand kippen. Elektronenmikroskopie und molekulare Marker bestätigten, dass GSNOR‑reiche oder Beclin‑1‑mutierte Fettzellen während des Beige‑zu‑Weiß‑Übergangs mehr Autophagosomen und weniger Mitochondrien aufwiesen.
Umprogrammierung von Beclin‑1 bestätigt den Mechanismus
Um zu zeigen, dass diese einzelne Stelle auf Beclin‑1 entscheidend ist, erzeugten die Autorinnen und Autoren Mäuse, in denen dieses Cystein so ersetzt wurde, dass es den Stickstoffmonoxid‑Anhang nicht mehr tragen kann. Diese Beclin‑1C351A‑Tiere zeigten in Fettgewebe mehr Autophagie, einen schnelleren Verlust beige‑typischer Merkmale und stärkere Weißfärbung, nachdem Kälte oder medikamentös induzierte Bräunung aufgegeben wurden, obwohl ihr Gesamtgewicht nicht sofort veränderte. In Zellkulturen konnte das Blockieren von GSNOR beige Eigenschaften nur erhalten, solange Beclin‑1 noch seine modifizierbare Stelle hatte; nach der Mutation half der Verlust von GSNOR nicht mehr. Schließlich stellte lokales Abschalten von GSNOR in einem Fettdepot bei mittelalten Mäusen beige Marker wieder her, verkleinerte Fettzellen und reduzierte die lokale Fettmasse, was unterstreicht, dass dieser Signalweg bei erwachsenen Tieren manipulierbar ist.
Was das für Gewichtszunahme in der Lebensmitte bedeutet
Kurz gesagt identifiziert diese Arbeit GSNOR als altersaktivierten Schalter im Fettgewebe, der den Verlust des „guten“, wärmebildenden beigen Fettes beschleunigt, indem er die zelluläre Recycling‑Maschinerie über Beclin‑1 überaktiviert. Wenn GSNOR in der Lebensmitte ansteigt, entfernt es das schützende Stickstoffmonoxid‑Tag von Beclin‑1, erlaubt übermäßiges Entfernen von Mitochondrien, Weißfärbung des Fettes, langsameren Stoffwechsel und eine erhöhte Anfälligkeit für Adipositas. Die Ergebnisse deuten darauf hin, dass Wirkstoffe, die GSNOR im subkutanen Fett sanft hemmen — oder anderweitig das Stickstoffmonoxid‑Markierung auf Beclin‑1 wiederherstellen — dazu beitragen könnten, die Funktion beigen Fettes zu bewahren und altersbedingter Gewichtszunahme sowie metabolischem Abbau entgegenzuwirken.
Zitation: Qiao, X., Xie, T., Zhang, Y. et al. S-nitrosoglutathione reductase GSNOR drives age-related obesity by promoting adipose tissue whitening through de-nitrosation of Beclin-1. Nat Commun 17, 3059 (2026). https://doi.org/10.1038/s41467-026-69793-3
Schlüsselwörter: altersbedingte Fettleibigkeit, beiges Fett, GSNOR, Autophagie, Nitric‑oxide‑Signalgebung