Clear Sky Science · de
Nicht-hydrolysierbare Acetyllysin-Analoga zur Untersuchung der Proteinacetylierung in vitro und in Zellen
Warum winzige chemische Anhängsel an Proteinen wichtig sind
Innerhalb jeder Zelle werden Proteine ständig mit kleinen chemischen Anhängseln versehen, die wie Ein/Aus-Schalter oder Dimmregler für ihre Aktivität wirken. Eines der wichtigsten dieser Anhängsel ist die Acetylierung, die das Verhalten eines Proteins verändern kann, ohne den zugrundeliegenden genetischen Code zu ändern. Es ist überraschend schwer, genau zu verstehen, was eine Acetylierung an einer bestimmten Stelle eines bestimmten Proteins bewirkt, weil Zellen diese Anhängsel ebenso schnell entfernen können, wie sie sie anbringen. Diese Studie stellt einen cleveren chemischen »Stand‑in« für Acetylierung vor, der nicht entfernt werden kann, und gibt Wissenschaftlern so die Möglichkeit, solche Schalter festzusetzen und zu beobachten, was passiert.
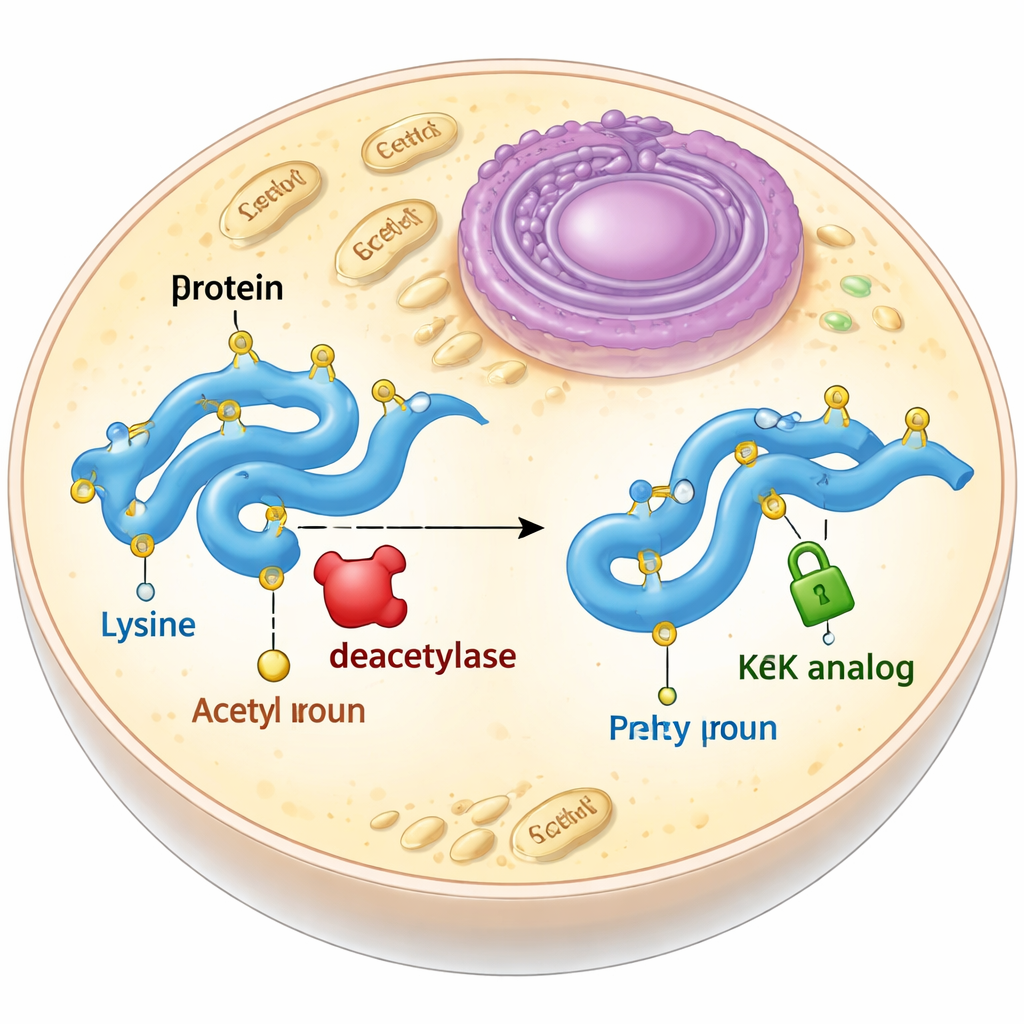
Ein stabiler Ersatz für ein flüchtiges Anhängsel
Acetylierung erfolgt meist an einer Aminosäurebausteinseite namens Lysin. Wenn ein Lysin acetylier t wird, verliert es seine positive Ladung und seine Seitenkette wird etwas länger. Biologen versuchen häufig, dies zu imitieren, indem sie Lysin in eine andere Aminosäure wie Glutamin umwandeln, die ungeladen, aber kürzer ist, oder indem sie echtes Acetyllysine mithilfe einer erweiterten genetischen Codeweitergabe einbauen. Beide Ansätze haben Nachteile: Glutamin reproduziert nicht vollständig die durch Acetylierung verursachten Formänderungen, und echtes Acetyllysine wird in Zellen schnell von Enzymen namens Deacetylasen wieder entfernt. Die Autorinnen und Autoren wollten daher Acetyllysin‑Nachahmer entwerfen und testen, die die richtige Größe und Form beibehalten, aber nicht entfernt werden können.
Testen neuer chemischer Nachahmer an einem Modellprotein
Das Team konzentrierte sich zunächst auf Ubiquitin, ein kleines, gut untersuchtes Protein, das selbst mit vielen verschiedenen Anhängseln versehen wird. Mit fortgeschrittener gentechnischer Technik setzten sie an einer Position in Ubiquitin verschiedene Lysin‑Varianten ein: natürliches Acetyllysine, zwei nicht entfernbaren Analoga namens TFAcK und Ketolysin (KeK) sowie gebräuchliche Ersatzstoffe wie Glutamin, Alanin und Arginin. Anschließend untersuchten sie, wie diese Veränderungen Form und Funktion von Ubiquitin beeinflussten. Hochauflösende NMR‑Messungen zeigten, dass Acetyllysine, TFAcK und KeK nahezu identische strukturelle Veränderungen hervorriefen, insbesondere in der Umgebung einer zentralen Helix, während Glutamin und andere einfache Mutationen dies nicht taten. Funktionelle Tests mit einem Enzym namens HDM2 ergaben, dass Ubiquitin mit Acetyllysine, TFAcK oder KeK sich ähnlich verhielt und sich vom Glutamin‑Variant unterschied, was deutlich macht, dass Länge und Volumen der Seitenkette – nicht nur ihre Ladung – entscheidend sind.
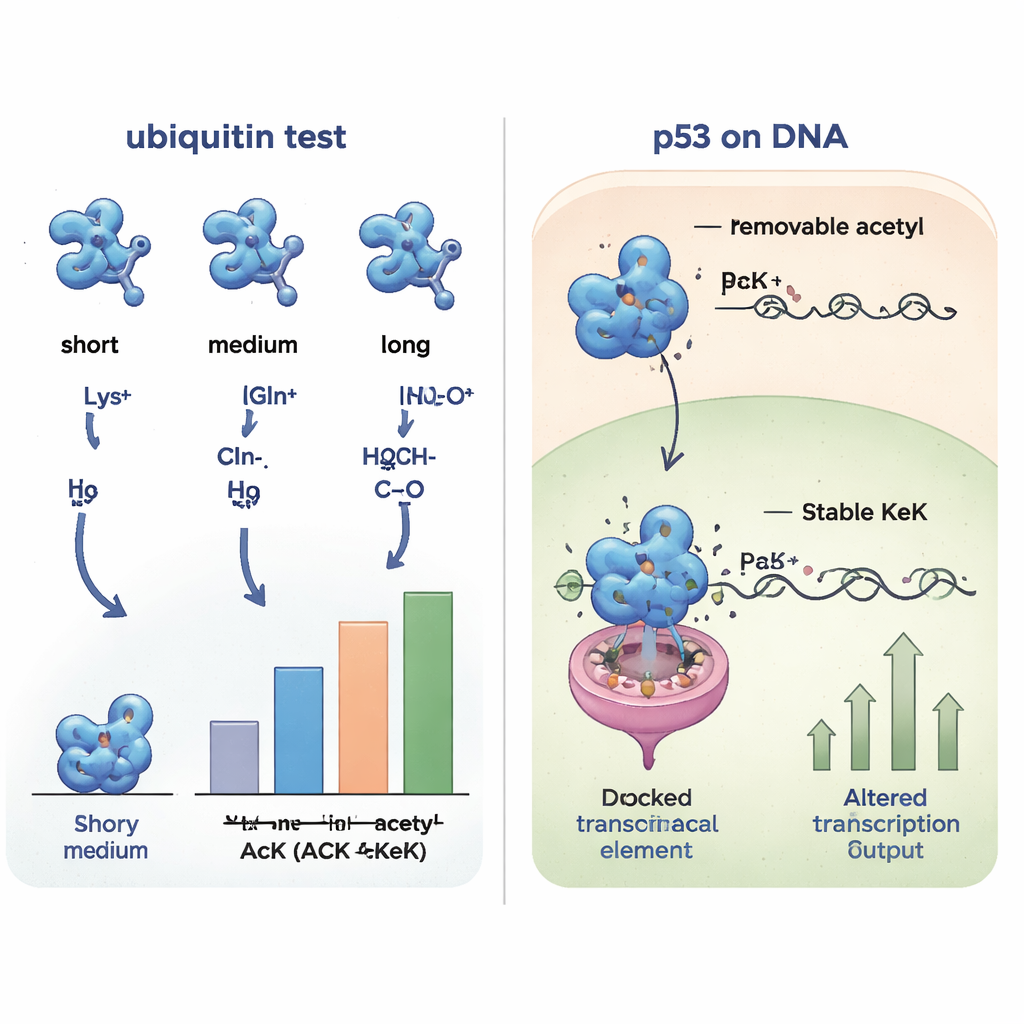
Untersuchung von Protein‑Partnern quer durch die Zelle
Da kleine strukturelle Änderungen beeinflussen können, mit welchen Partnern ein Protein interagiert, verglichen die Forschenden anschließend, wie die verschiedenen Ubiquitin‑Versionen an andere Proteine aus menschlichen Zelllysaten banden. Indem sie Bindungspartner herausfischten und diese mit Massenspektrometrie identifizierten, stellten sie fest, dass Ubiquitin mit Acetyllysine, TFAcK oder KeK sehr ähnliche Interaktionsmuster aufwies, während Formen mit Glutamin oder Alanin zusammen gruppierten und anders aussahen. Positiv geladene Varianten (Lysin oder Arginin) bildeten eine weitere Gruppe. Dieser systematische Vergleich zeigte, dass die nicht entfernbaren Analoga TFAcK und insbesondere KeK sowohl die Struktur als auch das Bindungsverhalten echter Acetylierung deutlich besser nachahmen als die traditionelle Glutamin‑Substitution.
Acetylierung am Tumorsuppressor p53 fixieren
Um zu prüfen, ob diese Werkzeuge auch in lebenden Zellen funktionieren, wandten sich die Autorinnen und Autoren p53 zu, einem wichtigen Tumorsuppressor, der oft als »Wächter des Genoms« bezeichnet wird. Bestimmte Lysinreste in der DNA‑Binderegion von p53 können acetylier t werden und dadurch beeinflussen, welche Gene es aktiviert, etwa solche, die den Zellzyklus stoppen oder den Zelltod auslösen. Das Team konstruierte humane Zellen so, dass p53 Acetyllysine, TFAcK oder KeK an zwei wichtigen Lysinpositionen (120 und 164) nur dann einbaute, wenn die jeweilige nicht‑standard Aminosäure zugegeben wurde. Alle drei konnten in p53 eingebaut werden, aber detaillierte Messungen zeigten, dass in Zellen die Acetyl‑ und TFAcK‑Gruppen weitgehend von Deacetylasen entfernt wurden, während KeK intakt blieb. Bei Tests der Fähigkeit von p53, einen Reportergenkassette sowie das natürliche p21‑Gen zu aktivieren, waren Varianten mit KeK an diesen Stellen deutlich weniger aktiv, was dem entspricht, was zu erwarten ist, wenn Acetylierung an diesen Positionen festgeschrieben wird; Acetyllysine und TFAcK verhielten sich dagegen eher wie normales p53, weil sie deacetylier t worden waren.
Was das für das Studium zellulärer Entscheidungen bedeutet
Insgesamt zeigt die Studie, dass KeK ein getreuer und nicht entfernbarer Stand‑in für Acetyllysine ist: Es reproduziert die strukturellen Veränderungen, Bindungspräferenzen und funktionellen Konsequenzen der Acetylierung sehr genau, kann aber nicht von zellulären Enzymen gelöscht werden. Für Nicht‑Spezialisten bedeutet das: Forschende haben nun eine Möglichkeit, einen normalerweise reversiblen chemischen Schalter an einer einzelnen Stelle eines Proteins »einzufrieren« und anschließend zu beobachten, wie sich das auf Prozesse wie Genregulation und zelluläre Schicksalsentscheidungen auswirkt. Das sollte es erheblich erleichtern, die spezifischen Rollen der Acetylierung von denen anderer überlappender Modifikationen zu trennen und schließlich zu klären, wie fehlregulierte Proteinacetylierung zu Krankheiten wie Krebs beiträgt.
Zitation: Kienle, S.M., Sigg, M., Schneider, T. et al. Non-hydrolyzable acetyllysine analogs to study protein acetylation in vitro and in cells. Nat Commun 17, 1985 (2026). https://doi.org/10.1038/s41467-026-69782-6
Schlüsselwörter: Proteinacetylierung, posttranslationale Modifikation, Ubiquitin, p53, Erweiterung des genetischen Codes