Clear Sky Science · de
Dynamische transkriptomische Umgestaltung in transplantierten humanen neuronalen Vorläuferzellen offenbart Mechanismen zum Erhalt des Sehens in einem Rattenmodell der Retinitis pigmentosa
Warum der Schutz schwindenden Sehens wichtig ist
Retinitis pigmentosa ist eine Gruppe vererbter Erkrankungen, die Menschen schrittweise ihr Sehvermögen rauben, oft beginnend mit Nachtblindheit und bis hin zur gesetzlichen Erblindung. Weil Hunderte verschiedener Genmutationen diese Krankheit auslösen können, ist es schwierig, jede einzelne mit gentherapeutischen Ansätzen zu behandeln. Diese Studie untersucht einen allgemeineren Ansatz: die Transplantation humaner neuronaler Vorläuferzellen — unreifer Nervenzellen, die im Labor gezüchtet wurden — ins Auge, um die verbleibenden lichtempfindlichen Zellen zu schützen. Das genaue Verständnis, wie diese transplantierten Zellen sich verhalten und zum Erhalt des Sehens beitragen, könnte künftige Behandlungen nicht nur für Retinitis pigmentosa, sondern auch für andere erblindende Erkrankungen prägen.
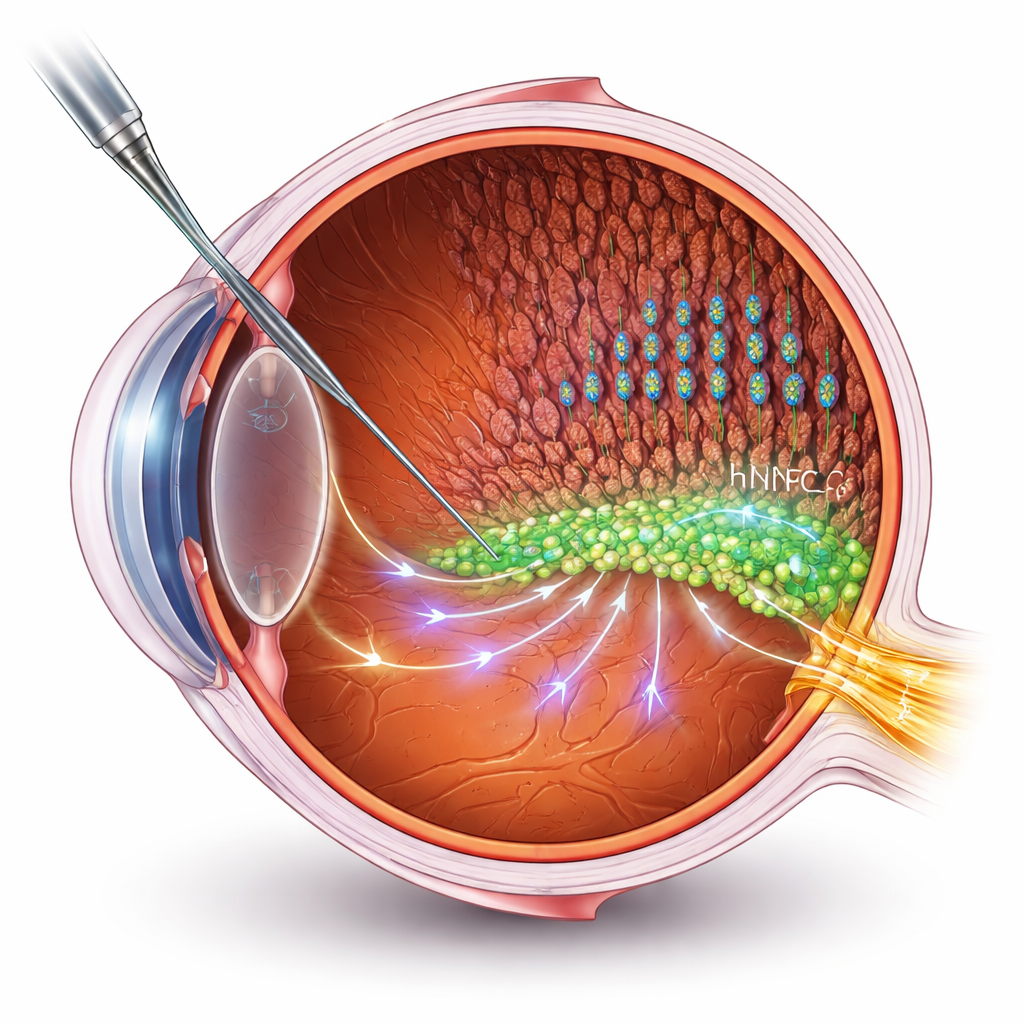
Zellen unterstützen statt ersetzen
Viele Stammzelltherapien zielen darauf ab, tote oder geschädigte Zellen zu ersetzen. Bei fortgeschrittenen Netzhauterkrankungen ist der Aufbau neuer Verbindungen zum Gehirn jedoch eine große technische Hürde. Die Forschenden wählen hier einen anderen Weg: Sie verwenden humane neuronale Vorläuferzellen (hNPCs) als „Helfer“, die die eigenen Netzhautzellen des Patienten unterstützen. Sie transplantierten hNPCs in den subretinalen Raum eines etablierten Rattenmodells der Retinitis pigmentosa und maßen anschließend das Sehvermögen mittels elektrischer Aufzeichnungen und Verhaltenstests. Die behandelten Ratten behielten eine bessere visuelle Funktion und intaktere Photorezeptorschichten — Stäbchen und Zapfen, die Licht aufnehmen — als unbehandelte Tiere, obwohl die Degeneration weiterhin langsam voranschritt.
Wie sich die transplantierten Zellen im kranken Auge verändern
Um auf molekularer Ebene zu sehen, was passiert, nutzte das Team die Einzelzell-RNA-Sequenzierung, eine Technik, die erfasst, welche Gene in Tausenden einzelner Zellen aktiviert sind. Sie verfolgten die transplantierten hNPCs zu zwei Zeitpunkten, ungefähr frühen und späteren Phasen nach der Transplantation. Statt sich in neue Photorezeptoren zu verwandeln, differenzierten die meisten transplantierten Zellen zu astrozytenähnlichen Stützzellen, ein kleinerer Teil zeigte Marker von Oligodendrozyten oder unreifen Neuronen. Im Laufe der Zeit stabilisierten sich diese Zellen und nahmen Eigenschaften an, die darauf hindeuten, dass sie darauf abgestimmt sind, in einer stressigen, degenerierenden Umgebung zu überleben und eng mit benachbarten Netzhautzellen zu interagieren.
Schützende Signale, Stoffwechsel und Aufräumprozesse
Die hNPCs produzierten eine reiche Mischung schützender Proteine, sogenannter tropher Faktoren. Darunter fanden sich MANF und MYDGF, die mit Zellüberleben, reduziertem oxidativem Stress und abgeschwächter Entzündung in Verbindung stehen, sowie andere Faktoren wie Midkine und Pleiotrophin, die Wachstum und Wanderung neuraler Zellen unterstützen. Diese Moleküle schienen sowohl auf das Transplantat selbst als auch auf die umgebende Netzhaut zu wirken. Bei behandelten Ratten zeigten Stäbchen und Zapfen Genaktivitätsmuster, die den gesunden Kontrollen näher kamen, mit verbessertem Support für visuelle Signalübertragung und Zellunterhalt. Die transplantierten Zellen stärkten zudem Wege, die an der Beseitigung zellulärer Trümmer und der Anpassung des Stoffwechsels beteiligt sind, was darauf hindeutet, dass sie Photorezeptoren helfen, mit Energiebedarf und toxischen Nebenprodukten umzugehen, die sich während der Krankheit ansammeln.
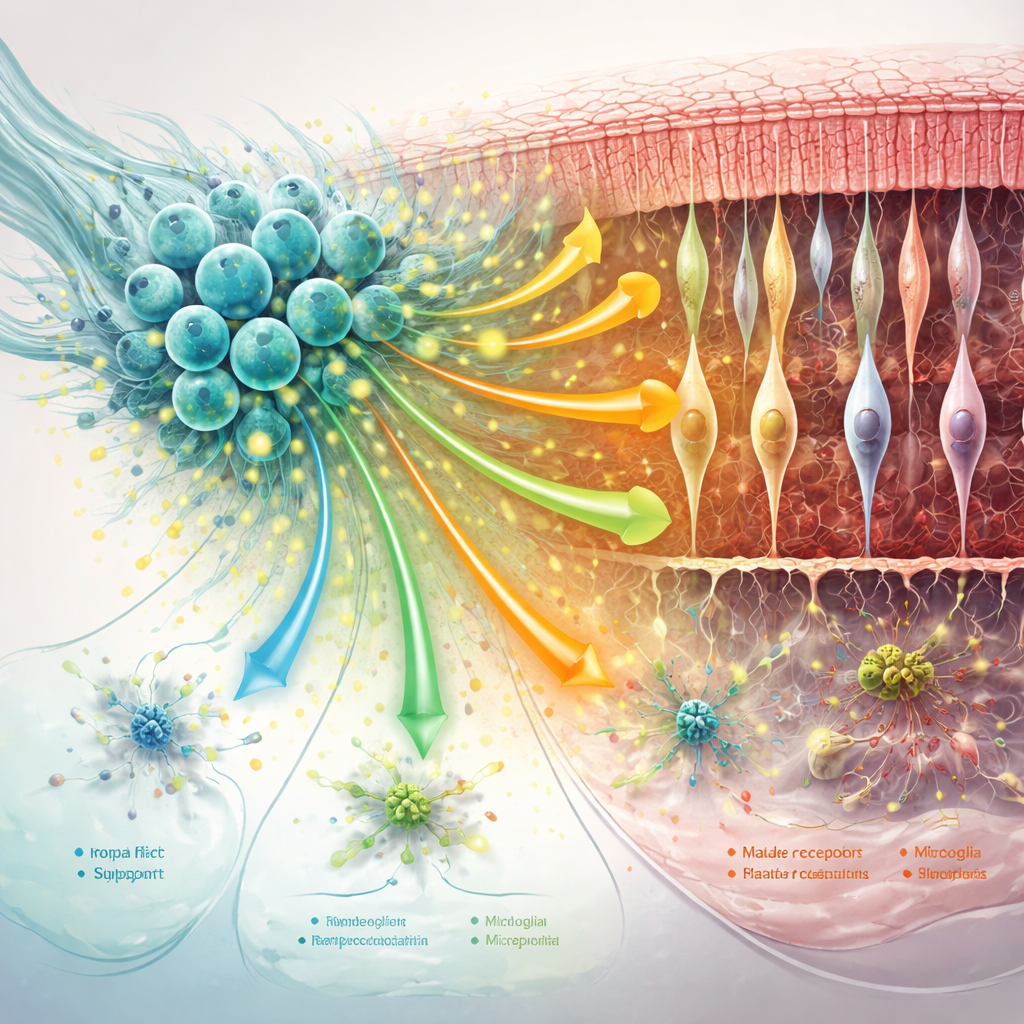
Beruhigen der Stützzellen und Umgestalten der retinalen Nachbarschaft
Das Unterstützungsnetz der Netzhaut — Müller-Glia, Mikroglia und die umgebende Protein-Matrix — spielt eine große Rolle dabei, die Degeneration entweder zu verschlimmern oder zu verlangsamen. Die Studie fand, dass die hNPC-Behandlung Schlüsselmarker schädlicher „reaktiver“ Veränderungen in Müller-Glia abschwächte und Mikroglia besonders in frühen Zeitpunkten von übermäßig entzündlichen Zuständen wegführte. Gleichzeitig wurden Kommunikationssignale gestärkt, die Synapsen stabilisieren, Zellen zusammenhalten und das Gerüst um Photorezeptoren aufrechterhalten. Mit Fortschreiten der Krankheit schwanden einige dieser Vorteile: Die Gesamtkommunikation zwischen Zellen schwächte sich, bestimmte Schutzwege — einschließlich MANF-assoziierter Signalwege — nahmen ab, und Stützzellen nahmen stärker stress- und immunfokussierte Profile an.
Was das für zukünftige Augen-Therapien bedeutet
Für Nicht-Fachleute lautet die Kernaussage, dass transplantierte humane neuronale Vorläuferzellen wie vor Ort agierende „Ersthelfer“ in einer degenerierenden Netzhaut wirken können. Sie bauen die Netzhaut nicht von Grund auf wieder auf, sondern geben schützende Moleküle ab, passen den Stoffwechsel an, dämpfen schädigende Entzündungen und helfen, die lokale Struktur intakt zu halten — Maßnahmen, die den Sehverlust verlangsamen. Dieser Schutzeffekt lässt jedoch mit der Zeit nach, sobald die Umgebung feindseliger wird und der Dialog zwischen Transplantat und Wirtszellen schwächer wird. Die Autoren schlagen vor, dass das Verstärken zentraler Faktoren wie MANF und die Verbesserung der Gesundheit der Wirtsnetzhaut — möglicherweise durch gentechnische Modifikation des Transplantats oder kombinierte Behandlungen — entscheidend sein könnten, um eine vorübergehende Atempause in eine langanhaltende Erhaltung des Sehens zu verwandeln.
Zitation: Shahin, S., Bell, S., Lu, B. et al. Dynamic transcriptomic remodeling in grafted human neural progenitor cells uncovers mechanisms for vision preservation in a rat model of retinitis pigmentosa. Nat Commun 17, 2164 (2026). https://doi.org/10.1038/s41467-026-69776-4
Schlüsselwörter: retinitis pigmentosa, Stammzelltherapie, Retinadeneration, Neuroprotektion, Einzelzell-RNA-Sequenzierung