Clear Sky Science · de
TCL1A vermittelt DNA‑Methylierungsfehler bei wiederkehrendem Hydatidiformmole mit pathogenen Varianten in NLRP7
Warum das für die Frauengesundheit wichtig ist
Manche Schwangerschaften scheitern sehr früh und verwandeln sich in eine Masse abnormalen Plazentagewebes statt in einen sich entwickelnden Fötus. Dieser Zustand, Hydatidiformmole genannt, kann bei einigen Frauen wiederkehren und in manchen Fällen in Krebs übergehen. Die Studie untersucht eine der Hauptursachen für diese seltenen, aber schweren Schwangerschaften und zeigt, wie ein einziger defekter Schutzmechanismus in der Eizelle die chemischen „Markierungen“ entgleisen lässt, die eine gesunde Entwicklung steuern.
Ein schwangerschaftsbedingtes Problem mit Ursprung in der Eizelle
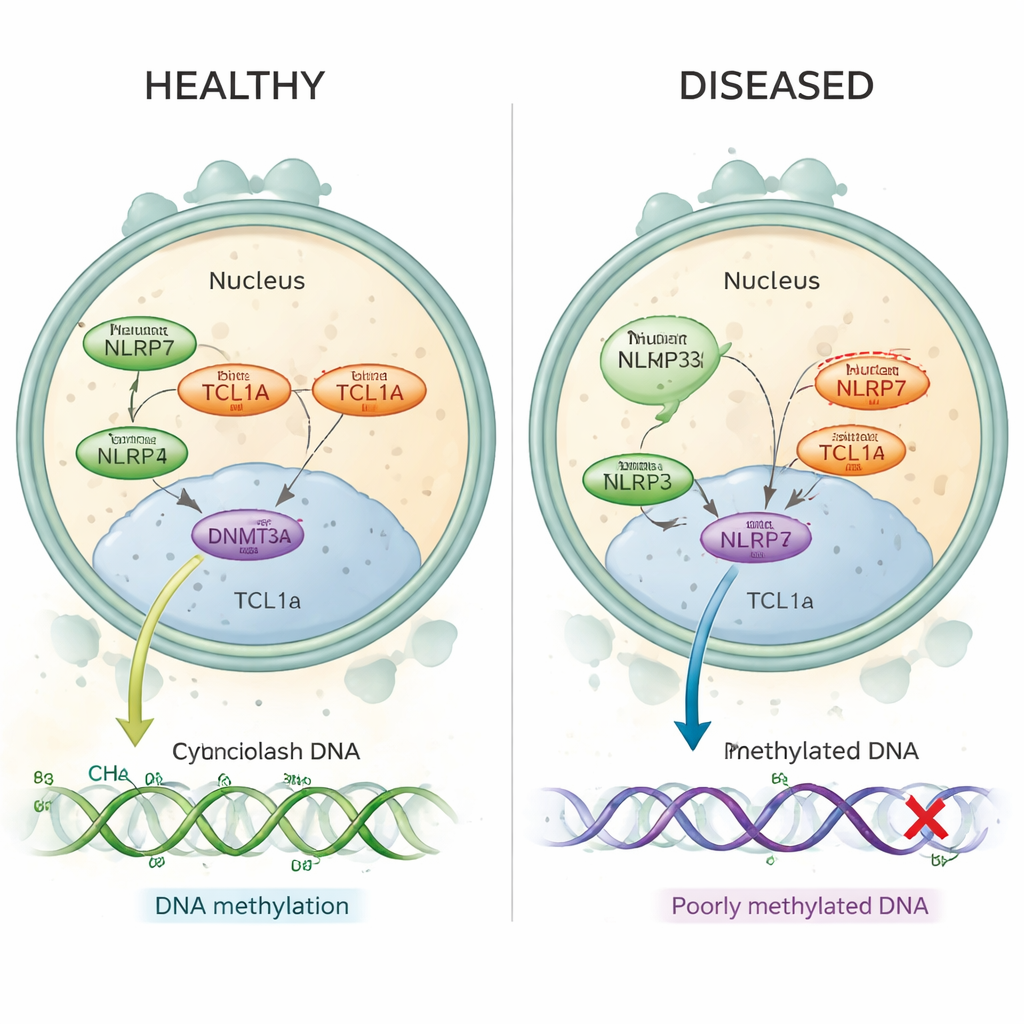
Das wiederkehrende Hydatidiformmole ist eine Erkrankung, bei der Frauen wiederholt Molenschwangerschaften erleben, häufig ohne dazwischenliegende normale Schwangerschaften. Viele dieser Fälle werden inzwischen auf schädliche Veränderungen in einem Gen namens NLRP7 zurückgeführt, das in der Eizelle vor und kurz nach der Befruchtung aktiv ist. Bei betroffenen Frauen fehlen an wichtigen DNA‑Abschnitten, die mütterliche „Imprints“ tragen sollten, die normalen Methylierungsmarken — kleine chemische Etiketten, die Gene zur richtigen Zeit an- oder ausschalten helfen. Bislang war unklar, wie ein Protein, das im Zytoplasma der Eizelle sitzt, wie NLRP7, die Methylierung kontrollieren kann, die auf der im Zellkern verpackten DNA stattfindet.
Auf der Spur eines fehlenden Partners
Um dieses Rätsel zu lösen, untersuchten die Forschenden verworfene menschliche Eizellen und sehr frühe Embryonen aus Kinderwunschkliniken. Sie isolierten NLRP7 und bekannte Partnerproteine aus diesen Zellen und identifizierten weitere Proteine, die mitkommen. Ein Protein stach heraus: TCL1A, bereits aus Blutkrebserkrankungen bekannt als ein Protein, das in den Zellkern gelangen und DNA‑Methylierungsenzyme namens DNMT3A und DNMT3B stören kann. TCL1A ist in menschlichen Eizellen ungewöhnlich reichlich vorhanden, was auf eine wichtige Rolle dort hindeutet. Detaillierte Wechselwirkungstests zeigten, dass TCL1A fest und spezifisch an NLRP7 bindet, nicht aber an eng verwandte Proteine, und dass dieser Komplex in eine größere eizell‑spezifische Struktur eingebunden ist, das subkortikale maternale Komplex.
Die molekulare Umarmung sehen
Das Team nutzte dann Kryo‑Elektronenmikroskopie, um die dreidimensionale Struktur des NLRP7–TCL1A‑Komplexes zu visualisieren. Sie fanden, dass sich zwei NLRP7‑Moleküle paaren und jedes ein TCL1A‑Dimer entlang einer gebogenen Oberfläche wiederholter Motive umfasst. Diese Anordnung erklärt, warum viele krankheitsverursachende Veränderungen in NLRP7 entlang jener Oberfläche gehäuft auftreten: Veränderungen an wichtigen Kontaktstellen schwächen oder zerstören die Bindung an TCL1A. Als die Forschenden mehr als 50 bekannte Patientenvarianten in Zellen rekonstruierten, destabilisierten die meisten der mit wiederkehrenden Molenschwangerschaften verbundenen Varianten entweder NLRP7 oder verringerten deutlich seine Fähigkeit, an TCL1A zu binden.
Wie fehlplatzierte Proteine DNA‑Marken stören
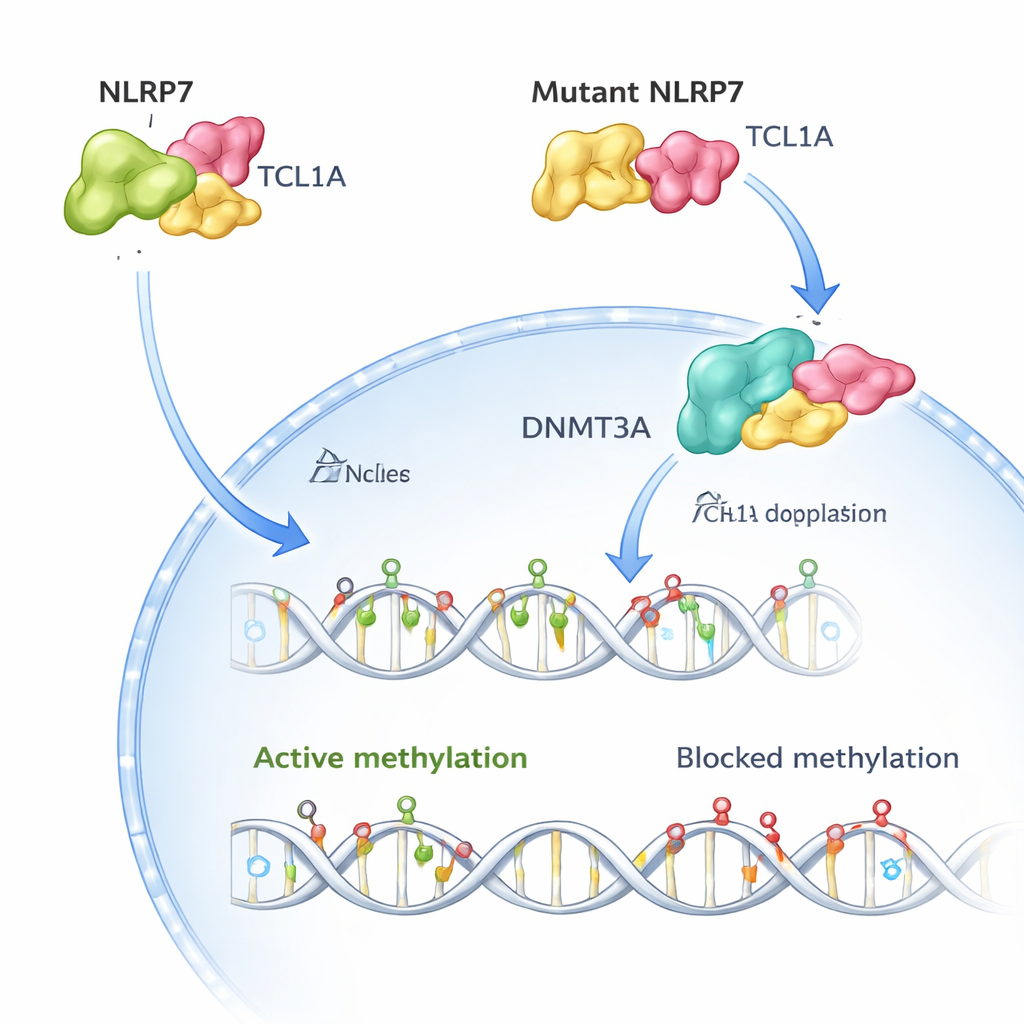
In gesunden menschlichen Eizellen finden sich sowohl NLRP7 als auch TCL1A überwiegend im Zytoplasma, wobei nur eine kleine Menge TCL1A in den Zellkern gelangt. Die Autorinnen und Autoren zeigen, dass NLRP7 effektiv als Türsteher fungiert: Wenn es TCL1A halten kann, bleibt TCL1A außerhalb des Zellkerns. Kann NLRP7 aufgrund einer Mutation nicht mehr gut binden, gelangt TCL1A in den Zellkern. Dort bindet es an DNMT3A, das Hauptenzym, das in Eizellen neue Methylierungsmarken setzt, und dämpft dessen Aktivität. In Stammzellmodellen, die normalerweise beim Reifen Methylierung gewinnen, führte Überproduktion von TCL1A zu einem dramatischen Verlust von Methylierungen im gesamten Genom, während gleichzeitige Expression von NLRP7 diesen Defekt teilweise ausglich. Zusammengenommen stützen diese Befunde ein einfaches Bild: Normales NLRP7 hält die Methylierungs‑„Bremse“ (TCL1A) im Zytoplasma verschlossen, damit DNMT3A die DNA korrekt markieren kann; defektes NLRP7 lässt diese Bremse in den Zellkern rutschen und blockiert so den Prozess.
Vom Mechanismus zur Diagnose
Über die Erklärung, wie wiederkehrende Molenschwangerschaften entstehen, hinaus schlägt die Studie einen praktischen Weg vor, um zu beurteilen, ob eine neu entdeckte NLRP7‑Veränderung bei einer Patientin tatsächlich schädlich ist. Die Autorinnen und Autoren vergleichen drei Ansätze — Labortests zur NLRP7–TCL1A‑Bindung, computerbasierte Vorhersagen und Standard‑Genetikbewertungen — und zeigen, dass der Verlust der TCL1A‑Bindung eng mit Varianten korreliert, die Krankheit verursachen. Sie entdecken zudem eine zuvor unerkannte schädliche Variante, L766R, in Familien mit wiederkehrenden Molen und bestätigen, dass diese sowohl das Protein schwächt als auch TCL1A in den Zellkern fehlleitet.
Was das einfach gesagt bedeutet
Diese Arbeit legt eine molekulare Kettenreaktion offen, die hinter einer seltenen, aber verheerenden Schwangerschaftserkrankung steht. Im Kern tragen die Eizellen betroffener Frauen ein defektes „Bodyguard“-Protein, NLRP7, das seinen Partner TCL1A nicht außerhalb des Zellkerns halten kann. Einmal im Kern, stört TCL1A das Enzym, das lebenswichtige chemische Markierungen auf der DNA anbringt. Fehlen diese Markierungen, wächst die frühe Plazenta abnormal und ein Embryo kann nicht entstehen. Indem die Studie diesen Weg Schritt für Schritt nachzeichnet, klärt sie, warum bestimmte genetische Veränderungen in Müttern Schwangerschaften wiederholt sabotieren können, und weist den Weg zu präziserer genetischer Beratung und Diagnostik für Frauen mit wiederkehrenden Hydatidiformmolen.
Zitation: Gao, Z., Liu, Q., Li, L. et al. TCL1A mediates DNA methylation defects in recurrent hydatidiform mole with NLRP7 pathogenic variants. Nat Commun 17, 2160 (2026). https://doi.org/10.1038/s41467-026-69744-y
Schlüsselwörter: DNA‑Methylierung, wiederkehrendes Hydatidiformmole, NLRP7, TCL1A, genomisches Imprinting