Clear Sky Science · de
Kontrolle ohne Chelatbildung bei Allylierungen von α‑oxy‑Ketonen mit Gruppe‑14‑Allylatranen
Molekulare Formen mit größerer Präzision aufbauen
Viele Medikamente und Naturstoffe wirken nur, wenn ihre Atome in genau der richtigen dreidimensionalen Anordnung vorliegen. Chemiker investieren deshalb enorme Anstrengungen, um zu steuern, wie neue Bausteine von einer Seite oder der anderen an ein Molekül „angedrückt“ werden. Dieser Artikel beschreibt einen neuen Weg, Allylgruppen — kurze Dreikohlenstoff‑Ketten — an eine häufige Molekülklasse anzufügen und so Zugang zu spiegelbildlichen Strukturen zu schaffen, die bisher nur schwer herstellbar waren.
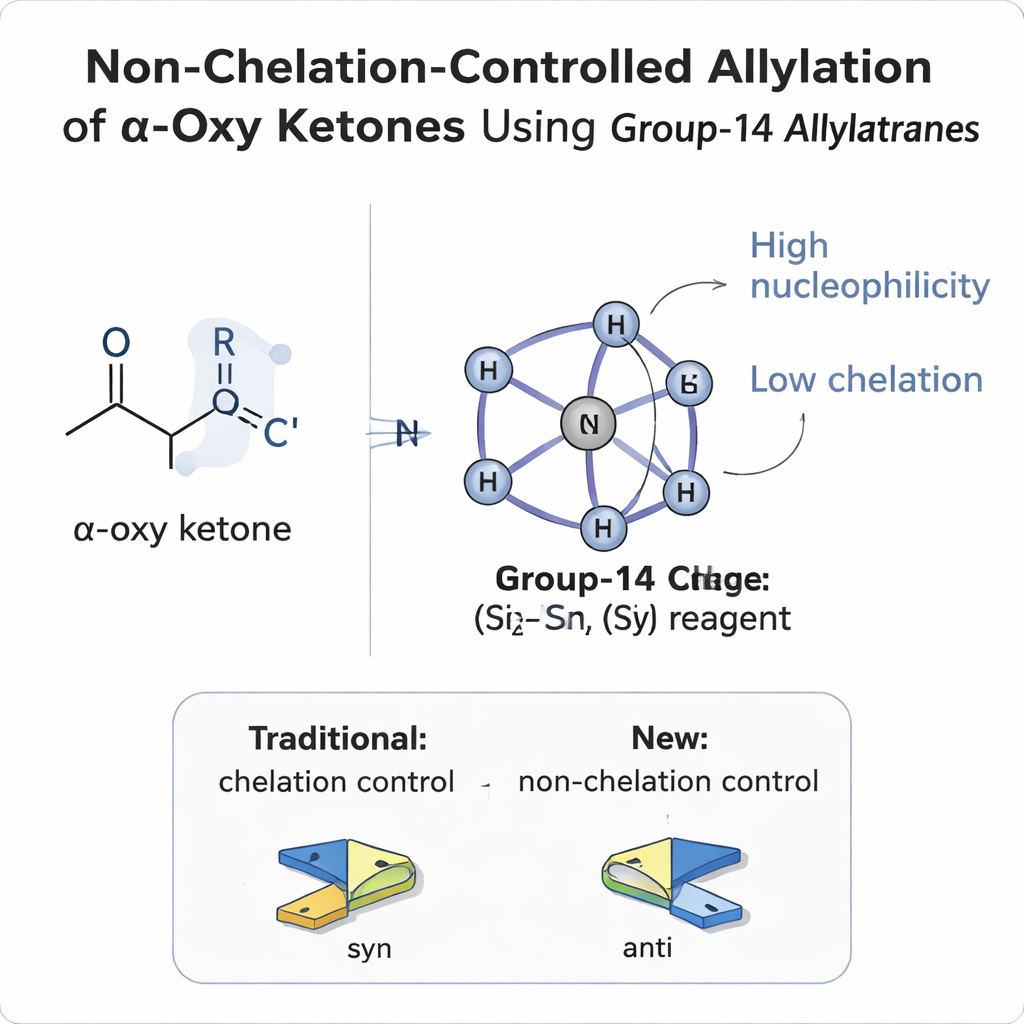
Warum es so schwer ist, die Angriffsseite eines Moleküls zu kontrollieren
Wenn eine neue Gruppe an eine flache, planare Kohlenstoff‑Sauerstoff‑Doppelbindung (ein Carbonyl) addiert wird, kann sie von beiden Seiten angreifen, wie ein Ball, der eine Münze von oben oder unten trifft. Sitzt am benachbarten Kohlenstoff (der α‑Position) bereits ein Substituent, entstehen zwei mögliche dreidimensionale Produkte, sogenannte Diastereomere. Jahrzehntelang stützten sich Chemiker auf einfache Modelle — Felkin–Anh, polar Felkin–Anh, Cram und Chelationsmodelle — um vorherzusagen, welche Seite ein Reagens bevorzugt. In α‑oxy‑Carbonylverbindungen, bei denen der benachbarte Substituent eine sauerstoffhaltige Gruppe (etwa Ether oder Ester) ist, wirkt das Sauerstoffatom häufig wie eine Kralle, die an Metallreagenzien bindet. Diese „Chelation“ fixiert das Molekül in einer Konformation und führt fast immer zu sogenannten syn‑Produkten, bei denen die neu gebildeten Alkoholgruppen auf derselben Seite der Kohlenstoffkette liegen.
Das seit Langem bestehende Problem mit sauerstoffhaltigen Nachbarn
Während der Chelationsweg sehr nützlich ist, ist er auch einschränkend: Er begünstigt stark syn‑Produkte und erschwert das Erreichen der entgegengesetzten anti‑Anordnung, bei der die beiden Alkoholgruppen auf gegenüberliegenden Seiten zeigen. Bei α‑oxy‑Aldehyden — Molekülen, deren Carbonylkohlenstoff mindestens ein Wasserstoffatom trägt — haben einige clevere Tricks mit speziellen Siliciumreagenzien und sorgfältig gewählten Lewis‑Säuren anti‑Produkte erzielt. Bei α‑oxy‑Ketonen, die weniger reaktiv und in komplexen Zielstrukturen häufiger vorkommen, ist die Herausforderung jedoch größer. Stärkere Nukleophile sind tendenziell Lewis‑saurer, was genau die Chelation fördert, die man vermeiden möchte. Die Balance zwischen „reaktiv genug“ und „nicht zu stark bindend“ gegenüber Sauerstoff war deshalb ein zentrales ungelöstes Problem.
Ein käfigartiges Reagenz, das die Regel bricht
Die Autoren stellen eine neue Reagenzfamilie vor, die Allylatrane heißt und auf Gruppe‑14‑Elementen — Silicium, Germanium und Zinn — in einem starren, käfigartigen Rahmen basiert. In diesen Molekülen reicht ein internes Stickstoffatom über den Käfig, um an das zentrale Atom zu binden und so ein hochkoordiniertes, nahezu einkapseltes Zentrum zu bilden. Dieses Design hat zwei entscheidende Effekte. Erstens erhöht es die Nukleophilie der gebundenen Allylgruppe, so dass diese bereitwillig eine neue Kohlenstoff‑Kohlenstoff‑Bindung eingeht. Zweitens zügelt es die Lewis‑Azidität des zentralen Atoms, so dass dieses deutlich weniger geneigt ist, stark an die Sauerstoffatome des Substrats zu binden. Quantenchemische Rechnungen und Kernspinresonanzdaten bestätigen, dass Ladung auf dem Allylfragment lokalisiert ist, während die elektronische Kommunikation mit dem Siliciumzentrum reduziert ist — das erklärt, wie das Reagenz zugleich kräftig und doch unwillig zu chelatieren sein kann.
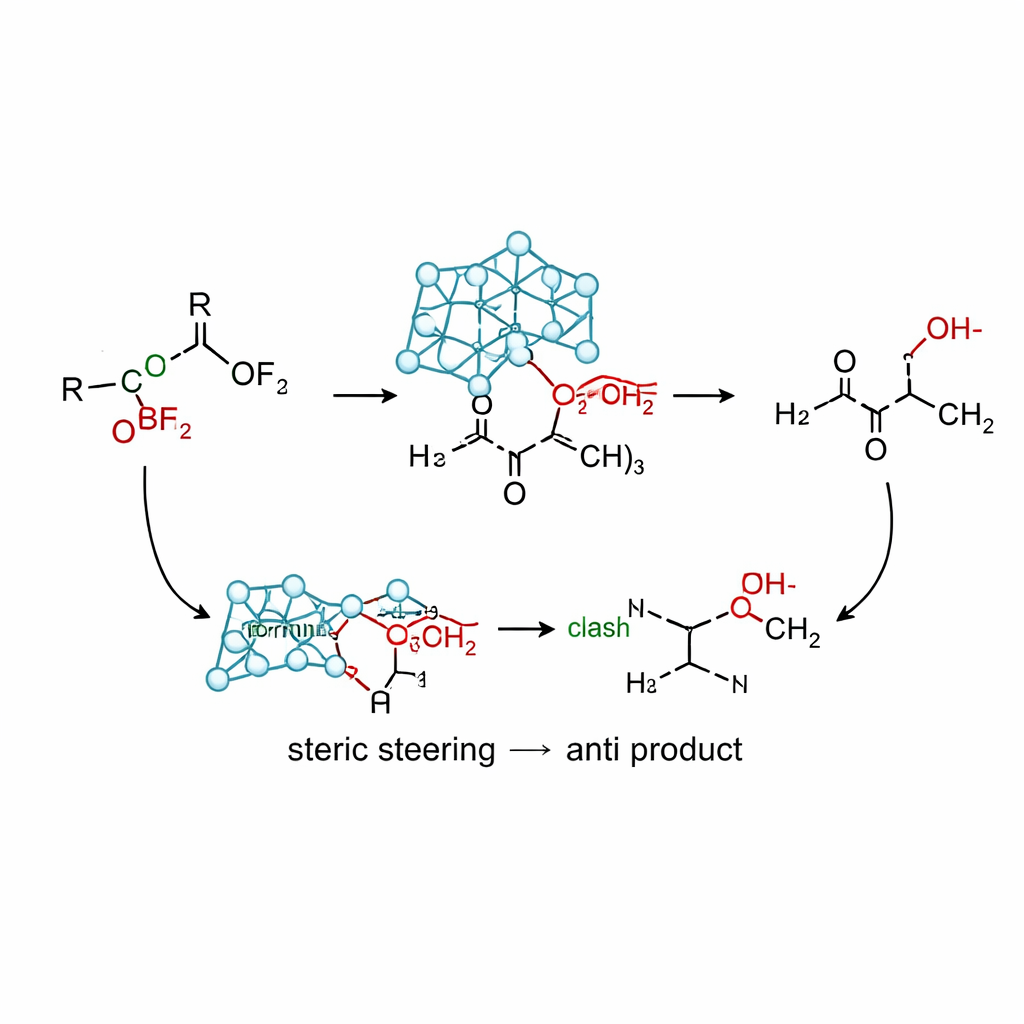
Wie die neue Reaktion praktisch funktioniert
Mit der Siliciumvariante dieses Reagenzes, Allylsilatrane, zusammen mit einer milden Lewis‑Säure (Bortrifluorid) entwickelten die Forscher Bedingungen, die hohe Ausbeuten an anti‑Homoallylalkoholen aus einer breiten Palette von α‑oxy‑Ketonen liefern. Vergleichsexperimente zeigen, dass viele traditionelle Allylquellen — auf Basis von Zinn, Indium, Magnesium, Lithium und einfachen Silanen — entweder das syn‑Produkt bevorzugen, Mischungen liefern oder zersetzen. Im Gegensatz dazu liefert Allylsilatrane routinemäßig anti/syn‑Verhältnisse über 95:5 bei Substraten mit Methoxy‑, Isopropoxy‑, Phenoxy‑, Acetoxy‑, Silyloxy‑ und Aminoxy‑Gruppen sowie verschiedenen aromatischen Ringen und cyclischen Ketonen. Rechnungen legen einen nicht‑chelatisierenden Mechanismus nahe, bei dem der voluminöse Atrane‑Rahmen die Annäherung der Allylgruppe in eine Konformation lenkt, die einem Cram‑Modell ähnelt: die Sauerstoffsubstituenten liegen gegenüber dem Carbonyl, während sterische Abstoßung zwischen dem Käfig und benachbarten Phenylringen die Bahn begünstigt, die zum anti‑Produkt führt.
Folgen für die Synthese von Wirkstoffen und Naturstoffen
Die Methode funktioniert auch bei starreren cyclischen Systemen, wo die Masse des Allylsilatrans den Angriff von weniger gehinderten Positionen fördert, und bei spezialisierten Derivaten, die substituierte Allylgruppen mit ähnlich hoher anti‑Selektivität übertragen. Da die resultierenden anti‑1,2‑Diolen mit einem Homoallylfragment häufige Motive in biologisch aktiven Molekülen sind — darunter Kandidaten für Enzymmodulatoren — bietet diese Transformation Chemikern einen verlässlichen Zugang zu Strukturvarianten, die zuvor mehrstufige Umwege erforderten oder schlicht unpraktisch waren. Wichtig ist, dass dieselben Substrate durch Umschalten zwischen einem chelatierenden Zinnsystem und dem neuen nicht‑chelatierenden Silatrane‑System entweder in syn‑ oder anti‑Produkte überführt werden können, wodurch sich die molekulare Gestalt präzise steuern lässt.
Was das einfach gesagt bedeutet
Im Kern haben die Forscher ein intelligentes Werkzeug zur Allyl‑Übertragung entwickelt, das das Zielkohlenstoffatom von der „unbevorzugten“ Seite trifft, ohne von benachbarten Sauerstoffatomen gefangen zu werden. Durch die gezielte Konstruktion eines Käfigs um Silicium entkoppelten sie Stärke und Haftung: Das Reagenz ist stark genug, um eine neue Bindung zu schmieden, aber nicht so „klebrig“, dass es umgebende Atome greift und die gewünschte Geometrie zerstört. Für Nichtfachleute bedeutet das: Chemiker haben jetzt ein wesentlich besseres Instrument, um dreidimensionale Molekülstrukturen zu formen, die vielen Medikamenten und Naturstoffen zugrunde liegen, und erweitern damit den Gestaltungsraum für künftige Wirkstoffe und komplexe synthetische Moleküle.
Zitation: Tsutsui, Y., Shiga, K., Konishi, A. et al. Non-chelation control in allylations of α-oxy ketones using group-14 allylatranes. Nat Commun 17, 2019 (2026). https://doi.org/10.1038/s41467-026-69732-2
Schlüsselwörter: stereoselektive Allylierung, alpha‑oxy‑Ketone, Allylsilatrane, Kontrolle ohne Chelatbildung, Homoallylalkohole