Clear Sky Science · de
Die N-Myc MB0–MBI-Region interagiert spezifisch und dynamisch mit der N-Lappen-Domäne der Aurora-Kinase A
Warum das für die Krebsbehandlung wichtig ist
Viele aggressive Kinderkrebserkrankungen sind auf ein Protein namens N-Myc angewiesen, damit Tumorzellen weiter proliferieren. N-Myc selbst ist schwer medikamentös zu blockieren, weil es sich eher wie ein flexibler Faden als wie ein starres Schloss verhält, in das ein Schlüssel passt. Diese Studie legt in bisher unerreichter Detailtiefe dar, wie N-Myc an ein anderes Protein – das Enzym Aurora-Kinase A (AurA) – bindet, um dessen Aktivität zu steigern und das Überleben von Krebszellen zu fördern. Durch die Kartierung dieser Partnerschaft zeigen die Forschenden einen realistischen Weg auf, sie mit kleinen Molekülen zu stören.
Ein flexibler Störenfried trifft auf einen festen Partner
N-Myc gehört zur MYC-Familie von Master-Schaltern, die Zellwachstum, Stoffwechsel und Teilung steuern. Wird es überproduziert, werden diese Schalter zu mächtigen Krebsantreibern, besonders in Tumoren des Nervensystems wie dem Hochrisiko-Neuroblastom bei Kindern. Anders als viele Enzyme oder Rezeptoren faltet sich N-Myc nicht zu einer festen 3D-Struktur; es ist ein „intrinsisch ungeordnetes“ Protein, das ständig zappelt und seine Form verändert. Diese Flexibilität macht es anpassungsfähig, aber auch berüchtigt schwer angreifbar mit Medikamenten. AurA dagegen ist ein gut geordnetes Enzym, das bei der Organisation der Zellteilung hilft. Früheren Arbeiten zufolge stabilisiert AurA N-Myc in Tumorzellen, und die beiden Proteine interagieren physisch, doch die genauen Kontaktstellen und ihre Bedeutung blieben unklar.
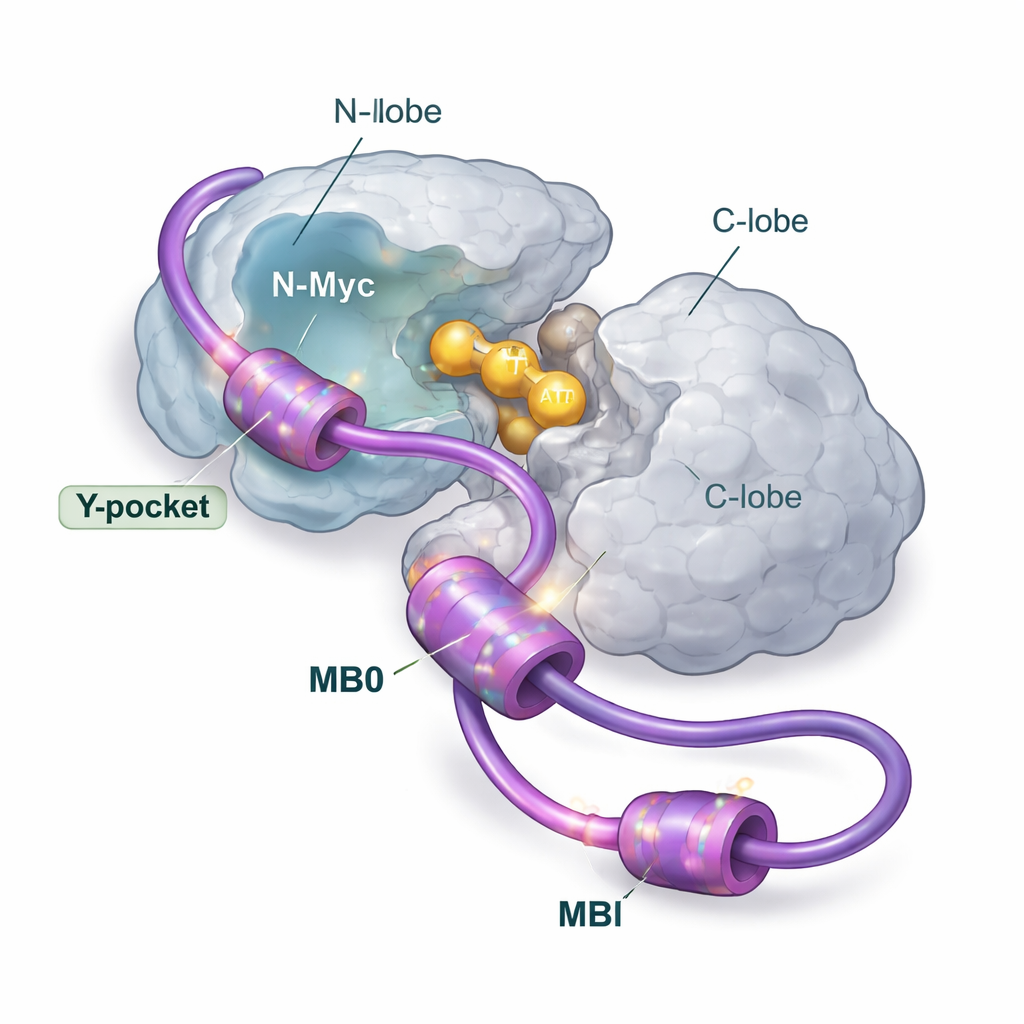
Mehrere Griffpunkte, ein primärer Landeplatz
Mithilfe eines breiten Instrumentariums struktureller und biophysikalischer Methoden – darunter Kernspinresonanz, Röntgenstreuung, Massenspektrometrie, Kalorimetrie und Computermodellierung – analysieren die Autorinnen und Autoren, wie N-Myc und AurA sich in Lösung zusammenfinden. Ihr Fokus lag auf dem Vorderende von N-Myc, das zwei konservierte Regionen namens MB0 und MBI enthält. Diese kurzen Segmente sind reich an aromatischen Bausteinen (wie Phenylalanin, Tyrosin und Tryptophan), die dazu neigen, an fettigen Taschen von Partnerproteinen haften zu bleiben. Das Team zeigt, dass N-Myc AurA überwiegend als 1:1-Komplex bindet, wobei MB0 und MBI die primären Kontaktzonen bilden. Ein weiterer N-Myc-Abschnitt, der in früheren Kristallstrukturen Aufmerksamkeit erregt hatte, spielt dagegen nur eine untergeordnete Rolle, wenn die volle MB0–MBI-Region vorhanden ist.
Ein dynamischer Händedruck, der das Enzym einschaltet
Anstatt sich in eine einzige starre Pose zu verkrampfen, bleibt N-Myc beim Binden an AurA weitgehend ungeordnet. Die Daten sprechen für einen „fuzzy“ (verschwommenen) Komplex: Mehrere N-Myc-Segmente wechseln sich ab und kontaktieren verschiedene Partien des AurA-N-Lappens, insbesondere eine Rinne, die als Y‑Pocket bekannt ist, und eine nahegelegene Schleife, die Signale zur aktiven Stelle verbindet. Trotz dieser Lockerheit ist der Effekt deutlich: Die Bindung von MB0 und MBI stabilisiert den AurA-N-Lappen und erhöht dessen Kinasetätigkeit, das heißt, er überträgt Phosphatgruppen effizienter auf seine Ziele. Als die Forschenden systematisch zentrale aromatische Reste in MB0 und MBI durch Alanin ersetzten, wurde der N-Myc–AurA-Komplex schwächer, das Enzym weniger stabilisiert und seine Aktivität verringerte sich. Das zeigt, dass spezifische aromatische „Anker“ in der ansonsten flexiblen N-Myc-Kette entscheidend dafür sind, AurA zu aktivieren.
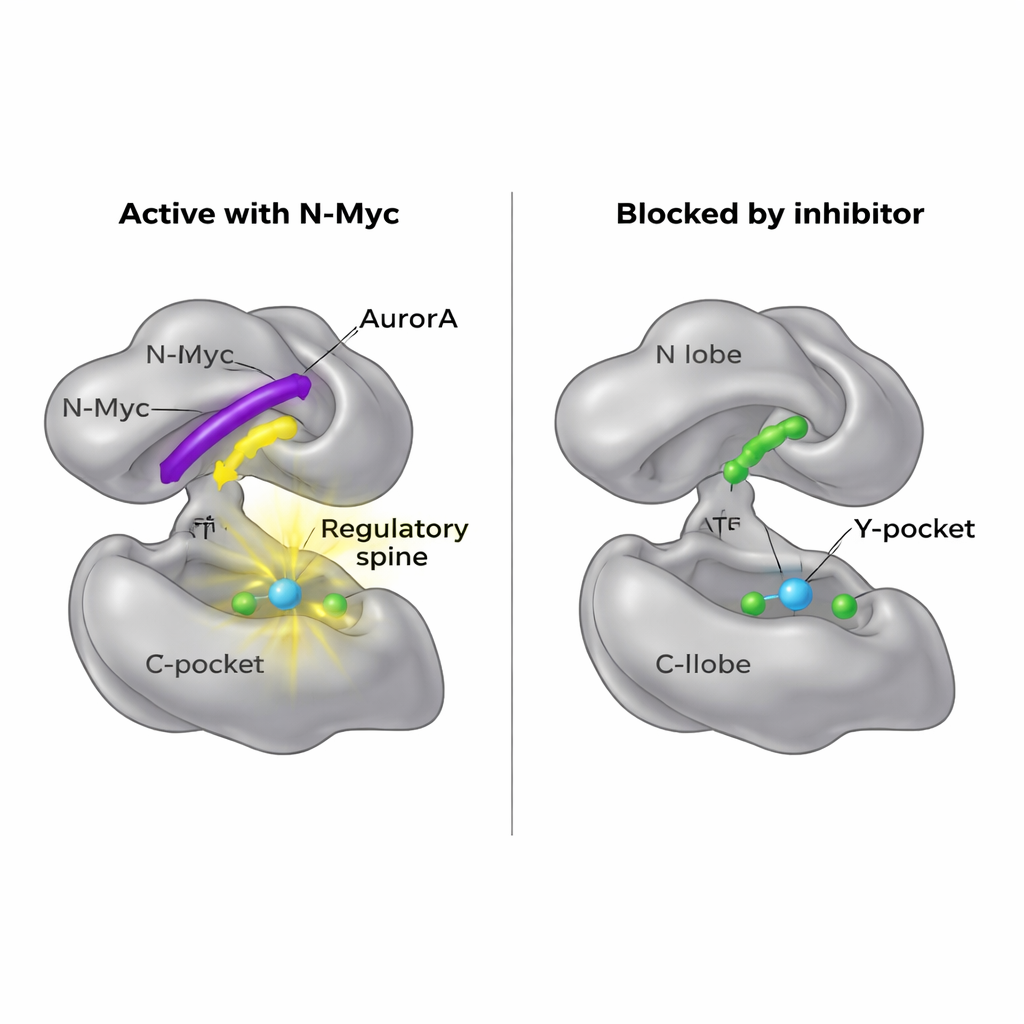
Ein neuer Angriffspunkt für Medikamente
Weil N-Myc selbst schwer zu therapieren ist, fragten die Forschenden, ob man stattdessen seine Andockstelle auf AurA blockieren könnte. Ihre Strukturkarten zeigten, dass MB0 und MBI denselben allgemeinen Bereich des N-Lappens belegen, den auch ein anderer Partner, TPX2, zur Aktivierung von AurA nutzt. Ein kleines Molekül namens AurkinA ist bereits dafür bekannt, sich in das Y‑Pocket zu schieben und TPX2 zu verdrängen. In Bindungsexperimenten konkurrierte AurkinA effektiv auch mit N-Myc um den AurA-N-Lappen und verhinderte sowohl das Andocken von N-Myc1–69 als auch von N-Myc1–100-Fragmenten. Dieses Ergebnis demonstriert, dass die N-Lappen-Oberfläche, insbesondere das Y‑Pocket, ein drugbares Hotspot ist, das nicht nur klassische Regulatoren wie TPX2, sondern auch ungeordnete Onkoproteine wie N-Myc kontrolliert.
Was das für künftige Therapien bedeutet
Diese Arbeit stellt die N-Myc–AurA-Partnerschaft als eine dynamische, multi-kontaktierte Umarmung in den Mittelpunkt, die auf dem AurA-N-Lappen zentriert ist, anstatt als eine einzige starre Bindestelle. Für Nicht-Fachleute lautet die Kernbotschaft: Selbst ein gestaltloses Krebsprotein wie N-Myc lässt sich indirekt angreifen, indem man ein festes Andockfeld auf seinem Partnerenzym adressiert. Indem die Studie zeigt, dass bereits vorhandene N-Lappen-bindende Verbindungen N-Myc von AurA verdrängen können, eröffnet sie einen klaren Pfad zu Wirkstoffen, die diese Interaktion selektiv stören. Solche Agenzien könnten eine kritische Stütze für N-Myc in Hochrisiko-Kindertumoren schwächen und mit weiterer Entwicklung eine neue Behandlungsoption für lange als „nicht angreifbar“ geltende Krebserkrankungen bieten.
Zitation: Hultman, J., Morad, V., Tanner, E. et al. The N-Myc MB0-MBI region interacts specifically and dynamically with the N-lobe of Aurora kinase A. Nat Commun 17, 2016 (2026). https://doi.org/10.1038/s41467-026-69725-1
Schlüsselwörter: N-Myc, Aurora-Kinase A, intrinsisch ungeordnete Proteine, Neuroblastom, Protein‑Protein-Interaktionsinhibitoren