Clear Sky Science · de
Spatial Perturb-seq: Einzelzell-Funktionsgenomik innerhalb intakter Gewebearchitektur
Gene in lebenden Hirnschaltkreisen beobachten
Viele Hirnerkrankungen, von Alzheimer bis Parkinson, sind mit Risikogenen verbunden, doch wir wissen noch wenig darüber, wie diese Gene einzelne Zellen im lebenden Gehirn beeinflussen. Diese Studie stellt eine leistungsfähige Methode vor, um zu verfolgen, was passiert, wenn bestimmte Gene in Einzelzellen ausgeschaltet werden, während diese Zellen in ihren natürlichen Nachbarschaften im Gewebe verbleiben. Der Ansatz, Spatial Perturb-Seq genannt, hilft, genetisches Risiko mit gestörtem Zellverhalten und Zell-zu-Zell-Kommunikation im intakten Gehirn zu verknüpfen.
Eine neue Möglichkeit, viele Gene gleichzeitig zu testen
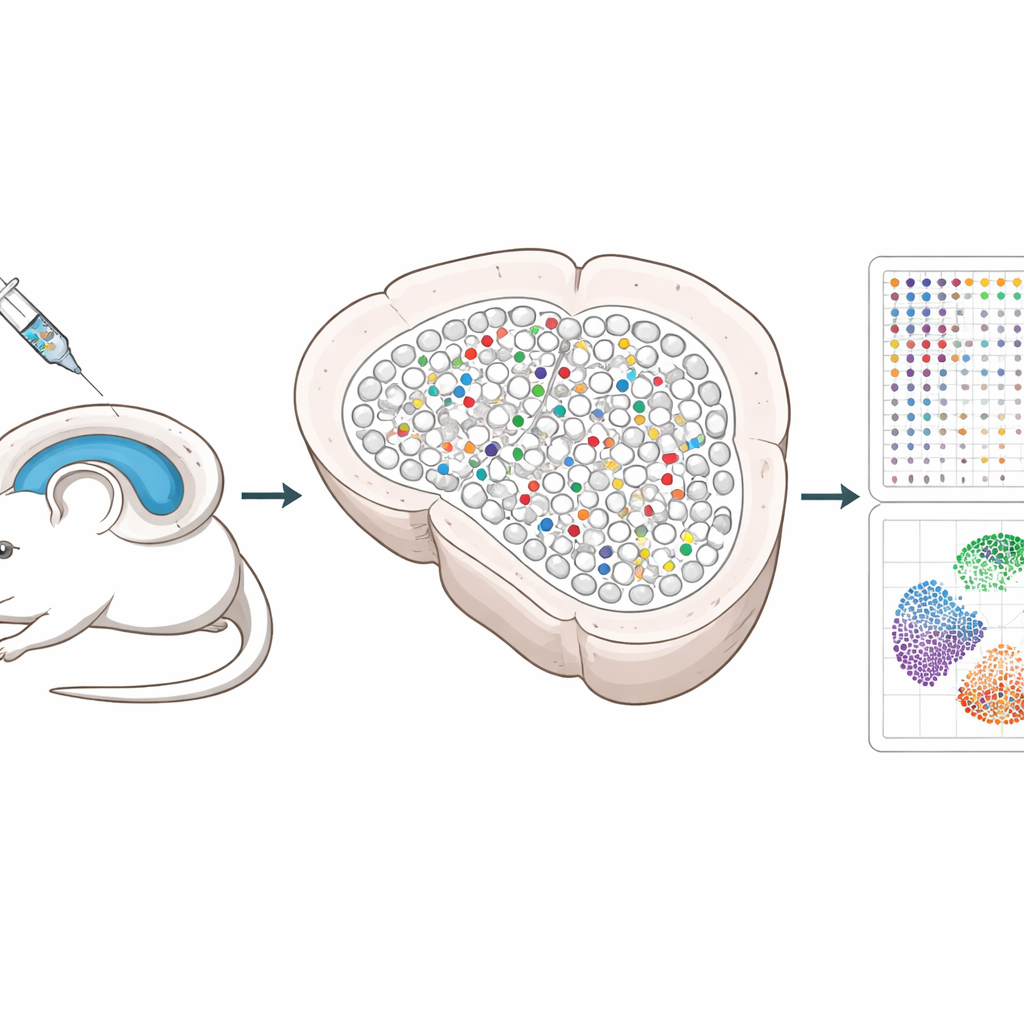
Die Forschenden entwickelten ein System, das CRISPR-Geneditierwerkzeuge mit harmlosen Viren in den Hippocampus einbringt, einen für das Gedächtnis wichtigen Gehirnbereich. Jeder Virusträger enthält drei Guides, die ein ausgewähltes Gen ausschalten, sowie einen einzigartigen DNA-„Barcode“ und einen fluoreszierenden Marker, damit editierte Zellen später gefunden werden können. Durch das Mischen dieser Viren und die Injektion in niedriger Dosis werden nur wenige, verstreute Zellen editiert, während die meisten Nachbarn unberührt bleiben. Dieses spärliche Muster erlaubt es den Wissenschaftlern, Veränderungen in editierten Zellen von denen in benachbarten gesunden Zellen zu trennen.
Die Karten des Gehirns intakt bewahren
Traditionelle Einzelzellmethoden erfordern das Auseinanderbrechen von Gewebe, wodurch die genauen Positionen der Zellen verloren gehen und empfindliche Neuronen unter Umständen verloren gehen. Spatial Perturb-Seq liest stattdessen die Genaktivität direkt aus dünnen Hirnschnitten aus, sodass der Ort jeder Zelle erhalten bleibt. Mit einer Technologie namens Stereo-seq erfasste das Team vollständige Genexpressionsprofile von mehr als 200.000 Zellen, während gleichzeitig die CRISPR-Barcodes ausgelesen und die Koordinaten jeder Zelle im Gewebe aufgezeichnet wurden. Anschließend nutzten sie fortgeschrittene bildbasierte Algorithmen, um jede Zelle zu umranden, sowie rechnerische Werkzeuge, um Zelltypen und lokale Nachbarschaften zu identifizieren, mit besonderem Fokus auf hippocampale Neuronen und ihre engen Kontakte.
Wie editierte Zellen ihre Nachbarn beeinflussen
Mit der Gewebekarte verglichen die Forschenden editierte Neuronen mit uneditierten Neuronen und getrennt davon mit den uneditierten Nachbarn um jede editierte Zelle. So konnten sie „zellautonome“ Effekte (innerhalb der editierten Zelle) von „nicht-zellautonomen“ Effekten (in der umgebenden Mikroumgebung) unterscheiden. Das Ausschalten von 18 verschiedenen Genen, von denen viele mit dem Risiko für neurodegenerative Erkrankungen verknüpft sind, erzeugte jeweils charakteristische Muster von Genänderungen in den editierten Neuronen. Manche Editierungen, etwa gegen das Gen Cfap410, lösten auch starke Verschiebungen der Genaktivität in benachbarten Zellen aus, was auf veränderte lokale Signalübertragung und Unterstützungsfunktionen hindeutet.
Hinweise auf Wege der Neurodegeneration
Mehrere Gene lieferten besonders aufschlussreiche Erkenntnisse. Das Deaktivieren von Lrrk2, einem wichtigen Parkinson-Risikogen, führte zu großen Veränderungen in den editierten Neuronen, einschließlich reduzierter Mengen an Bc1, einem RNA-Molekül, das wichtig für die Feinabstimmung der Proteinproduktion an Synapsen ist. Gleichzeitig zeigten benachbarte Zellen veränderte Expression von Genen, die an Synapsenstruktur, Proteintransport und Calcium‑Handling beteiligt sind, was nahelegt, dass Lrrk2‑bedingte Probleme sich durch lokale Schaltkreise ausbreiten. Das Ausschalten eines anderen Gens, Srf, störte ein Netzwerk von Genen, das mit neuronalem Wachstum und Plastizität verknüpft ist, und schwächte spezifische Ligand–Rezeptor‑Signalwege zwischen Neuronen, was auf gestörte Zell‑zu‑Zell‑Kommunikation hinweist. Durch systematische Bewertung dieser Signalpaare konnte das Team ermitteln, welche Kommunikationswege bei jedem Gen am stärksten betroffen waren.
Flexible Werkzeuge zur Kartierung genetischer Effekte
Um zu zeigen, dass Spatial Perturb-Seq nicht auf eine einzige Plattform beschränkt ist, passten die Forschenden die Methode auch an ein bildbasiertes System namens Xenium an. Dort lesen vorgefertigte Sondenpanels und kundenspezifische Barcode-Sonden ausgewählte Gene und Barcodes direkt im Gewebe aus. Obwohl dieser gezielte Ansatz weniger Gene abdeckt als das komplette Transkriptom von Stereo-seq, stimmten Muster der Genänderungen für Schlüsseltargets wie Lrrk2 und Srf gut zwischen den beiden Methoden und mit einem großen externen Gehirnatlas überein. Diese Gegenprüfung untermauert die Robustheit der beobachteten Gen- und Nachbarschaftseffekte.
Was das für die Forschung zur Gehirngesundheit bedeutet
Einfach gesagt erlaubt Spatial Perturb-Seq Wissenschaftlern, viele verschiedene Gene in einzelnen Gehirnzellen auszuschalten und dann zu beobachten, wie diese Zellen und ihre unmittelbaren Nachbarn reagieren — und das alles, während das Verschaltungsdiagramm des Gewebes erhalten bleibt. So lässt sich nachvollziehen, wie genetische Risikofaktoren nicht nur einzelne Zellen, sondern auch die Gespräche zwischen ihnen stören, die für eine gesunde Gehirnfunktion entscheidend sind. Mit der Zeit, wenn Sequenzierung günstiger wird und größere Experimente durchgeführt werden, könnte dieser Ansatz helfen, jene Gene und lokalen Schaltkreise zu identifizieren, die in frühen Stadien von Erkrankungen wie Alzheimer, Parkinson und ALS am wichtigsten sind, und so präzisere Behandlungsstrategien leiten.
Zitation: Shen, K., Seow, W.Y., Keng, C.T. et al. Spatial perturb-seq: single-cell functional genomics within intact tissue architecture. Nat Commun 17, 3018 (2026). https://doi.org/10.1038/s41467-026-69677-6
Schlüsselwörter: räumliche Genomik, CRISPR-Screens, Einzelzell-Sequenzierung, Neurodegeneration, Zell-Zell-Kommunikation