Clear Sky Science · de
FLEXTAG: ein kleines und selbsterneuerndes Protein-Markierungssystem für anti-bleichende Mehrfarben-Superauflösungs-Bildgebung
Das Unsichtbare im Inneren von Zellen sichtbar machen
Ein Großteil der modernen Biologie baut auf Bildern der Moleküle auf, die unsere Zellen am Leben erhalten. Doch selbst die besten Lichtmikroskope kämpfen mit einem einfachen Problem: Die leuchtenden Marker, mit denen Proteine hervorgehoben werden, verblassen schnell, und es ist schwierig, viele verschiedene Ziele gleichzeitig zu markieren, ohne die Zellfunktion zu stören. Dieser Artikel stellt FLEXTAG vor, eine neue Familie winziger, erneuerbarer Marker, die deutlich länger leuchten, Mehrfarben-Unterstützung bieten und mit den leistungsstärksten Mikroskopen kompatibel sind, die Forscher zur Untersuchung der inneren Zellarchitektur verwenden.
Warum schärfere Zellfotos so schwer zu erreichen sind
Konventionelle Fluoreszenzmikroskope zeigen Strukturen von etwa einem Viertel Mikrometer Größe, was immer noch deutlich größer ist als die meisten einzelnen Proteine. Superauflösungsverfahren drücken noch mehr Details heraus und erreichen Bereiche von wenigen Nanometern, allerdings nur, wenn sich die fluoreszenten Marker perfekt verhalten. Heute verbreitete Proteinmarker sind entweder sperrige Antikörper, schwache fluoreszente Proteine oder chemische Tags, deren Farbstoffe unter dem intensiven Licht dieser Techniken schnell ausbrennen. Das Fixieren von Zellen für detaillierte Bildgebung kann Proteine zudem so miteinander verbinden, dass Farbstoffe ihre Ziele nicht mehr erreichen, und freie Farbmoleküle können unspezifisch haften und das Bild mit Hintergrundleuchten verschleiern.
Eine neue Art nachfüllbarer Proteinmarker
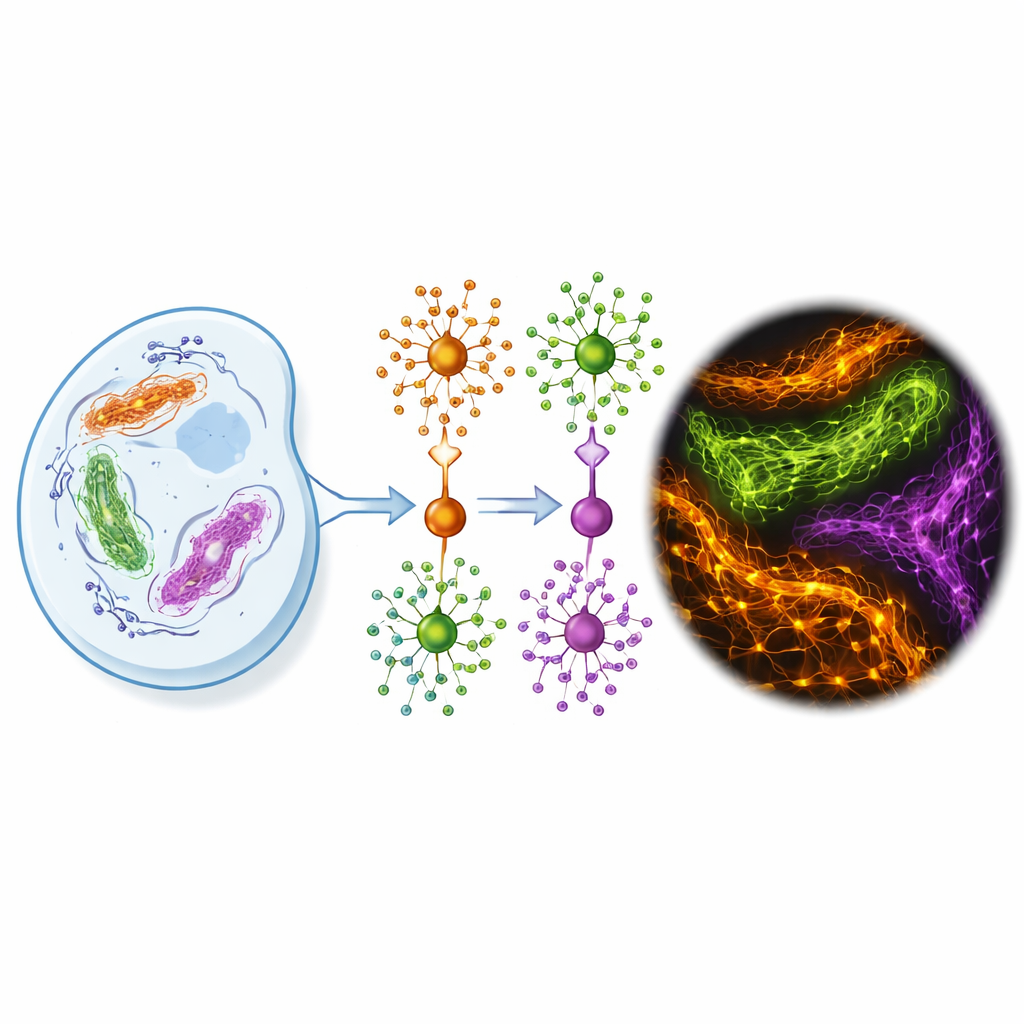
Die Autoren entwickelten FLEXTAG (Kurzform für Fluorescent Labeling for Exchangeable, X-resilient Tagging in Advanced Generic Nanoscopy), um diese Einschränkungen direkt anzugehen. FLEXTAG ist kein einzelner Marker, sondern ein koordiniertes Trio—FLEXTAG1, FLEXTAG2 und FLEXTAG3—jeweils ein kleines, konstruiertes Protein (12–18 Kilodalton, etwa halb so groß wie klassische Tags wie GFP und deutlich kleiner als HaloTag). Jeder FLEXTAG bindet ein passendes kleinmolekulares Ligand, das einen hellen organischen Farbstoff trägt. Entscheidend ist, dass diese Bindung reversibel ist: Farbstoff–Ligand-Moleküle kommen und gehen kontinuierlich. Wenn ein Fluorophor durch Licht geschädigt wird, ersetzt ein frisches aus der umgebenden Lösung es, sodass das Signal praktisch „selbsterneuernd“ ist, anstatt stetig zu verblassen.
Drei kompakte und zuverlässige Tags entwickeln
Um FLEXTAG1–3 zu schaffen, verwendete das Team drei bekannte Proteinskelette aus Zellbiologie und Wirkstoffdesign und nutzte strukturelles Modellieren sowie bildgebende Assays, um ihr Verhalten umzugestalten. FLEXTAG1 stammt von einer Bromodomänen-Protein, das ein modifiziertes kleines Molekül erkennt; die Autoren führten Mutationen ein, um die Neigung zur Dimerisierung und Klumpenbildung zu verringern, während die starke Ligandbindung erhalten blieb. FLEXTAG2 basiert auf bakterieller Dihydrofolatreduktase. Durch das Einfügen einer strategischen Disulfidbrücke und das Abstimmen flexibler Linker stabilisierten sie das Protein und erhöhten dramatisch, wie viele Tags zu jedem Zeitpunkt Farbstoff tragen, während die Bindung reversibel blieb. FLEXTAG3 beruht auf einem humanen FKBP-Protein, das in der chemischen Biologie genutzt wird; hier balancierte das Team Bindungsstärke und -geschwindigkeit so aus, dass Farbstoffe schnell genug abfallen, um ersetzt zu werden, aber dennoch stark genug binden, um helle Bilder zu liefern und übermäßige Aggregation zu vermeiden.
Tags beim Fixieren schützen und Hintergrundleuchten reduzieren
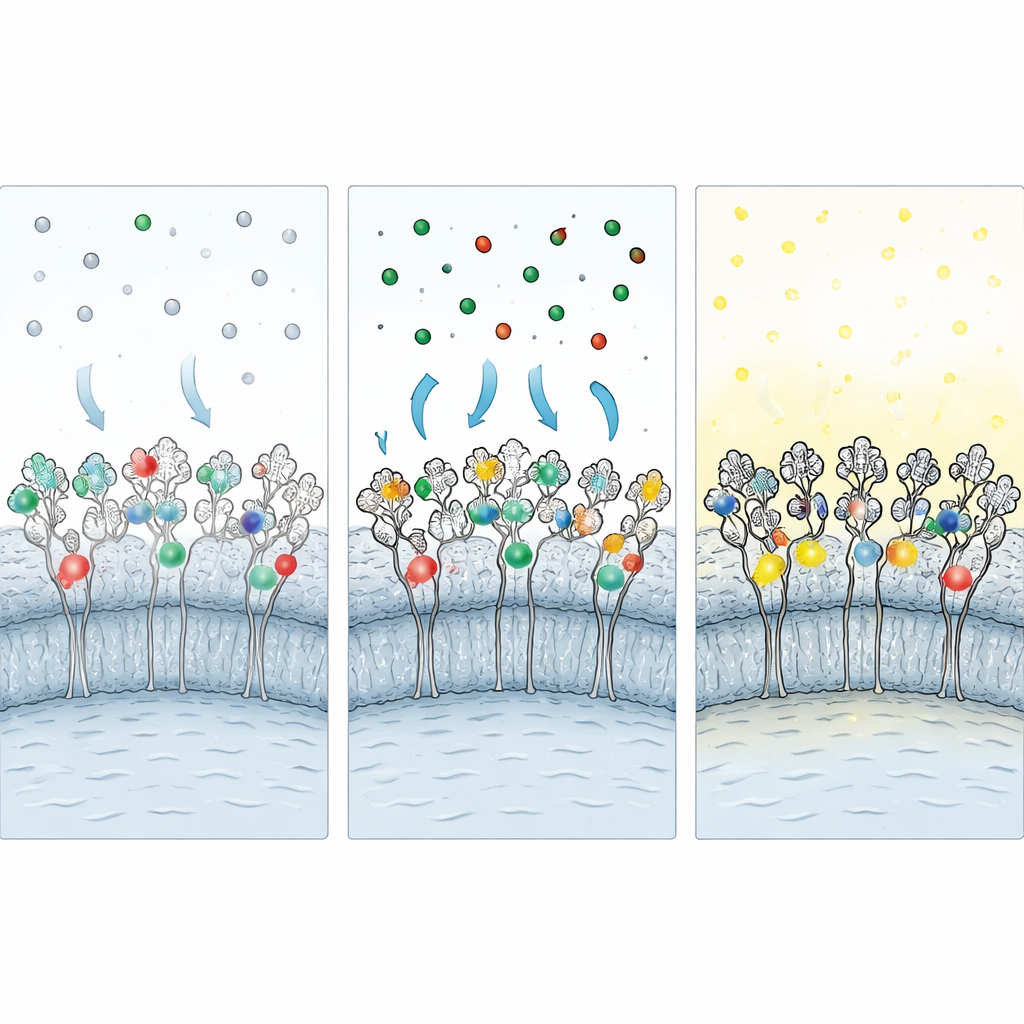
Da viele wichtige Experimente die Bildgebung fixierter Zellen erfordern, entwickelten die Forscher eine „schützende Fixierungs“-Strategie. Bevor aldehydische Fixativa zugegeben werden, durchfluten sie lebende Zellen mit unlabeled Versionen jedes Ligands, die die Bindetasche des Tags blockieren. Während der Fixierung schützen diese Schutzliganden empfindliche Aminosäuren vor chemischer Vernetzung. Nach der Fixierung werden die Schutzliganden ausgewaschen und durch fluoreszente Liganden ersetzt, wodurch der Zugang zum Tag wiederhergestellt wird. Zusätzliche Schritte—chemische Reduktion zur Neutralisierung verbleibender reaktiver Gruppen und eine Blockiermischung aus Albumin, Detergens und einem chaotropen Salz—verringern weiter das klebrige, unspezifische Binden freier Farbstoffe. Zusammen bewahren diese Maßnahmen etwa 60–70 % der Markierung, die in lebenden Zellen zu sehen ist, und verbessern gleichzeitig deutlich Signal-zu-Rausch-Verhältnis.
Schärfere, länger anhaltende Filme über viele Methoden hinweg
Mit dem FLEXTAG-Rahmenwerk prüften die Autoren dessen Leistungsfähigkeit in den wichtigen Familien der Superauflösungsmikroskopie. In Verfahren mit strukturierter Beleuchtung wie SIM und STED ermöglichten FLEXTAGs Mehrfarbenaufnahmen von Mitochondrien, Mikrotubuli, endoplasmatischem Retikulum und Aktin mit deutlich weniger Ausbleichen als gängige kovalente Tags; über Dutzende von Aufnahmezyklen halbierte sich das Signal konventioneller Tags oder mehr, während die FLEXTAG-Signale nahezu konstant blieben. In Ein-Molekül-Methoden wie PAINT und STORM erzeugte der schnelle On–Off-Austausch der FLEXTAG-Liganden reichhaltige, stabile Lokalisierungsströme, die in dreidimensionale, mehrfarbige Karten subzellulärer Strukturen umgewandelt werden konnten, sogar in lebenden Zellen über viele Minuten. FLEXTAG2 zeigte besonders günstige Kinetiken für PAINT, während FLEXTAG3 in langanhaltenden STORM-Filmen brillierte. Da die Tags zueinander orthogonal sind und mit einer breiten Palette von Farbstoffen kompatibel sind, können Wissenschaftler mehrere Proteine gleichzeitig markieren und dann den Bildgebungsmodus wählen, der für ihre Fragestellung am besten geeignet ist, ohne die zugrunde liegenden Konstrukte zu ändern.
Was das für den Blick ins Zellinnere bedeutet
FLEXTAG bietet eine Art universellen, nachfüllbaren Verbindungspunkt zwischen Proteinen und hellen Farbstoffen. Seine winzige Größe verringert das Risiko, dass der Tag die Lokalisation oder Funktion eines Proteins verzerrt, und seine selbsterneuernden Farbstoffe umgehen das langjährige Problem des Photobleachings bei leistungsstarken Mikroskopen. Indem diese Tags mit schützender Fixierung und Hintergrundunterdrückungschemie kombiniert werden, können Forschende sauberere, länger anhaltende und farbenreichere Einblicke in die Organisation und Bewegung von Proteinen in Zellen gewinnen. Praktisch bedeutet das bessere Karten der zellulären Architektur, zuverlässigeres Verfolgen molekularer Interaktionen über die Zeit und ein vielseitiges Werkzeugset, das sowohl der Grundlagenzellbiologie als auch translationalen Studien zugutekommen sollte, die auf die nanoskalige Beobachtung krankheitsbezogener Veränderungen angewiesen sind.
Zitation: Zhang, H., Yao, Y., Wang, X. et al. FLEXTAG: a small and self-renewable protein labeling system for anti-fading multi-color super-resolution imaging. Nat Commun 17, 2156 (2026). https://doi.org/10.1038/s41467-026-69658-9
Schlüsselwörter: Superauflösungsmikroskopie, fluoreszente Proteinmarkierung, Lebendzellbildgebung, Photobleichen-Resistenz, zelluläre Architektur