Clear Sky Science · de
Effiziente Umwandlung von Methanol zu Ethylenglykol und Glykolaldehyd durch divergente C−C-Kupplungssynthese
Aus einem einfachen Brennstoff nützliche Bausteine machen
Methanol, ein einfaches Alkohol, das aus Kohlendioxid, Erdgas, Kohle oder Biomasse hergestellt werden kann, ist bereits ein wichtiger Brennstoff und chemischer Rohstoff. Diese Studie zeigt, wie Lichtstrahlen und sorgfältig entworfene Nanomaterialien Methanol in komplexere, höherwertige Moleküle verwandeln können – während gleichzeitig Wasserstoffgas als sauberer Energieträger freigesetzt wird. Die Arbeit offenbart eine neue Methode, ein einzelnes Ausgangsmaterial in zwei unterschiedliche nützliche Produkte zu lenken, allein durch die Veränderung der Anordnung einzelner Metallatome auf einer winzigen Katalysatoroberfläche. 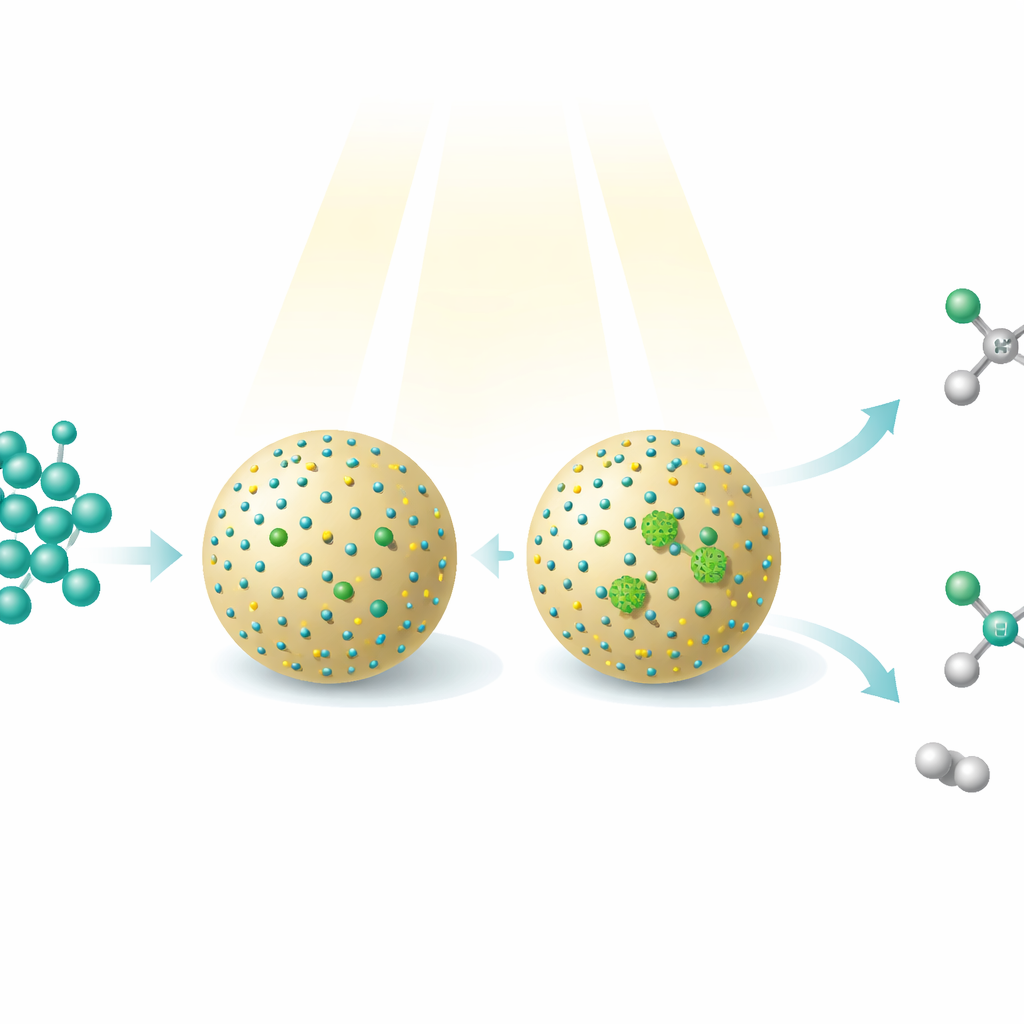
Warum die Aufwertung von Methanol wichtig ist
Da die Welt nach Alternativen zum Erdöl sucht, hat sich Methanol als attraktiver flüssiger Stoff erwiesen, der Energie und Kohlenstoff speichern kann. Die meisten industriellen Prozesse, die Methanol in größere Moleküle umwandeln, sind jedoch grobe Werkzeuge: Sie erfordern hohe Temperaturen, basieren oft auf fossilen Rohstoffen und erzeugen häufig viele unerwünschte Nebenprodukte. Chemiker möchten Methanolmoleküle präzise koppeln, um gezielt nur die gewünschten Verbindungen herzustellen. Wenn dies unter milden Bedingungen mit Licht statt Wärme gelingt, lässt sich die chemische Produktion leichter mit erneuerbarer Energie verknüpfen.
Lichtaktivierte Nanosphären leisten die Arbeit
Die Forschenden bauten einen Photokatalysator – wörtlich einen lichtgetriebenen Katalysator – indem sie winzige Cadmiumsulfid-Quantenpunkte auf kugelförmige Silica-Partikel aufbrachten. Diese Quantenpunkte absorbieren Licht und erzeugen energetische Elektronen und Löcher, die Wasserstoffatome aus Methanol herausreißen können und so hochreaktive Fragmente bilden. Anschließend wurden Nickelatome in zweierlei Ausführung auf den Quantenpunkten abgeschieden. In einem Material lagen die Nickel größtenteils als isolierte Einatome vor; im anderen bildeten sie sehr kleine Cluster aus mehreren Atomen. Obwohl die Gesamtzusammensetzung kaum verändert war, veränderte dieser subtile Unterschied in der Nickelanordnung dramatisch, welche Reaktionen an der Oberfläche abliefen.
Zwei Nickel-Designs, zwei saubere Produkte
Wenn der Katalysator mit einzelnen Nickelatomen im Methanol dem Licht ausgesetzt wurde, begünstigte er die Paarung zweier identischer Methanol-abgeleiteter Fragmente und führte hauptsächlich zu Ethylenglykol – einem zwei-Kohlenstoff-Diol, das vielfach in Frostschutzmitteln und Kunststoffen verwendet wird. Dieser Weg erreichte etwa 90 % Selektivität, das heißt fast das gesamte umgesetzte Methanol wurde zu diesem einen Produkt, während gleichzeitig Wasserstoffgas in entsprechenden Mengen aus den entfernten Wasserstoffatomen erzeugt wurde. Im Gegensatz dazu leitete der Katalysator mit Nickelclustern dieselben Methanolfragmente entlang eines anderen Pfades. Hier wurde ein Teil des Methanols weiter zu einem kurzlebigen formaldehydähnlichen Zwischenprodukt oxidiert, das dann mit einem anderen Fragment zu Glykolaldehyd reagierte, einer weiteren Zwei-Kohlenstoff-Verbindung mit zahlreichen Anwendungen in der Feinchemie und potenziell in biobasierten Prozessen. Dieser Weg lieferte Glykolaldehyd mit 96 % Selektivität, ebenfalls begleitet von Wasserstoff. Der Silica-Träger half den Quantenpunkten, Licht effizienter zu nutzen, und machte die Partikel über viele Nutzungszyklen robuster. 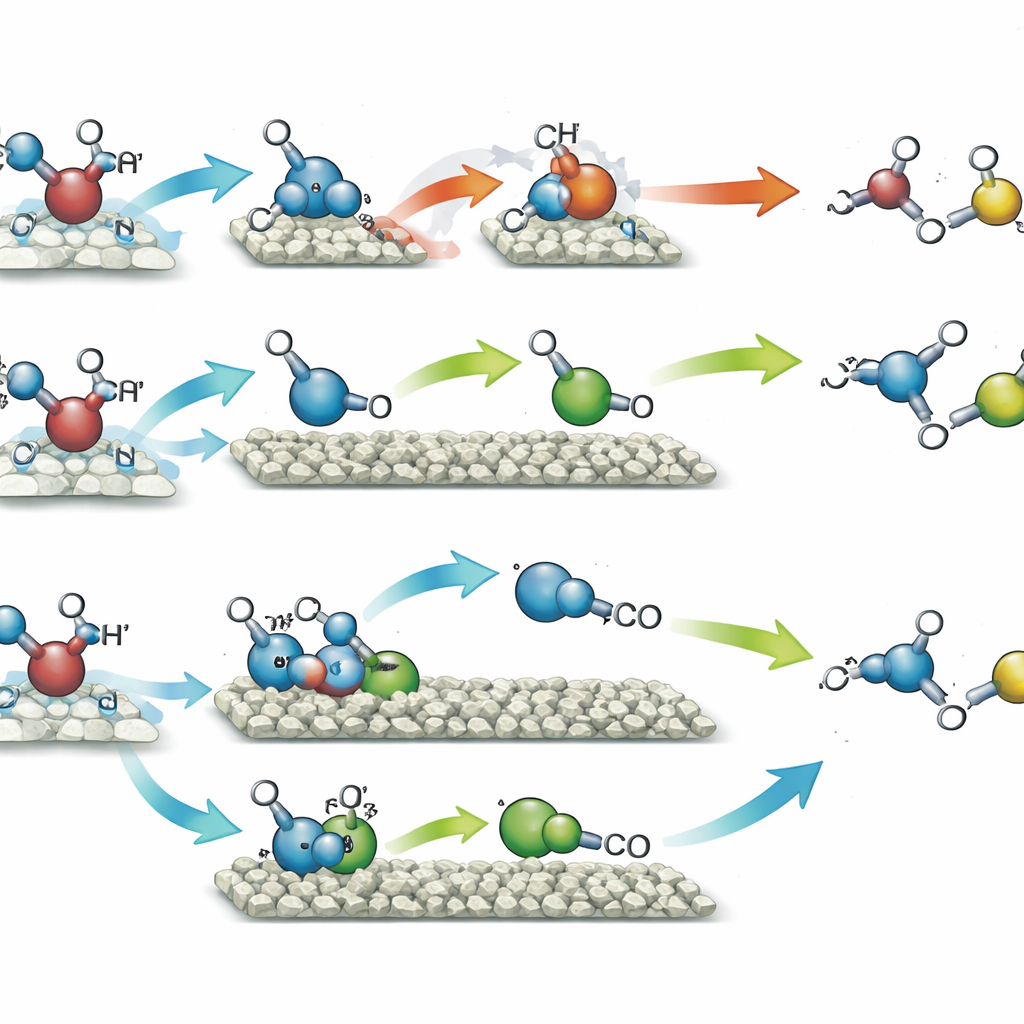
Blick unter die Motorhaube der Reaktion
Um zu verstehen, warum die beiden Nickelanordnungen so unterschiedlich reagierten, kombinierte das Team eine Reihe fortgeschrittener Messmethoden mit Computersimulationen. Elektronische Paramagnetresonanz-Experimente zeigten, dass beide Katalysatoren unter Lichteinfluss methanolbasierte Radikale erzeugten, doch der Cluster-Katalysator förderte zusätzlich die Spaltung der Sauerstoff–Wasserstoff-Bindung, was zu vielfältigeren Reaktionsfragmenten und zum Formaldehyd-Zwischenprodukt führte. Zeitaufgelöste Tests bestätigten, dass dieses Zwischenprodukt zunächst anstieg und dann wieder abfiel, während es zur Bildung von Glykolaldehyd verbraucht wurde. Quantenchemische Berechnungen kartierten die Energiekosten jedes einzelnen Schrittes. Auf einzelnen Nickeleinatomen war die direkte Kopplung zweier identischer Radikale zur Bildung von Ethylenglykol der energetisch einfachste Weg. Auf Nickelclustern hingegen blieb das gleiche Koppelungsprodukt zu stark gebunden, sodass seine Freisetzung erschwert war, während der Weg über das asymmetrische Zwischenprodukt hin zu Glykolaldehyd energetisch bevorzugt wurde.
Ein neuer Hebel für sauberere Chemie
Anschaulich zeigt diese Arbeit, dass das „Wo“ jedes Nickelatoms auf einer Nanometerskala darüber entscheiden kann, „was“ aus Methanol wird, wenn es durch Licht angeregt wird. Durch das Umschalten zwischen Einatomen und kleinen Nickelclustern können die Forschenden das Hauptprodukt von Ethylenglykol zu Glykolaldehyd wechseln, wobei beide effizient und sauber zusammen mit Wasserstoffbrennstoff hergestellt werden. Diese Strategie, Katalysatoren Atom für Atom zu gestalten, bietet einen vielversprechenden Weg, einfache, erneuerbare Rohstoffe wie Methanol in eine Reihe nützlicher Chemikalien umzuwandeln, ohne auf Erdöl, harte Produktionsbedingungen oder verschwenderische Nebenreaktionen angewiesen zu sein.
Zitation: Qi, MY., Tan, CL., Tang, ZR. et al. Efficient methanol upcycling to ethylene glycol and glycolaldehyde via divergent C−C coupling synthesis. Nat Commun 17, 2835 (2026). https://doi.org/10.1038/s41467-026-69656-x
Schlüsselwörter: Methanol-Aufwertung, Photokatalyse, Nickel-Einatome, Ethylenglykol, Glykolaldehyd