Clear Sky Science · de
Exon‑Inklusionssignaturen ermöglichen genaue Schätzung der Aktivität von Spleißfaktoren
Die verborgenen Editierzeichen der Zelle lesen
Jede Zelle in unserem Körper bearbeitet fortlaufend ihre RNA‑Botschaften, bevor sie in Proteine übersetzt werden. Diese Bearbeitung, Spleißen genannt, beeinflusst maßgeblich, ob eine Zelle gesund bleibt oder krebsartig wird. Die Studie hinter diesem Artikel zeigt, dass sich durch genaues Betrachten, welche RNA‑Abschnitte erhalten bleiben oder ausgelassen werden — sogenannte Exon‑Inklusionssignaturen — die Aktivität der molekularen „Editoren“, die das Spleißen steuern, zuverlässig ableiten lässt, selbst bei komplexen Erkrankungen wie Krebs.
Wie Zellen ihre Botschaften schneiden und zusammenfügen
Gene werden nicht als ein durchgängiger Text abgelesen. Stattdessen entfernen Zellen nicht‑kodierende Abschnitte und fügen kodierende Stücke, die Exons, zusammen, um die endgültigen RNA‑Botschaften zu erzeugen. Spezialisierte Proteine, Spleißfaktoren genannt, lenken diesen Schneide‑und‑Klebe‑Prozess und entscheiden, welche Exons inkludiert werden. Ihr Verhalten wird von vielen Regulierungsstufen beeinflusst: wie viel von ihrer eigenen RNA und ihrem Protein produziert wird, welche chemischen Modifikationen sie tragen, wo sie sich in der Zelle befinden und wie sie mit anderen Proteinen interagieren. Weil so viele Stellschrauben das Verhalten von Spleißfaktoren verändern können, reicht das Messen einer einzelnen Datenquelle — etwa der Genexpression — oft nicht aus, um ihr tatsächliches Wirken zu erkennen.
Exonmuster in Aktivitätsmesswerte übersetzen
In Anlehnung an frühere Arbeiten zu Transkriptionsfaktoren schlagen die Autorinnen und Autoren eine andere Strategie vor: Statt Spleißfaktoren direkt zu messen, liest man ihre Aktivität aus ihren Wirkungen ab. Wenn ein Spleißfaktor verändert wird, verschiebt sich die Inklusion seiner Ziel‑Exons in erkennbaren Mustern. Das Team sammelte Hunderte von Experimenten, in denen einzelne Spleißfaktoren herunterreguliert, ausgeschaltet oder überexprimiert wurden, und nutzte diese Daten, um „empirische Netzwerke“ zu erstellen, die jeden Faktor mit den Exons verbinden, die er eindeutig beeinflusst. Anschließend passten sie ein rechnerisches Framework namens VIPER an, um aus einer neuen Exon‑Inklusionssignatur zu lesen und zu bewerten, wie aktiv jeder Spleißfaktor sein muss, um das beobachtete Muster zu erklären.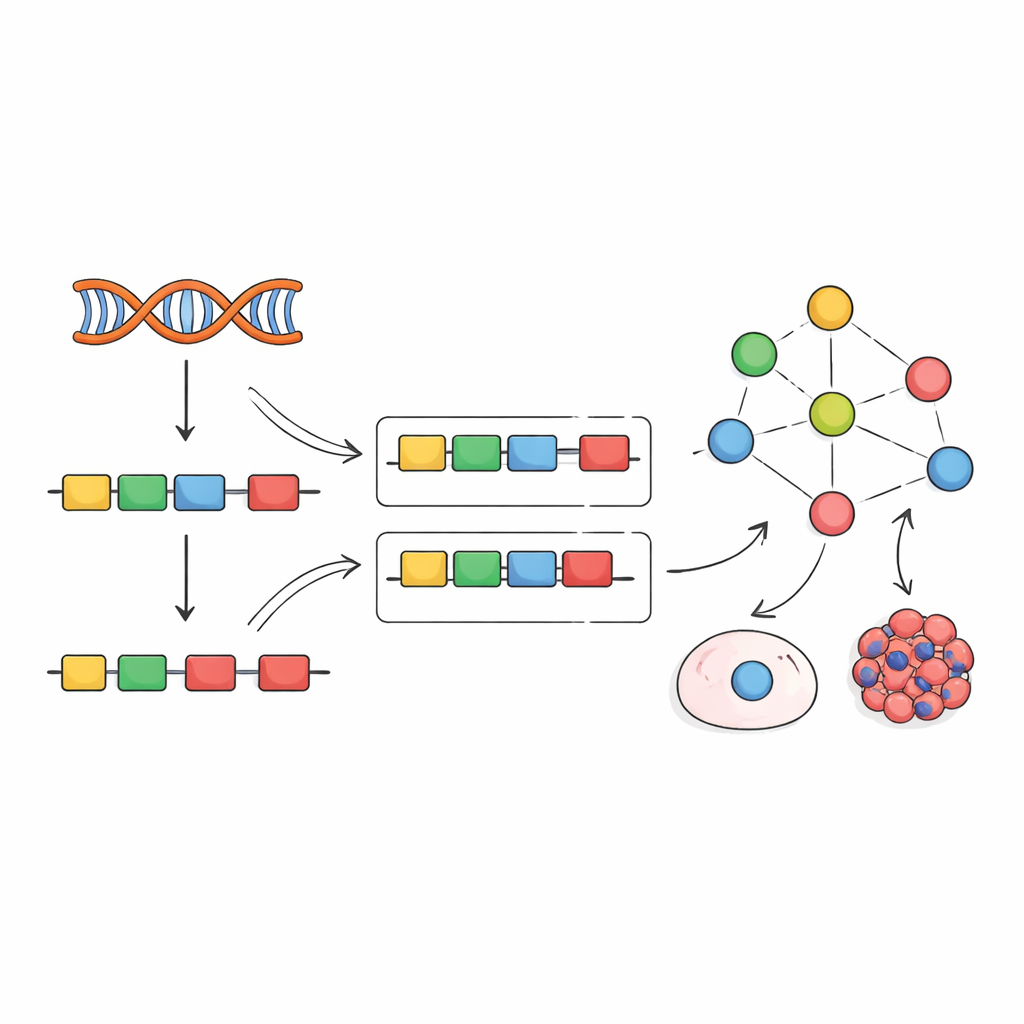
Tests der Methode in realen Störszenarien
Um zu prüfen, ob dieser Ansatz funktioniert, verglichen die Forschenden mehrere Wege, Netzwerke zu erstellen und Aktivitätswerte zu berechnen. Empirische Netzwerke, die direkt aus Perturbations‑Experimenten abgeleitet wurden, kombiniert mit VIPERs Enrichment‑Analyse, übertrafen deutlich Alternativen, die allein auf statistischer Inferenz beruhen. Die Methode identifizierte in den meisten Tests korrekt den experimentell veränderten Spleißfaktor, selbst über verschiedene Zelltypen und Studien hinweg. Sie erfasste auch subtilere Regulationsmechanismen. Ein Beispiel: Das Krebsmedikament Indisulam löst den Abbau des Spleißfaktors RBM39‑Proteins aus, während dessen RNA‑Spiegel anscheinend als Kompensationsversuch ansteigen. Eine herkömmliche Expressionsanalyse würde fälschlich eine erhöhte Aktivität von RBM39 suggerieren, doch der exonsbasierte Aktivitätswert enthüllte korrekt einen starken Funktionsverlust, passend zur bekannten Wirkungsweise des Medikaments.
Verborgene Spleißprogramme im Krebs aufdecken
Mit diesem Werkzeug wandten sich die Autorinnen und Autoren dem Cancer Genome Atlas zu und analysierten Exon‑Level‑Daten aus mehreren Tumortypen und den entsprechenden gesunden Geweben. Sie entdeckten zwei breite, wiederkehrende Spleißprogramme. Das eine Programm umfasst Spleißfaktoren, die in Tumoren tendenziell aktiver sind und mit schlechterem Überleben der Patientinnen und Patienten assoziiert sind — ein onkogen‑ähnliches Programm. Das andere umfasst Faktoren, die systematisch weniger aktiv in Tumoren sind und mit besseren Verläufen verknüpft werden, was an Tumorsuppressoren erinnert. Diese Programme betreffen Gene, die an grundlegenden Merkmalen von Krebs beteiligt sind, etwa schneller Zellteilung und der Fähigkeit von Tumoren, sich dem Immunsystem zu entziehen. Beispielsweise scheinen einige Exons, die vom tumorsuppressor‑ähnlichen Programm reguliert werden, die Ansprechrate auf Immun‑Checkpoint‑Therapien zu beeinflussen — ein Hinweis auf neue Marker oder Interventionspunkte.
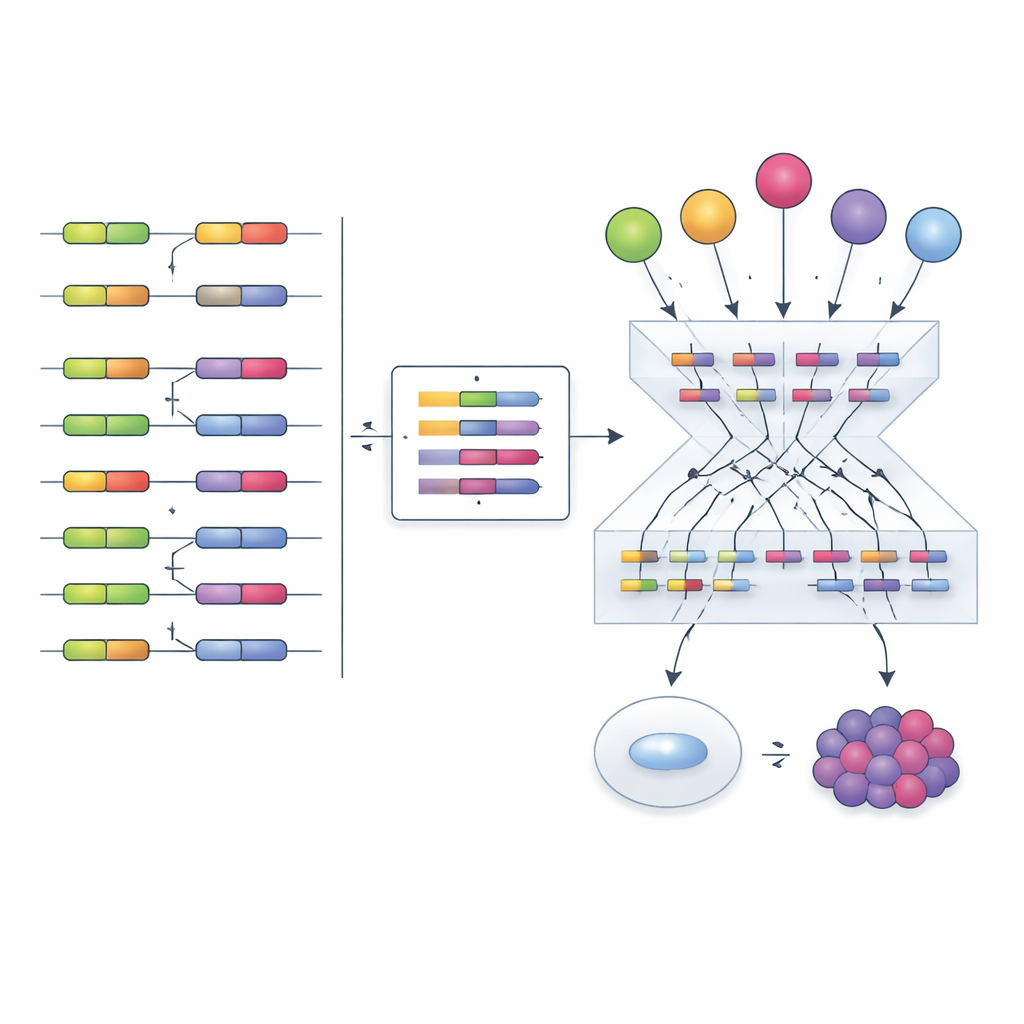
Spleißveränderungen auf dem Weg zur Krebserkrankung folgen
Das Team untersuchte außerdem ein Stufenmodell menschlicher Zellen, die sich von normal über immortalisiert und tumorbildend bis hin zu metastasierend entwickeln. Sie stellten fest, dass das onkogen‑ähnliche Spleißprogramm mit dem Erwerb krebsfördernder Mutationen stärker wird, während das tumorsuppressor‑ähnliche Programm an Aktivität verliert. Durch die Integration mehrerer Datenebenen — RNA‑Spiegel, Proteinmengen, chemische Modifikationen und Spleißveränderungen innerhalb der Spleißfaktoren selbst — identifizierten sie eine fokussierte Menge potenzieller molekularer Ereignisse, die diese Programmverschiebungen antreiben könnten, und lieferten eine priorisierte Liste für zukünftige experimentelle Prüfungen.
Warum das für Patientinnen, Patienten und künftige Forschung wichtig ist
Im Kern zeigt die Studie, dass sich das komplexe Verhalten von Spleißfaktoren auf einen einzigen, interpretierbaren Aktivitätswert verdichten lässt, der aus der Art ableitbar ist, wie Exons inkludiert oder übersprungen werden. Dadurch wird es möglich, Spleißregulation in großen Patientenkohorten und in vielfältigen Experimenten allein mit Standard‑RNA‑Sequenzierungsdaten zu untersuchen, ohne teure Multi‑Omics‑Profilierung. Für Leserinnen und Leser ohne Fachhintergrund lautet die Kernbotschaft: Muster darin, wie Gene geschnitten und zusammengefügt werden, enthalten reichhaltige Informationen über die verborgenen Kontrollsysteme der Zelle, und durch das Entschlüsseln dieser Muster lassen sich neue Krebsantreiber finden, Prognosen verbessern und die Suche nach präziseren Therapien leiten.
Zitation: Anglada-Girotto, M., Segura-Morales, C., Moakley, D.F. et al. Exon inclusion signatures enable accurate estimation of splicing factor activity. Nat Commun 17, 1994 (2026). https://doi.org/10.1038/s41467-026-69642-3
Schlüsselwörter: RNA‑Spleißen, Spleißfaktoren, Krebsgenomik, Transkriptomik, Proteinaktivitäts‑Schätzung