Clear Sky Science · de
LOAd703-induzierte Genmodifikation des Tumormikromilieus in Kombination mit Atezolizumab bei metastasiertem malignem Melanom: eine Phase-I/II-Studie
Warum diese neue Melanom‑Studie wichtig ist
Für Menschen mit fortgeschrittenem Hautmelanom, das auf die heute verfügbaren leistungsfähigen Immuntherapien nicht mehr anspricht, sind die Behandlungsoptionen begrenzt und oft belastend. Diese Studie prüft eine andere Idee: einen gentechnisch veränderten Virus, der direkt in Tumore injiziert wird, zusammen mit einem bereits etablierten immunstärkenden Medikament, um die körpereigene Abwehr zu wecken und die Kontrolle über den Krebs wiederzugewinnen. Die frühen Ergebnisse deuten darauf hin, dass sich dieser Ansatz sicher verabreichen lässt und einem relevanten Teil der Patientinnen und Patienten helfen kann, deren Erkrankung zuvor gegen die Standardtherapie resistent war.
Ein hartnäckiger Hautkrebs, der Behandlungen aussticht
Das Melanom zählt zu den häufigsten schweren Hautkrebserkrankungen in westlichen Ländern, und seine Häufigkeit ist in den letzten Jahrzehnten stark gestiegen. Moderne Checkpoint‑Inhibitoren — die den Bremsen von T‑Zellen lösen — haben die Prognose verändert und die Fünfjahresüberlebensraten beim fortgeschrittenen Melanom auf etwa die Hälfte der Patientinnen und Patienten angehoben. Dennoch hören viele Tumoren schließlich auf zu reagieren. Häufig sind diese resistenten Krebserkrankungen von einer „kalten“ Umgebung aus Zellen und Molekülen umgeben, die Immunzellen fernhält oder abschaltet. Wege zu finden, dieses Tumormikromilieu so umzuprogrammieren, dass T‑Zellen den Tumor wieder erkennen und angreifen können, ist eine zentrale Forschungsaufgabe.
Ein Virus, das die Nachbarschaft des Tumors umgestaltet
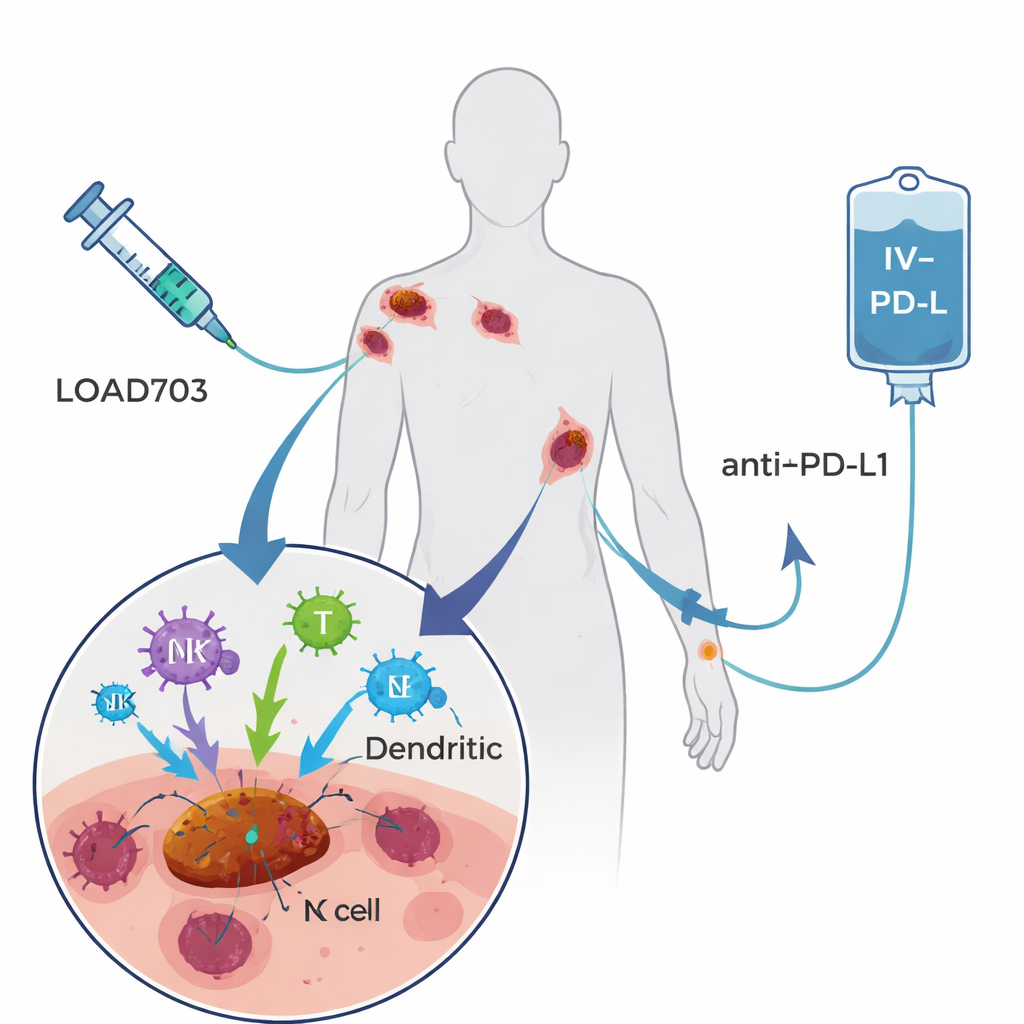
Die hier getestete Therapie, LOAd703 genannt, ist ein modifizierter Adenovirus — eine Art Erkältungsvirus —, der so konstruiert wurde, dass er zwei Aufgaben erfüllt. Erstens repliziert er bevorzugt in Tumorzellen und zerstört diese, eine Strategie, die als onkolytische Virotherapie bekannt ist. Zweitens trägt er genetische Anweisungen für zwei starke immunstimulierende Signale, die auf infizierten Zellen exprimiert werden. Diese Signale, CD40L und 4‑1BBL, fördern die Reifung professioneller Immunwächter (dendritische Zellen) und deren Präsentation von Tumorfragmenten und stärken sowie vermehren T‑Zellen und natürliche Killerzellen, die gegen den Krebs kämpfen. Die Studienteilnehmenden erhielten alle drei Wochen LOAd703 direkt in einen oder mehrere Tumore injiziert, zusammen mit Atezolizumab, einem etablierten Antikörper, der intravenös verabreicht wird und die PD‑L1‑Bremse der T‑Zellen blockiert. Die Hoffnung war, dass das Virus Tumore in körpereigene Impfstoffproduktionsstätten verwandelt, während der Antikörper die wiederbelebten T‑Zellen aktiv hält.
Wer behandelt wurde und wie es ihnen erging
Die Phase‑I/II‑Studie schloss 24 Personen mit Melanom im Stadium IV ein, das trotz mindestens einer vorherigen PD‑1‑Blockade eindeutig progredient war; viele hatten bereits mehrere Linien von Immuntherapien und zielgerichteten Medikamenten erhalten. Es wurden zwei Virendosisstufen getestet. Insgesamt war die Kombination gut verträglich. Die häufigsten mit dem Virus in Zusammenhang stehenden Nebenwirkungen — Fieber, Schüttelfrost, Übelkeit und grippeähnliche Symptome — waren größtenteils mild und vorübergehend. Nur zwei Patientinnen bzw. Patienten erlitten bei der höheren Dosis ernstere, jedoch reversibele Reaktionen, und niemand musste die Behandlung aufgrund virusbedingter Probleme abbrechen. Betrachtete man die Tumorantworten, zeigten vier Patientinnen bzw. Patienten (17 %) messbare Tumorschrumpfungen, und mehr als die Hälfte hatte zumindest zeitweise eine stabile Erkrankung. Zwei Jahre nach Studieneintritt lebte nahezu die Hälfte der Teilnehmenden noch, darunter einige, deren Bildgebung nach Abschluss der Therapie eine langanhaltende Kontrolle oder vollständige Beseitigung nachweisbarer Erkrankung zeigte.
Anzeichen für eine Wiederaktivierung des Immunsystems
Um zu untersuchen, was in den Tumoren und im Blut geschah, analysierte das Team Gewebebiopsien und Blutproben, die vor der Behandlung und etwa neun Wochen nach Beginn entnommen wurden. In den injizierten Tumoren beobachteten sie eine erhöhte Aktivität von Genen, die mit Typ‑1‑Immunantworten assoziiert sind, einschließlich Markern aktivierter T‑Zellen und natürlicher Killerzellen, sowie Molekülen, die diesen Zellen helfen, aus den umliegenden Blutgefäßen in Tumore einzudringen. Signale, die mit der Antigenpräsentation — dem Prozess, durch den Tumorfragmente T‑Zellen gezeigt werden — verbunden sind, nahmen ebenfalls zu, was darauf hindeutet, dass die virale Therapie das Tumormikromilieu von unterdrückend zu immunfreundlicher umwandelte. Im Blut stiegen mehrere immunbezogene Proteine, einschließlich PD‑L1 selbst, nach der Therapie an, was mit einer breiten Aktivierung immunologischer Wege übereinstimmt. Patientinnen und Patienten mit längerem Überleben zeigten tendenziell Genmuster, die mit robuster T‑Zell‑Funktion und antiviraler Schutzwirkung verknüpft sind, während kürzer überlebende Personen Muster zeigten, die mit unterdrückenden Zelltypen und Gewebeumbau‑Signalen assoziiert waren.
Was das für die künftige Versorgung bedeuten könnte
Dies war eine kleine, einarmige Studie ohne Vergleichsgruppe, sodass Aussagen zu Überleben und Ansprechrate mit Vorsicht zu interpretieren sind. Dennoch deuten die gute Verträglichkeit, die Immunaktivierung in den Tumoren und die ermutigende Krankheitskontrolle bei stark vorbehandelten Patientinnen und Patienten darauf hin, dass gentechnisch veränderte onkolytische Viren wie LOAd703 das Melanom für Checkpoint‑Blockade wieder empfindlich machen oder Tumore sogar eigenständig in Schach halten könnten. Die Ergebnisse untermauern die Notwendigkeit größerer, kontrollierter Studien, möglicherweise in Kombination mit weiteren immunzielgerichteten Medikamenten, um zu klären, welche Patientengruppen am meisten profitieren und wie sich diese Strategie am besten in die Melanom‑Behandlung integrieren lässt.
Zitation: Hamid, O., Ekström-Rydén, V., Mehmi, I. et al. LOAd703-induced tumor microenvironment gene engineering in combination with atezolizumab in metastatic malignant melanoma: a phase I/II trial. Nat Commun 17, 1760 (2026). https://doi.org/10.1038/s41467-026-69629-0
Schlüsselwörter: Melanom, Immuntherapie, onkolytisches Virus, Tumormikromilieu, Resistenz gegenüber Checkpoint-Inhibitoren