Clear Sky Science · de
Wirkstoff-gekoppelte Medikamente ermöglichen photocatalytische Doppel‑Decaging von Stickstoffmonoxid und Anästhetika für antibakterielle Analgesie
Gegen Keime und Schmerz zugleich
Bakterielle Infektionen gefährden nicht nur unsere Gesundheit; sie schmerzen auch — oft sehr. Übliche Behandlungen zielen meist auf die Erreger, während Patienten zusätzlich auf separate Schmerzmittel angewiesen sind, die schnell nachlassen oder Nebenwirkungen verursachen können. Diese Studie stellt eine lichtgesteuerte Therapie vor, die darauf abzielt, Bakterien zu töten und Schmerzen in einem abgestimmten Schritt zu lindern, und so einen Ausblick auf intelligentere, komfortablere Infektionsbehandlungen bietet.
Die Idee eines Zwei‑in‑Eins‑Medikaments
Die Forscher bauten ihren Ansatz um Tetracain auf, ein bekanntes Lokalanästhetikum zur Betäubung von Haut und Nerven. Sie verbanden chemisch Stickstoffmonoxid, ein kleines Gas mit starken antibakteriellen und entzündungshemmenden Eigenschaften, mit Tetracain. So entstand ein „Prodrug“ namens TTC‑NO, das weitgehend inaktiv ist, bis es ausgelöst wird. TTC‑NO wurde zusammen mit einem lichtempfindlichen Hilfsmolekül in winzige Polymerblasen — Micellen — verpackt, die sich in wässrigen Umgebungen wie Blut oder Gewebeflüssigkeit bewegen können. 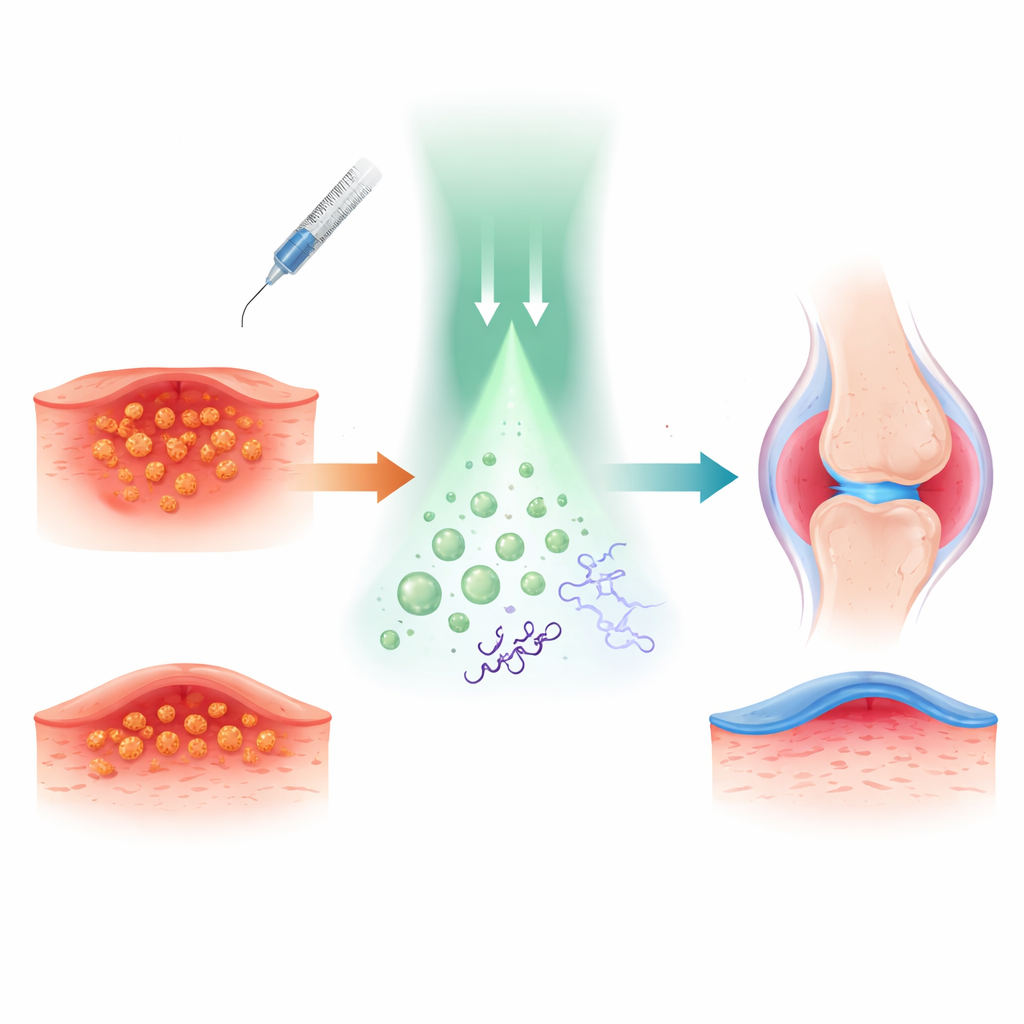
Das Medikament mit sanftem Licht einschalten
Um zu verstehen, wie dieser Licht‑Schalter funktioniert, untersuchte das Team die Chemie in Lösung. Sie zeigten, dass ein photocatalytischer Iridiumkomplex bei Bestrahlung mit grünem Licht ein Elektron auf TTC‑NO übertragen kann. Dies schwächt eine bestimmte Bindung, wodurch Stickstoffmonoxid freigesetzt und Tetracain in seine aktive Form zurückgeführt wird. Messungen mittels Spektroskopie und Chromatographie bestätigten, dass TTC‑NO unter diesen Bedingungen nahezu vollständig in Tetracain und Stickstoffmonoxid umgewandelt wird, während es im Dunkeln im Wesentlichen unverändert bleibt. Kapselten die Forscher die beiden Komponenten in Micellen, blieben die Partikel stabil, etwa 80 Nanometer groß, und setzten ihren Inhalt nur bei Bestrahlung frei. Damit zeigt sich, dass das Konzept des „drug‑caged drug“ von außen mit Licht kontrollierbar ist.
Infizierte Wunden schneller heilen lassen
Als Nächstes testete das Team das System an Mäusen mit absichtlich mit methicillinresistentem Staphylococcus aureus (MRSA) infizierten Hautwunden, einem problematischen Krankenhauskeim. Einige Wunden erhielten Standardbehandlungen wie ein Antibiotikum oder Wachstumsfaktoren, andere wurden mit den TTC‑NO‑Micellen behandelt, teils mit, teils ohne Licht. Bei Aktivierung durch Licht reduzierte das TTC‑NO‑System die Bakterienzahlen deutlich, dämpfte Entzündungen, förderte die Neubildung von Blutgefäßen und steigerte die Kollagenablagerung — alles Voraussetzungen für eine ordnungsgemäße Reparatur. Solche Wunden schlossen schneller und vollständiger als solche, die nur Tetracain oder unbeleuchtete Micellen erhielten, und erreichten eine Leistung, die mit einem gängigen Antibiotikum vergleichbar war. Wichtigerweise zeigten Sicherheitsuntersuchungen keine nennenswerten Schäden an Organen oder Blutparametern.
Schmerzlinderung und Beruhigung von Nervenaktivität
Da Infektion und Gewebeschaden Schmerzbahnen stark aktivieren, maßen die Wissenschaftler Schmerzreaktionen im gleichen Wundmodell sorgfältig. Konventionelles Tetracain erhöhte kurzzeitig die Kraft, die nötig ist, um eine Schmerzreaktion auszulösen, ließ aber innerhalb weniger Stunden nach. Im Gegensatz dazu boten lichtaktivierte TTC‑NO‑Micellen eine Linderung für bis zu 12 Stunden. Mikroskopische Untersuchungen von Nervenknoten nahe dem Rückenmark und Aktivitätsmessungen in der sensorischen Großhirnrinde zeigten, dass die kombinierte Behandlung das Feuern schmerzempfindlicher Neurone noch lange dämpfte, nachdem reines Tetracain seine Wirkung verloren hatte. Weitere Experimente deuteten darauf hin, dass die verlängerte Wirkungsdauer von der Reduktion der bakteriellen Last und der Entzündung durch Stickstoffmonoxid herrührt und nicht allein von der Betäubung der Nerven.
Schützen schmerzhafter, infizierter Gelenke
Die Forscher prüften das System außerdem an Mäusen mit septischer Arthritis, einer schweren MRSA‑Infektion im Kniegelenk, die Schwellung, Knochenverlust und starke Schmerzen verursacht. Lichtaktivierte TTC‑NO‑Micellen verringerten die Gelenkbreite, senkten die Bakterienzahlen und schützten die Knochenstruktur, wie hochauflösende Scans zeigten. Schadliche Entzündungsmediatoren im Blut nahmen ab, während schützende Signalstoffe anstiegen. Verhaltenstests zeigten, dass behandelte Mäuse stärkeren mechanischen Druck auf die betroffene Pfote ertragen konnten und sich in einem offenen Arena‑Test freier bewegten — wiederum mit länger anhaltender Linderung als durch Tetracain allein. Nerven‑ und Hirnmessungen spiegelten diese Verhaltensverbesserungen wider und deuteten auf eine weitreichende Dämpfung der Schmerzbahnen hin, ohne offensichtliche lokale oder systemische Toxizität. 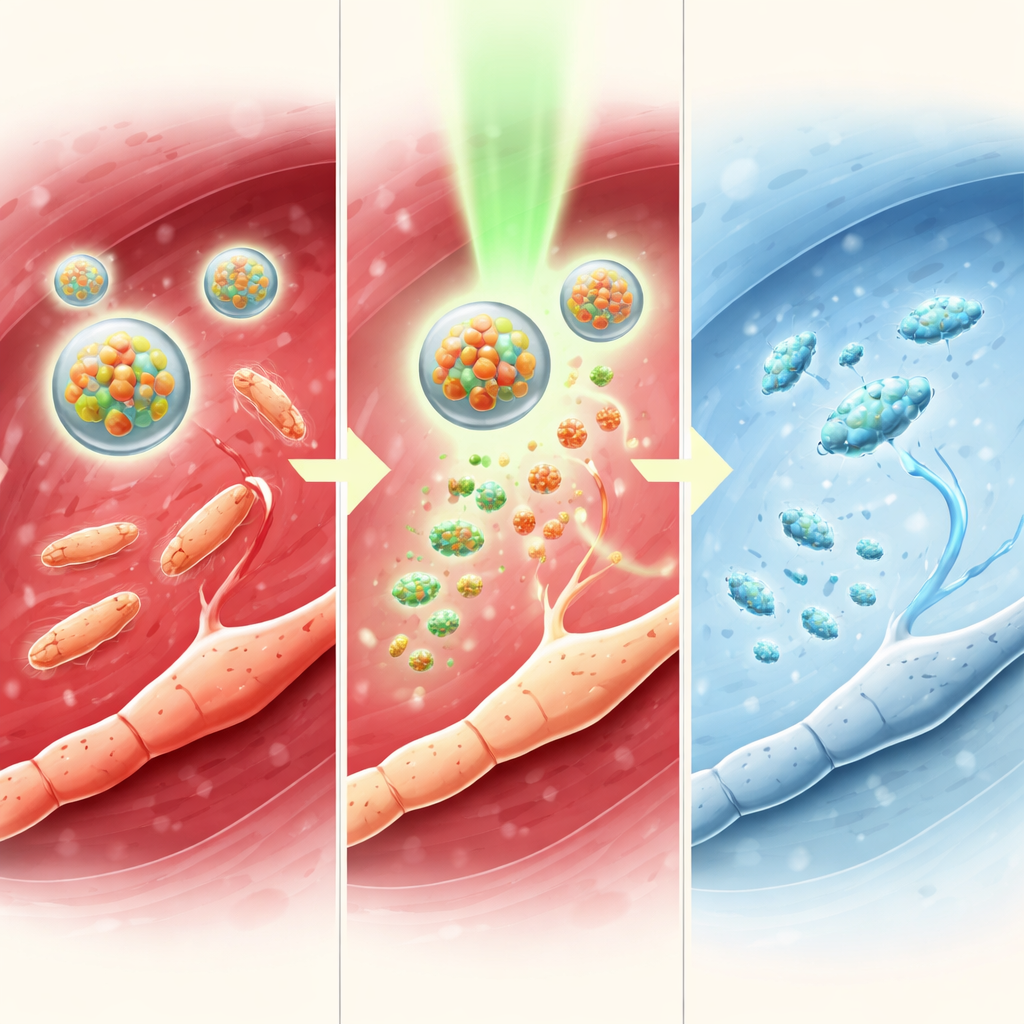
Was das für Patienten bedeuten könnte
Insgesamt demonstriert die Arbeit ein einziges, lichtaktiviertes Nanosystem, das hartnäckige bakterielle Infektionen beseitigen und gleichzeitig die damit verbundenen Schmerzen deutlich reduzieren kann. Durch die chemische „Einbettung“ eines Anästhetikums in eine stickstoffmonoxid‑freisetzende Struktur und die Verpackung in Micellen erreichen die Autoren eine bedarfs‑ und lokal begrenzte Freisetzung zweier nützlicher Wirkstoffe mittels mildem sichtbarem Licht. In Tiermodellen für Hautwunden und Gelenkinfektionen beschleunigt dieses Design die Heilung und verlängert die Schmerzlinderung gegenüber einem konventionellen Lokalanästhetikum. Auch wenn vor einem Einsatz am Menschen noch umfangreiche Tests nötig sind, zeigt die Studie, wie intelligente, schaltbare Medikamente künftig Infektionsbehandlungen wirksamer und komfortabler machen könnten.
Zitation: Zhang, J., Gan, G., Cao, C. et al. Drug-caged drugs enable photocatalytic dual decaging of nitric oxide and anesthetics for antibacterial analgesia. Nat Commun 17, 2843 (2026). https://doi.org/10.1038/s41467-026-69624-5
Schlüsselwörter: Stickstoffmonoxid‑Therapie, lichtaktivierte Medikamente, antibakterielle Analgesie, Nanomedizin, MRSA‑Infektionen