Clear Sky Science · de
T-Zellen, die gegen den Dickkopf‑1–A2-Komplex entwickelt wurden, können zur Behandlung von HLA‑A2+ soliden und hämatologischen Krebserkrankungen eingesetzt werden
Neue Hoffnung für schwer behandelbare Krebsarten
Viele hochwirksame neue Immuntherapien funktionieren gut bei Blutkrebserkrankungen, scheitern jedoch häufig an soliden Tumoren wie Pankreas-, Lungen- und Brustkrebs. Diese Studie stellt eine speziell entwickelte T‑Zelle vor, die auf eine molekulare „Flagge“ zielt, die in einer breiten Palette von Krebsarten vorkommt, aber weitgehend in normalen Geweben fehlt. Das eröffnet die Möglichkeit einer einzigen Behandlung, die sowohl solide als auch hämatologische Tumoren bei Patienten mit einem verbreiteten Immuntyp sicher ansprechen könnte.
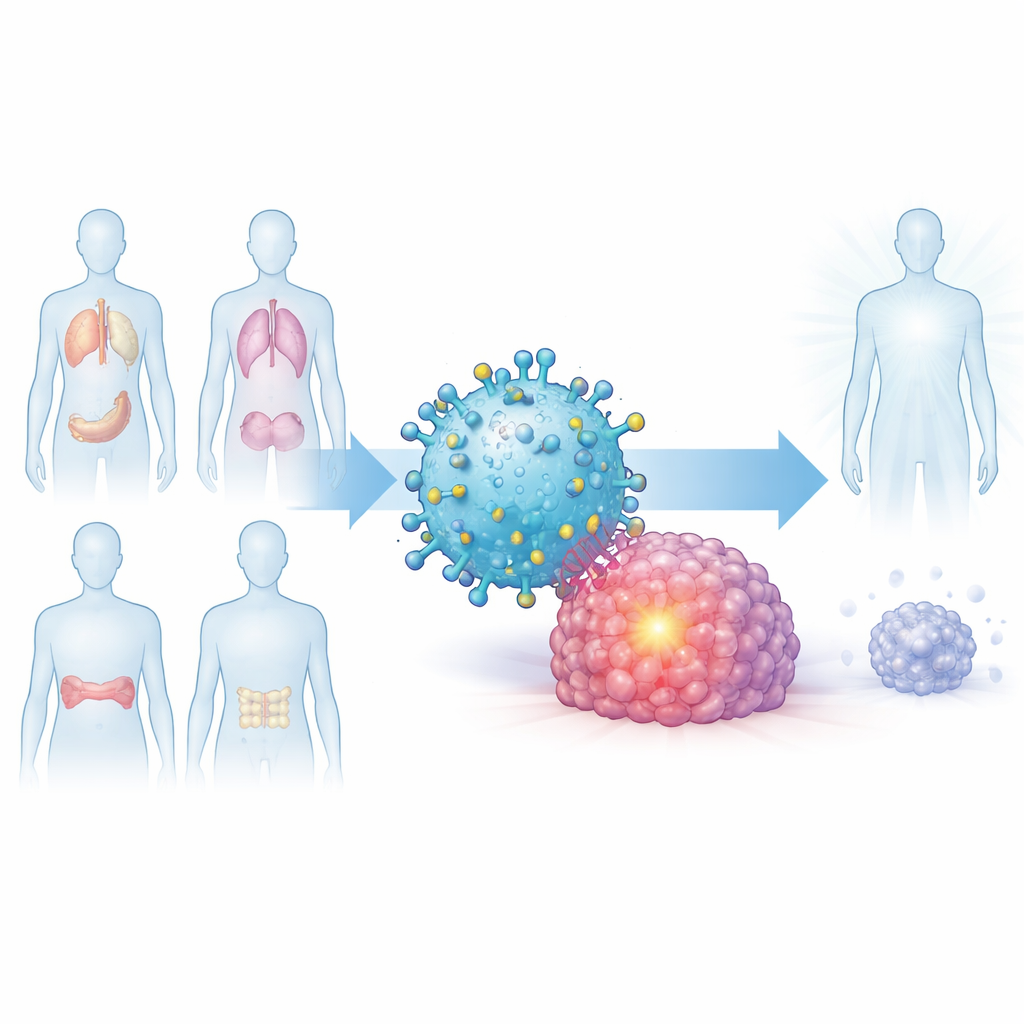
Ein gemeinsames Signal, das viele Tumoren teilen
Die Forscher fragten zunächst, ob es ein gemeinsames molekulares Merkmal gibt, das in verschiedenen Krebsarten vorkommt, aber selten in gesunden Organen. Sie konzentrierten sich auf ein Protein namens Dickkopf‑1 oder DKK1, das Zellwachstumspfade reguliert und in hohen Mengen beim Multiplen Myelom, Pankreaskrebs, Lungenkrebs und aggressivem triple-negativem Brustkrebs vorkommt. Durch die Auswertung großer öffentlicher Gen-Datenbanken und die Untersuchung von Tumorproben zeigten sie, dass DKK1 in vielen Tumoren deutlich häufiger vorkommt als in entsprechenden gesunden Geweben und dass Patientinnen und Patienten mit stärkerer DKK1‑Expression in ihren Tumoren oft eine schlechtere Überlebensprognose haben.
Eine Tumorflagge in ein präzises Ziel verwandeln
Da DKK1 normalerweise außerhalb von Zellen vorkommt, ist es kein offensichtlicher Ansatzpunkt für T‑Zellen, die kurze Proteinstücke erkennen, welche von HLA‑Molekülen an der Zelloberfläche präsentiert werden. Frühere Arbeiten hatten ein kurzes DKK1‑Fragment identifiziert, das von einem sehr verbreiteten HLA‑Typ, bekannt als HLA‑A2, präsentiert wird. Das Team hatte bereits einen Antikörper namens C2 entwickelt, der dieses DKK1‑Fragment erkennt, wenn es von HLA‑A2 auf der Tumorzelloberfläche präsentiert wird, jedoch nicht auf den meisten gesunden Zellen. In der vorliegenden Studie bauten sie einen chimären Antigenrezeptor (CAR) unter Verwendung des Erkennungsanteils dieses Antikörpers und verbanden ihn mit intrazellulären T‑Zell‑Signalbausteinen, sodass gewöhnliche T‑Zellen umprogrammiert werden können, um die DKK1–HLA‑A2‑Kombination zu erkennen, die als DKK1‑A2‑Komplex bezeichnet wird.
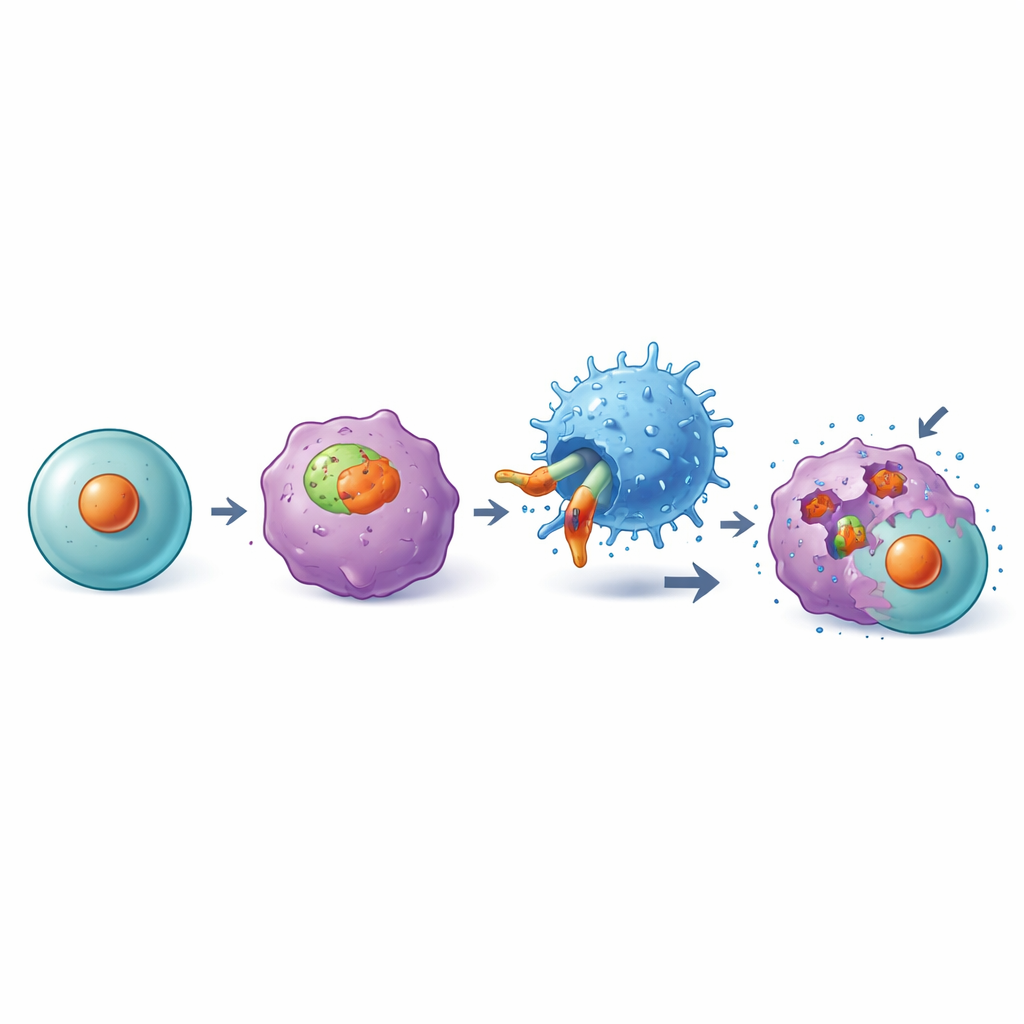
Entwickelte T‑Zellen, die Tumoren aufspüren und zerstören
Die Wissenschaftler testeten diese DKK1‑A2 CAR‑T‑Zellen gegen ein breites Panel menschlicher Krebszelllinien im Labor, darunter Multiple Myelom, Pankreas‑, Lungen‑ und triple‑negativen Brustkrebszellen. Immer wenn Tumorzellen sowohl DKK1 als auch HLA‑A2 präsentierten, vermehrten sich die entwickelten T‑Zellen kräftig, setzten starke Immunmoleküle frei und töteten die Krebszellen effizient. Wurde DKK1 aus den Tumorzellen entfernt oder fehlte HLA‑A2, griffen die CAR‑T‑Zellen nicht mehr an, was zeigt, dass ihre Aktivität hochspezifisch für das beabsichtigte Ziel ist.
Wirksamkeitsnachweis in lebenden Modellen
Um zu prüfen, ob dieser Ansatz etablierte Tumoren in lebenden Organismen verkleinern kann, nutzte das Team mehrere Mausmodelle mit menschlichen Tumoren. DKK1‑A2 CAR‑T‑Zellen kontrollierten oder eliminierten Multiples Myelom, das im Knochenmark wuchs, Pankreastumoren, die in die Bauchspeicheldrüse eingepflanzt worden waren, über die Blutbahn gestreuten Lungenkrebs und aggressive Brustkrebserkrankungen, während standardmäßig eingesetzte CD19‑gerichtete CAR‑T‑Zellen als Kontrolle kaum Wirkung zeigten. Die Therapie wirkte auch gegen Tumoren, die aus echten Patienten‑Pankreaskarzinomen in Mäuse transplantiert worden waren und damit die menschliche Erkrankung realitätsnäher nachbilden. Eine humanisierte Version des CAR, die für den klinischen Einsatz geeignet ist, zeigte eine noch bessere Langzeitkontrolle, teils weil diese T‑Zellen einen erinnerungsähnlichen Zustand einnahmen, der es ihnen erlaubte, anzuhalten und erneut zu reagieren, wenn Tumoren wieder auftauchten.
Sicherheitsprüfungen an gesundem Blut und Organen
Jede zielgerichtete Therapie muss gesunde Gewebe schonen. Die Autoren färbten daher Dutzende von Typen normalen menschlichen Gewebes an und stellten fest, dass der DKK1‑A2‑Komplex mit Ausnahme der Mandeln im Grunde nicht vorhanden war. In Labortests beschädigten die DKK1‑A2 CAR‑T‑Zellen keine Blut‑ oder Knochenmarkszellen von gesunden HLA‑A2‑positiven Spendern, im Gegensatz zu CD19 CAR‑T‑Zellen, die erwartungsgemäß normale B‑Zellen zerstörten. In Mausmodellen, die so konstruiert waren, dass sie humanes DKK1 und HLA‑A2 exprimieren, führten die neuen CAR‑T‑Zellen nicht zu einer Erschöpfung wichtiger Blutzellpopulationen oder der Thrombozyten und verursachten weniger Anzeichen einer gefährlichen Zytokinausschüttung als einige bestehende CAR‑Konstruktionen, was ein günstiges Sicherheitsprofil unterstützt.
Was das für Patientinnen und Patienten bedeuten könnte
Insgesamt deuten die Ergebnisse darauf hin, dass der DKK1‑A2‑Komplex ein vielversprechendes „Zielgebiet“ ist, das bei vielen schwer zu behandelnden Krebsarten auftritt, aber weitgehend in normalen Geweben fehlt. Mit dem DKK1‑A2‑CAR bewaffnete T‑Zellen konnten in präklinischen Modellen unterschiedliche Tumoren erkennen und zerstören und zeigten dabei begrenzte Toxizität. Wenn sich diese Ergebnisse beim Menschen bestätigen, könnte dieser Ansatz eine neue gemeinsame Immuntherapie für Patienten mit HLA‑A2‑positivem Multiplem Myelom, Pankreas‑, Lungen‑ und bestimmten Brustkrebserkrankungen bieten und den Anwendungsbereich von CAR‑T‑Behandlungen über Blutkrebserkrankungen hinaus auf solide Tumoren ausweiten.
Zitation: Zhang, Y., Xiong, W., Qian, J. et al. T cells engineered against Dickkopf-1-A2 complex can be used to treat HLA-A2+ solid and hematologic cancers. Nat Commun 17, 2818 (2026). https://doi.org/10.1038/s41467-026-69621-8
Schlüsselwörter: CAR‑T‑Zelltherapie, DKK1, Pankreaskrebs, Multiples Myelom, Immuntherapie gegen solide Tumoren