Clear Sky Science · de
Isolierbare Radikalkation und Dikation von Dialumenen
Warum diese Aluminiumgeschichte wichtig ist
Chemiker suchen ständig nach günstigeren, reichlicher vorhandenen Metallen, die komplexe Aufgaben übernehmen können, die derzeit teureren Elementen wie Palladium oder Platin vorbehalten sind. Diese Studie zeigt, dass Aluminium – ein Metall, das man sonst von Getränkedosen oder Flugzeugteilen kennt – in ungewöhnlich reaktive Formen überführt werden kann, die sich ein wenig wie winzige elektronische Schalter verhalten. Das Verständnis und die Kontrolle dieser exotischen Aluminiumspezies könnte langfristig helfen, neue Katalysatoren für sauberere chemische Prozesse und Materialien zu entwickeln.
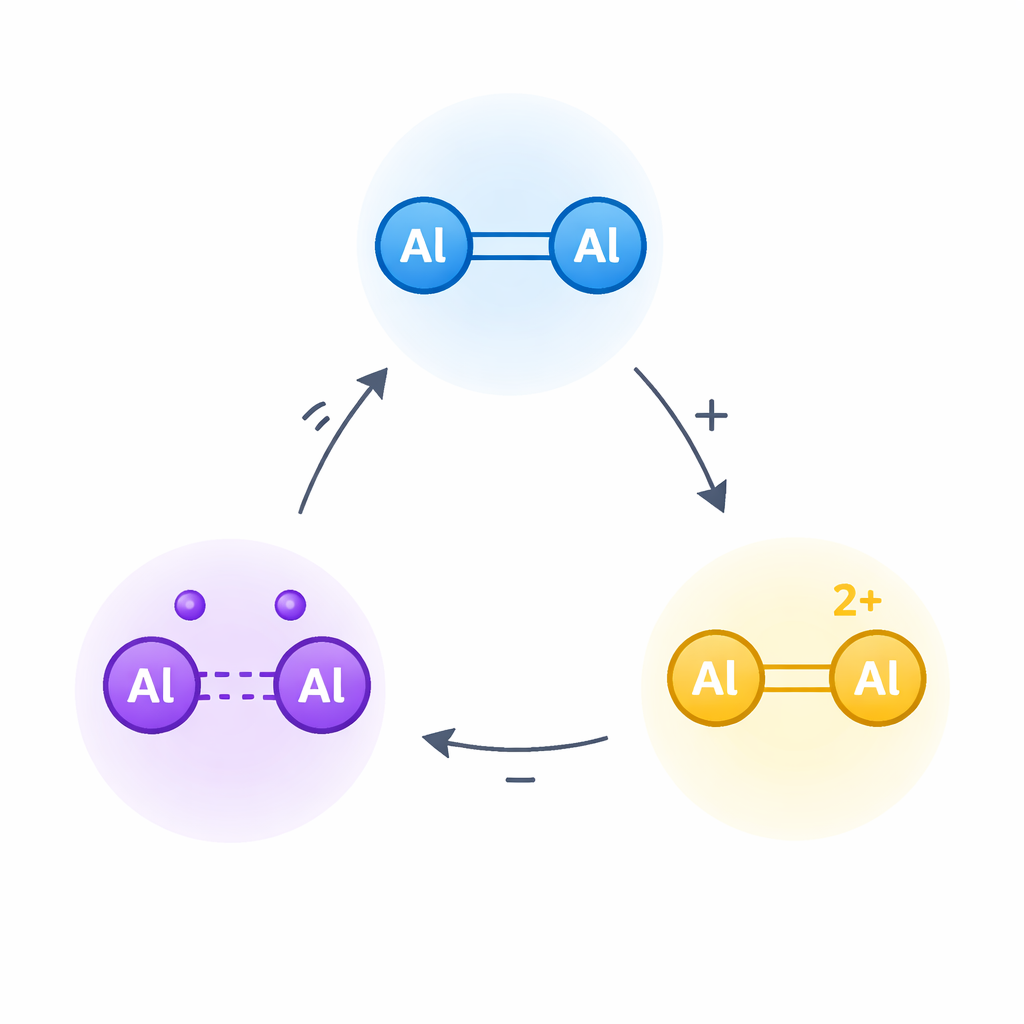
Eine vertraute Bindung als elektronischer Schalter
Die Arbeit konzentriert sich auf Dialumene, Moleküle, in denen zwei Aluminiumatome eine Doppelbindung teilen, ähnlich der Kohlenstoff–Kohlenstoff-Doppelbindung in gewöhnlichen Alkenen. In organischen Molekülen können solche Doppelbindungen schrittweise oxidiert werden, sodass Radikalkationen und dann Dikationen entstehen – stark geladene, hochreaktive Formen, die vielen Reaktionen in der Elektrochemie und Materialwissenschaft zugrunde liegen. Die Autoren fragten, ob die Aluminium–Aluminium-Doppelbindung in Dialumenen einen ähnlichen zweistufigen Oxidationsweg durchlaufen kann, obwohl Aluminium stark elektronenhungrig ist und solche geladenen Spezies ausgesprochen instabil erscheinen sollten.
Entwurf eines schützenden molekularen Rahmens
Um diese Reaktivität zu zähmen, baute das Team ein Dialumene, das von sperrigen siliziumbasierten Gruppen und starken, elektronendonierenden „Carben“-Liganden umgeben ist. Diese wirken wie gepolsterte Rüstung und elektronische Kissen: Sie schützen den empfindlichen Aluminium–Aluminium-Kern vor unerwünschten Reaktionen und liefern dort Elektronendichte, wo sie gebraucht wird. Ausgehend von diesem neutralen Dialumene, bezeichnet als 1, setzten sie sorgfältig ausgewählte Oxidationsmittel ein, um zuerst ein Elektron und dann ein zweites zu entfernen, wodurch zuerst ein aluminiumzentriertes Radikalkation (2) und dann ein Dikation (3) entstanden. Röntgenkristallografie lieferte Momentaufnahmen aller drei Zustände und zeigte, wie die Aluminium–Aluminium-Bindung beim Entziehen von Elektronen schrittweise länger wird und ihren Charakter ändert.
Nachweis eines echten dreizuständigen Redoxzyklus
Schlüsselmessungen bestätigten, dass das Radikalkation tatsächlich ein ungepaartes Elektron trägt, das zwischen den beiden Aluminiumatomen lokalisiert ist und nicht auf den umgebenden Liganden. Elektronenspin-Resonanzspektroskopie zeigte ein klares Signal, das mit einem einzelnen Elektron übereinstimmt, das von beiden Aluminiumzentren geteilt wird. Rechenstudien unterstützten dieses Bild und zeigten, dass das verbleibende Bindungselektron ein überwiegend aluminium–aluminium-orbital besetzt. Wenn das zweite Elektron entfernt wird, um das Dikation zu bilden, schwächt sich die Bindung in Richtung einer Einfachbindung und positive Ladung sammelt sich am Aluminiumpaar an. Wichtig ist, dass die Forscher zeigten, dass all diese Veränderungen reversibel sind: Durch Zugabe von Elektronen mit einem Reduktionsmittel wird zuerst das Radikalkation und dann das ursprüngliche Dialumene regeneriert, und durch Mischen der neutralen und der zweifach geladenen Form entsteht durch Komproportionierung das Radikalkation. Zusammen demonstrieren diese Reaktionen einen robusten, isolierbaren dreizuständigen Redoxzyklus an einer einfachen Aluminium–Aluminium-Einheit.
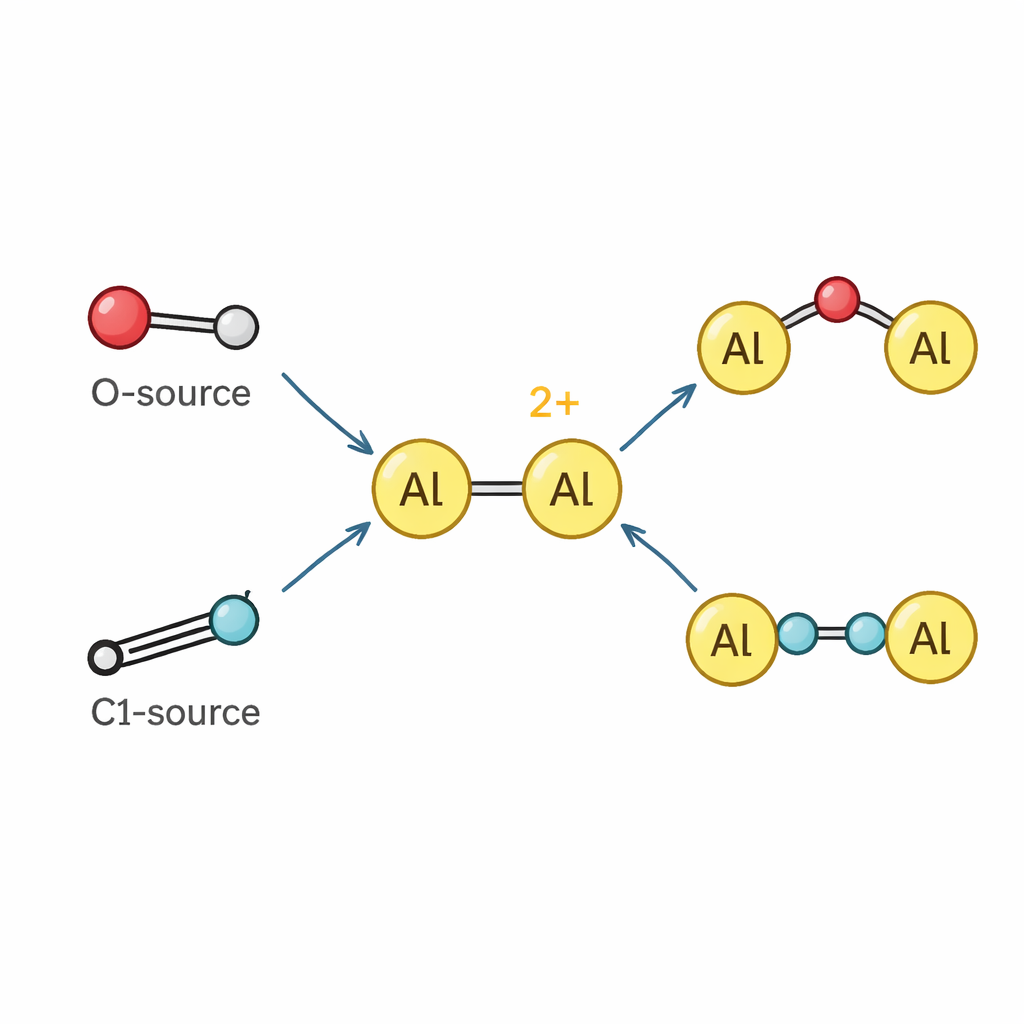
Aluminium wie ein Übergangsmetall wirken lassen
Mit dem Dikation in der Hand untersuchte das Team, wie es mit anderen Molekülen reagiert. Weil seine Aluminiumatome stark elektronengierig sind, verhält sich das Dikation wie eine starke Lewis-Säure und bindet bereitwillig basische Partner wie Pyridin und verwandte Moleküle, wodurch neue Dialuminiumkomplexe entstehen. Über einfache Bindung hinaus kann das Dikation chemische Bindungen spalten und sich einklinken. Es entzieht Distickstoffoxid und Pyridin-N-oxid Sauerstoffatome und bildet stabile Spezies, in denen ein Sauerstoffatom die beiden Aluminiumzentren überbrückt oder in eine kurze Aluminium–Sauerstoff–Silizium-Kette eingebaut wird, die an einen winzigen Fragment eines Zeolithgerüsts erinnert. Es geht auch mit Isonitrilen ein – kleinen Kohlenstoff–Stickstoff-Einheiten, die als Ein-Kohlenstoff-Bausteine dienen – Verbindungen ein, um sie zu längeren N–C–C–N-Fragmenten zusammenzufügen, die zwischen zwei Aluminiumatomen verlaufen, und demonstriert damit ein seltenes Beispiel für eine von einem Hauptgruppen-Kation getriebene Isonitril‑„Homologation“.
Was das für die Zukunft bedeutet
Anschaulich haben die Forscher eine Aluminium–Aluminium-Bindung in einen kontrollierbaren dreipositionigen elektronischen Schalter verwandelt, der zwischen neutralem, einfach- und zweifach-positiv geladenem Zustand umgeschaltet werden kann, wobei jeder Zustand unterschiedliche Formen und Reaktivitäten aufweist. Die zweifach geladene Variante ist besonders vielseitig: Sie entnimmt Elektronen und kleine Fragmente aus anderen Molekülen auf eine Weise, die sonst eher teureren Übergangsmetallen zugeschrieben wird. Indem gezeigt wurde, dass ein solches Verhalten mit Aluminium möglich ist und die verschiedenen Zustände zuverlässig ineinander überführbar sind, öffnet diese Arbeit die Tür zur Entwicklung neuer, nachhaltiger Katalysatoren und funktionaler Materialien aus einem der reichhaltigsten Metalle der Erde.
Zitation: Liu, X., Kostenko, A., Körber, E. et al. Isolable radical cation and dication of dialumene. Nat Commun 17, 1937 (2026). https://doi.org/10.1038/s41467-026-69607-6
Schlüsselwörter: Aluminiumkatalyse, redox-schaltbare Moleküle, Hauptgruppench chemie, Radikalkationen, Aktivierung kleiner Moleküle