Clear Sky Science · de
Die Treg-γδ-T-Zell-Achse bestimmt die geschlechtsspezifische Dimorphie bei der Hepatokarzinogenese
Warum einige Leberkrebserkrankungen Männer stärker treffen
Ärztinnen und Ärzte wissen seit langem, dass Leberkrebs bei Männern ungefähr doppelt so häufig auftritt wie bei Frauen, doch die Gründe reichen über einfache Unterschiede in den Sexualhormonen hinaus. Diese Studie geht den Immunzellen nach, die in Lebertumoren leben, und deckt ein verstecktes Gespräch zwischen zwei T‑Zell‑Typen auf, das erklärt, warum männliche Lebern verwundbarer sind – und wie dieses Wissen auf neue, gezieltere Therapien hinweisen könnte.
Das immunologische Tauziehen in Lebertumoren
Leberkrebs, insbesondere das hepatozelluläre Karzinom, wächst in einem komplexen Umfeld aus Immunzellen, Blutgefäßen und vernarbtem Gewebe. Die Autoren verglichen Tumoren von Männern und Frauen, sowohl bei Patientinnen und Patienten als auch in Mausmodellen, und fanden ein auffälliges Ungleichgewicht: Männliche Tumoren waren stark mit regulatorischen T‑Zellen, sogenannten Tregs, durchsetzt – einer Zellart, die normalerweise überschießende Immunreaktionen dämpft. Gleichzeitig unterschieden sich die Gesamtzahlen anderer häufiger T‑Zellen zwischen den Geschlechtern kaum. Da hohe Treg‑Werte mit schlechterem Überleben verknüpft waren, vermutete das Team, dass diese Zellen nicht nur Beobachter sind, sondern aktive Komplizen, die Tumoren helfen, der Immunabwehr zu entkommen. 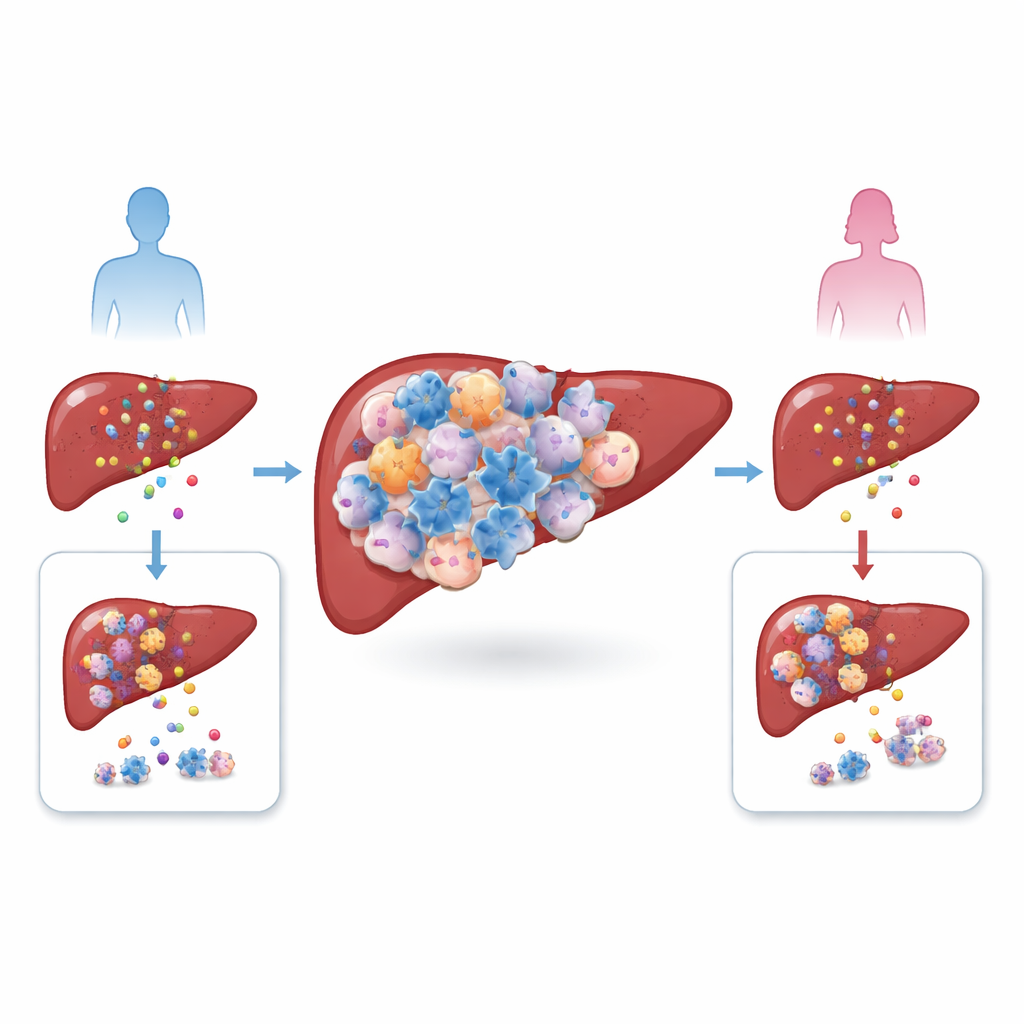
Wie männliche Hormone Unterdrückerzellen anlocken
Um zu verstehen, warum männliche Tumoren mehr Tregs anziehen, konzentrierten sich die Forschenden auf chemische Signale, die von Krebszellen produziert werden. Sie fanden heraus, dass männliche Lebertumoren höhere Mengen eines Moleküls namens Ccl2 herstellen, während Tregs mehr des passenden Rezeptors Ccr2 tragen. Diese Paarung wirkt wie ein Orientierungssignal, das Tregs in den Tumor zieht. Wenn das Ccl2‑Signal oder der Ccr2‑Rezeptor in Mäusen ausgeschaltet wurde, verkleinerten sich die Tumoren und deutlich weniger Tregs wanderten in die Leber ein, besonders bei Männchen. Das Team zeigte dann, dass Testosteron, das wichtigste männliche Sexualhormon, diesen Prozess antreibt: Es aktiviert eine Proteinkette in Leberkrebszellen, die das Ccl2‑Gen einschaltet und so den chemischen Lockruf für Tregs verstärkt. Kastrierte Männchen, die weniger Testosteron produzieren, hatten niedrigere Ccl2‑Werte in ihren Tumoren und weniger einwandernde Tregs.
Schutzzellen, die Krebs bekämpfen könnten — aber gebremst werden
Ein anderer T‑Zell‑Typ, bekannt als Gamma‑Delta‑T‑Zellen, kann als schnelle „Wache“ wirken, die Tumorzellen erkennt und tötet, ohne die übliche Antigenpräsentationsmaschinerie. In gesunder Leber sind diese Zellen relativ selten, doch in Leberkrebs können sie starke Tumorkämpfer sein. Die Studie ergab, dass Tumoren von Frauen mehr dieser Gamma‑Delta‑Zellen enthielten und dass diese aktiver und besser mit toxischen Molekülen ausgerüstet waren. Das Entfernen männlicher Sexualhormone bei Mäusen erhöhte Anzahl und Aktivität der Gamma‑Delta‑Zellen in Tumoren, während klassische CD8‑Killerzellen weitgehend unverändert blieben. In Zellkultur beschädigten Gamma‑Delta‑Zellen Leberkrebszellen leicht, doch dieser Effekt wurde abgeschwächt, wenn Tregs hinzugefügt wurden, was nahelegt, dass Tregs speziell diese vielversprechende antitumorale Population bremsen.
Hypoxie, geheime Pakete und stummgeschaltete Verteidiger
Die Forschenden gingen der Frage nach, wie Tregs Gamma‑Delta‑T‑Zellen abschalten. In Tumoren ist Sauerstoff oft knapp – ein Zustand, der als Hypoxie bezeichnet wird. Unter diesen niedrigen Sauerstoffbedingungen begannen Tregs in männlichen Tumoren, große Mengen eines Proteins namens S100a4 zu produzieren. Anstatt frei zu wirken, wurde S100a4 in winzige, membranumhüllte Partikel verpackt, so genannte extrazelluläre Vesikel. Diese Vesikel knospten von Tregs ab und wurden von benachbarten Gamma‑Delta‑Zellen aufgenommen. Einmal im Inneren veränderte S100a4 die genetischen Steuerungsmechanismen der Zellen: Es verringerte die Zugänglichkeit von DNA‑Regionen, die wichtige Signalisierungs‑ und Tötungsmoleküle kontrollieren, und senkte deren Aktivität. Die Gamma‑Delta‑Zellen reagierten weniger über ihre T‑Zell‑Rezeptoren und waren weniger fähig, toxische Proteine und Zytokine freizusetzen – ihre antitumorale Klinge wurde dadurch wesentlich stumpfer. 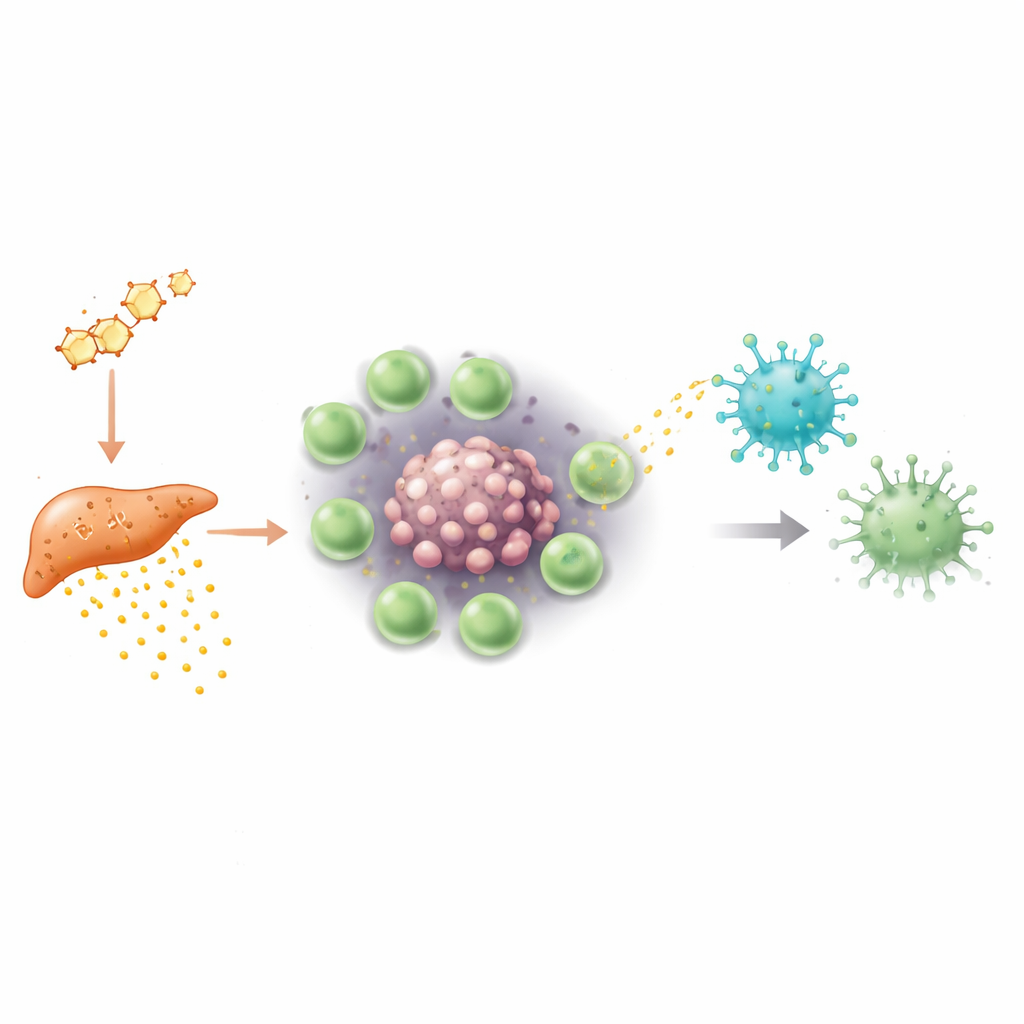
Den schädlichen Kreislauf durchbrechen
Schließlich prüfte das Team, was passiert, wenn diese Treg–S100a4–Gamma‑Delta‑Achse unterbrochen wird. In Mäusen, bei denen Tregs kein S100a4 herstellen konnten, schrumpften männliche Lebertumoren, der Gesamt‑S100a4‑Spiegel in den Tumoren fiel, und Gamma‑Delta‑Zellen wurden zahlreicher und aktiver. Bemerkenswerterweise sank die Anzahl der Tregs im Tumor nicht – nur ihre suppressive Wirkung auf Gamma‑Delta‑Zellen wurde aufgehoben. Diese Veränderung beseitigte nahezu die übliche Lücke in der Tumorlast zwischen männlichen und weiblichen Mäusen und unterstrich, wie zentral dieser Pfad für geschlechtsbasierte Unterschiede bei Leberkrebs ist.
Was das für künftige Therapien bedeutet
Einfach gesagt zeigt die Studie, dass männliche Hormone Leberkrebszellen dazu bewegen, stärkere „Willkommenssignale“ für immununterdrückende Tregs auszusenden. Einmal im Tumor – und unter dem Stress niedriger Sauerstoffversorgung – verschicken diese Tregs S100a4‑gefüllte Vesikel, die nahegelegene Gamma‑Delta‑Zellen stillschweigend entwaffnen, obwohl diese Zellen den Krebs sonst in Schach halten könnten. Indem man entweder das Ccl2‑Signal unterbindet, das Tregs anzieht, oder die S100a4‑Botschaften blockiert, die Gamma‑Delta‑Zellen stummschalten, könnten künftige Therapien die körpereigene Abwehr wiederherstellen – insbesondere bei Männern. Diese Arbeit legt nahe, dass die Behandlung von Leberkrebs geschlechtsbewusst sein und die einzigartigen Stärken der Gamma‑Delta‑T‑Zellen nutzen sollte, statt sie zu übersehen.
Zitation: Liang, Q., Zhang, Q., Zhang, W. et al. Treg-γδ T cell axis determines sexual dimorphism in hepatocarcinogenesis. Nat Commun 17, 2640 (2026). https://doi.org/10.1038/s41467-026-69603-w
Schlüsselwörter: hepatozelluläres Karzinom, regulatorische T-Zellen, Gamma-Delta-T-Zellen, Geschlechtsunterschiede, Tumorimmunologie