Clear Sky Science · de
Pyrimidinerges Kalzium-Signal vermittelt den Zusammenhang von Tubulusstoffwechsel und Fibrose bei Nierenerkrankungen
Warum Nierenvernarbung wichtig ist
Chronische Nierenerkrankungen betreffen weltweit stillschweigend Hunderte Millionen Menschen und enden häufig damit, dass die Nieren vernarben und versteifen. Hat sich diese Vernarbung, Fibrose genannt, erst etabliert, ist verlorene Nierenfunktion nur schwer wiederzugewinnen. Trotzdem fehlen Ärzten nach wie vor Medikamente, die Fibrose gezielt stoppen. Diese Studie stellt eine grundlegende, aber entscheidende Frage: Wie verwandelt sich kurzzeitige Schädigung der Niertubuli allmählich in dauerhaftes Narbengewebe, und könnte das Unterbrechen dieser Ereigniskette das Fortschreiten zur Niereninsuffizienz verlangsamen oder verhindern?
Fleißige Nierentubuli und ihre verborgene Chemie
Die proximalen Tubuli der Niere sind mikroskopische Arbeitstiere, die den Großteil von Wasser und Nährstoffen, die aus dem Blut gefiltert werden, zurückgewinnen. Für diese Aufgabe ist ihr Stoffwechsel ungewöhnlich aktiv. Durch Analyse von Einzelzell-Genexpressionsdaten aus Mäusen fanden die Forschenden, dass diese Tubuluszellen besonders reich an Genen sind, die am Umgang mit Pyrimidinen beteiligt sind — einer Familie kleiner Moleküle, die normalerweise beim Aufbau und der Reparatur von DNA und RNA helfen. In verletzten Tubuli war ein Enzym des sogenannten Salvage-Wegs, die Cytidin-Deaminase, stark hochreguliert, was darauf hindeutet, dass geschädigte Zellen den Pyrimidinverbrauch umorganisieren, um bestimmte energiereiche Bausteine wie eine Verbindung namens UDP aufzufüllen.
Signale, die aus geschädigten Zellen austreten
Als das Team menschliche, tubulusähnliche Zellen im Kulturmodell mit Toxinen verletzte, die Chemotherapie oder Folsäure-Überdosis nachahmen, setzten die Zellen UDP in das umgebende Medium frei. In tatsächlichen Nieren von verletzten Mäusen zeigten Färbungen von Gewebeschnitten sowohl hohe Werte des Pyrimidin-verarbeitenden Enzyms in Tubuli als auch Anzeichen dafür, dass benachbarte Stützzellen, sogenannte Fibroblasten, aktiviert wurden und ihre Form änderten. Fibroblasten sitzen normalerweise ruhig zwischen Tubuli, doch wenn sie aktiviert werden, vermehren sie sich und legen Kollagen und andere Fasern ab, die das Nierengewebe verdicken und versteifen. Diese Beobachtungen legten eine einfache Idee nahe: Verletzte Tubuli könnten chemische Stresssignale „auslaufen“ lassen, die von benachbarten Fibroblasten wahrgenommen werden.
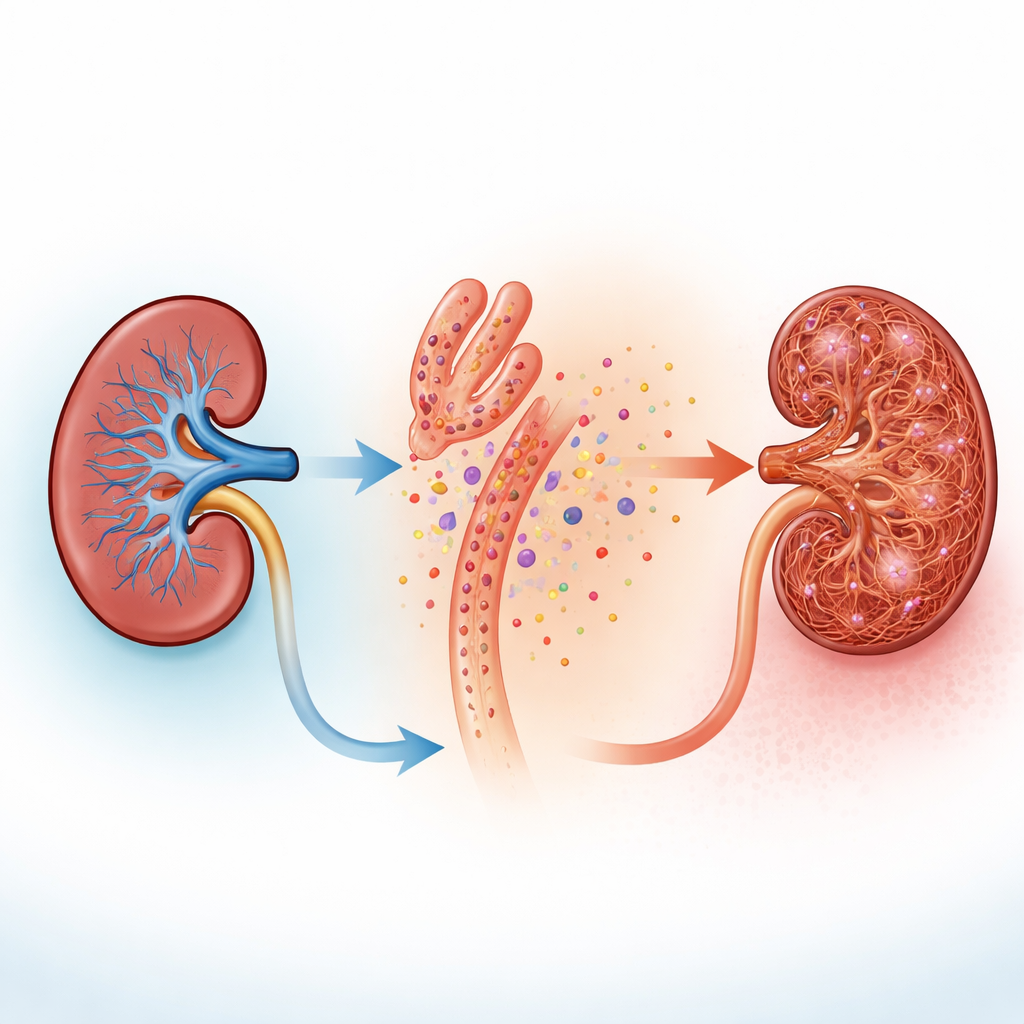
Wie Fibroblasten mit Kalziumflashes zuhören
Als vermutete „Ohren“ der Fibroblasten identifizierten die Autor:innen P2Y6-Rezeptoren, Oberflächenproteine, die auf UDP reagieren. Beim Durchsuchen mehrerer Einzelzelldatensätze sahen die Forschenden, dass P2Y6 auf stromalen Zellen exprimiert war und in Mausmodellen chronischer Nierenerkrankung weiter anstieg. Messungen in ganzen Nieren bestätigten starke Erhöhungen der P2Y6-Werte in zwei unterschiedlichen Narbungsmodellen. In frischen Nierenschnitten und in kultivierten Nierenfibroblasten, die so konstruiert wurden, dass sie aufleuchten, wenn intrazelluläres Kalzium ansteigt, lösten Zugaben von UDP oder eines P2Y6-aktivierenden Wirkstoffs schnelle Kalziumanstiege aus. Diese Flashes begannen in den langen, dünnen Fortsätzen, die Tubuli umschlingen, und liefen dann in den Zellkörper hinein; sie verschwanden, wenn P2Y6 blockiert oder Kalzium chemisch gebunden wurde. Bei lebenden Mäusen zeigte hochaufgelöste intravitale Mikroskopie, dass Fibroblasten um Tubuli häufige, unregelmäßige Kalziumaktivität aufweisen, die bei Tubulusschädigung dramatisch zunimmt, während die Tubuluszellen selbst still werden.
Von kurzen Signalen zu dauerhaften Narben
Kalziumausbrüche innerhalb einer Zelle sind nicht nur Feuerwerk; sie können das Verhalten umprogrammieren. Wurden Fibroblasten in Kultur einem P2Y6-aktivierenden Stoff ausgesetzt, vermehrten sie sich schneller, krochen aktiver und schalteten Gene ein, die mit einem aggressiveren „Myofibroblasten“-Zustand assoziiert sind. Diese Gene kodieren Proteine wie Fibronectin, Vimentin und Kollagen, die direkt zur Narbenbildung beitragen. Die Blockade von P2Y6 oder das Verhindern von Kalziumanstiegen beseitigte diese Veränderungen, und das Herunterregulieren des Rezeptorgens dämpfte die Reaktion. In Mäusen zeigten zwei verschiedene Formen der Nierenschädigung — Harnleiterverlegung und Folsäurenephropathie — dasselbe Muster: verletzte Nieren hatten mehr proliferierende Fibroblasten, mehr Myofibroblastenmarker, mehr Kollagen und größere Fibroseflächen.
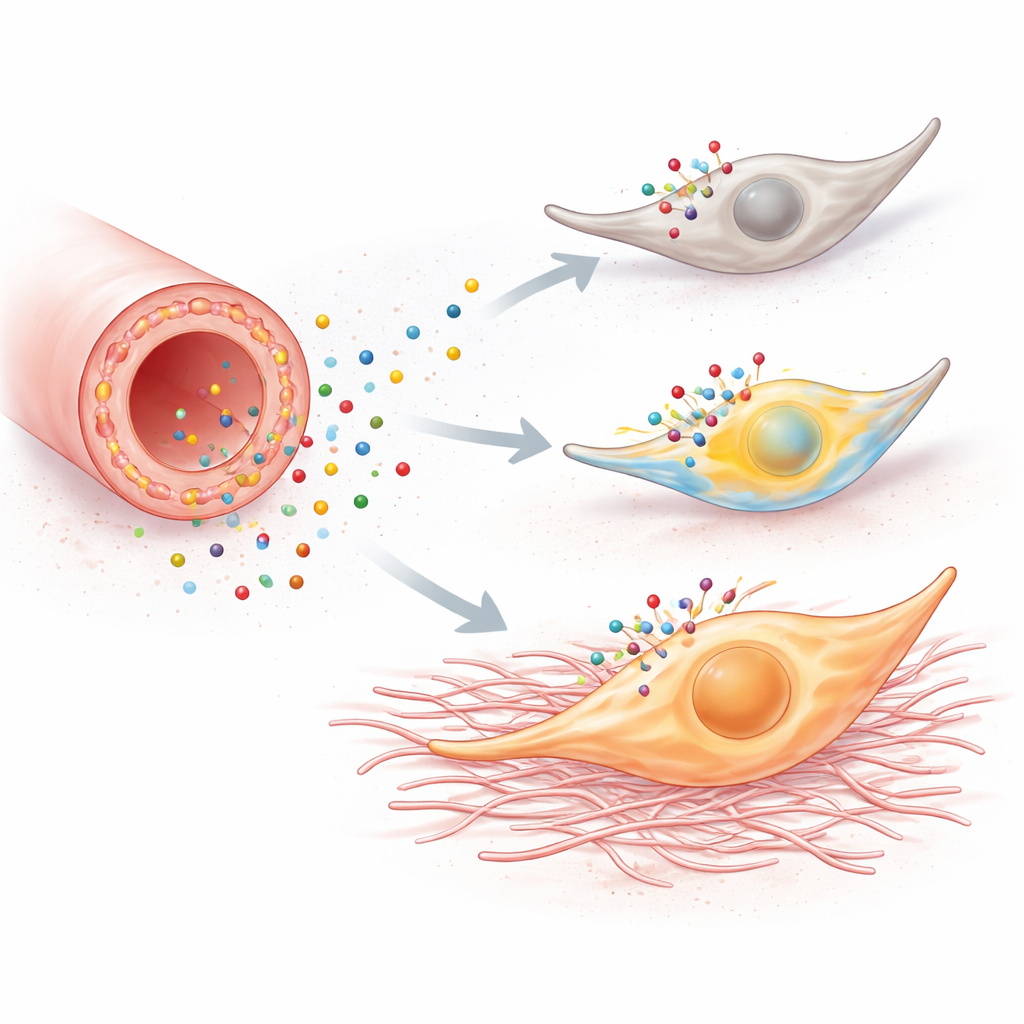
Die Lautstärke schädlicher Signale herunterdrehen
Um zu prüfen, ob dieser Signalweg nicht nur vorhanden, sondern tatsächlich schädlich ist, entfernten die Forschenden entweder P2Y6 genetisch oder blockierten den Rezeptor pharmakologisch. Mäuse ohne diesen Rezeptor entwickelten nach Harnleiterverlegung oder Folsäureschädigung weniger Nierenfibrose: Ihre Fibroblasten teilten sich weniger, lagerten weniger faserreiche Matrix ab und rekrutierten weniger entzündliche Zellen. Blutwerte zeigten, dass diese Knockout-Tiere außerdem eine bessere Filterfunktion der Niere beibehielten. Die Behandlung normaler Mäuse mit einem P2Y6-blockierenden Wirkstoff brachte vergleichbaren Schutz, einschließlich gedämpfter Kalziumaktivität in Fibroblasten und verringerter Vernarbung, wenngleich Verbesserungen in Blutparametern variabler ausfielen.
Was das für künftige Therapien bedeutet
Insgesamt zeigt die Arbeit eine einfache, aber wirkungsvolle Ereigniskette. Wenn Nierentubuluszellen verletzt werden, ändern sie ihre interne Chemie und setzen UDP in das umliegende Gewebe frei. Benachbarte Fibroblasten erkennen dieses Molekül über ihre P2Y6-Rezeptoren, antworten mit intrazellulären Kalziumausbrüchen und schalten dann in einen narbenbildenden Modus um — sie vermehren sich, wandern und lagern Kollagen ab. Das Unterbrechen dieses pyrimidinbasierten Kalziumsignals, besonders am Schritt des P2Y6, mildert die Fibrose in mehreren Mausmodellen deutlich. Für Patientinnen und Patienten deutet das auf ein neues Wirkziel hin: Wirkstoffe, die P2Y6 in der Niere selektiv blockieren, könnten helfen, die Verbindung zwischen alltäglichen Nierenschäden und der langsamen, irreversiblen Vernarbung, die zur chronischen Nierenerkrankung führt, zu durchbrechen.
Zitation: Figurek, A., Jankovic, N., Kollar, S. et al. Pyrimidinergic calcium signaling links tubular metabolism to fibrosis in kidney disease. Nat Commun 17, 3004 (2026). https://doi.org/10.1038/s41467-026-69602-x
Schlüsselwörter: chronische Nierenerkrankung, renale Fibrose, Fibroblastensignalgebung, Pyrimidinstoffwechsel, P2Y6-Rezeptor