Clear Sky Science · de
Organokatalysierte Bottom-up-Bildung von Protocells
Von einfachen Chemikalien zu zellähnlichen Tropfen
Wie konnte leblose Chemie auf der frühen Erde erstmals etwas hervorbringen, das wie eine Zelle aussah und sich so verhielt? Diese Studie untersucht einen überraschend einfachen Weg: Aus kleinen, leicht verfügbaren Molekülen kann ein einzelnes Reaktionsnetzwerk seifenähnliche Lipide erzeugen, die sich spontan zu mikroskopischen Tröpfchen zusammenlagern und schließlich zu Protocells — zellähnlichen Kompartimenten — werden, die die ersten Schritte Richtung Leben geschützt haben könnten.
Warum Kompartimente für Leben wichtig sind
Leben beruht darauf, „innen“ von „außen“ zu trennen. Moderne Zellen verwenden Membranen — dünne Hüllen, die größtenteils aus fettartigen Molekülen bestehen —, um nützliche Chemikalien einzuschließen und zu konzentrieren und schädliche fernzuhalten. Jahrzehntelang haben Forscher zum Ursprung des Lebens dies mit fertig hergestellten Fettsäuren oder Phospholipiden nachgebaut und Hohlblasen, sogenannte Vesikel, erzeugt. Dadurch bleibt jedoch eine zentrale Frage offen: Konnte die Chemie der frühen Erde sowohl die membranbildenden Moleküle als auch die primitiven Kompartimente in einem kontinuierlichen Prozess erzeugen, ohne von bereits fertigen Lipiden auszugehen?
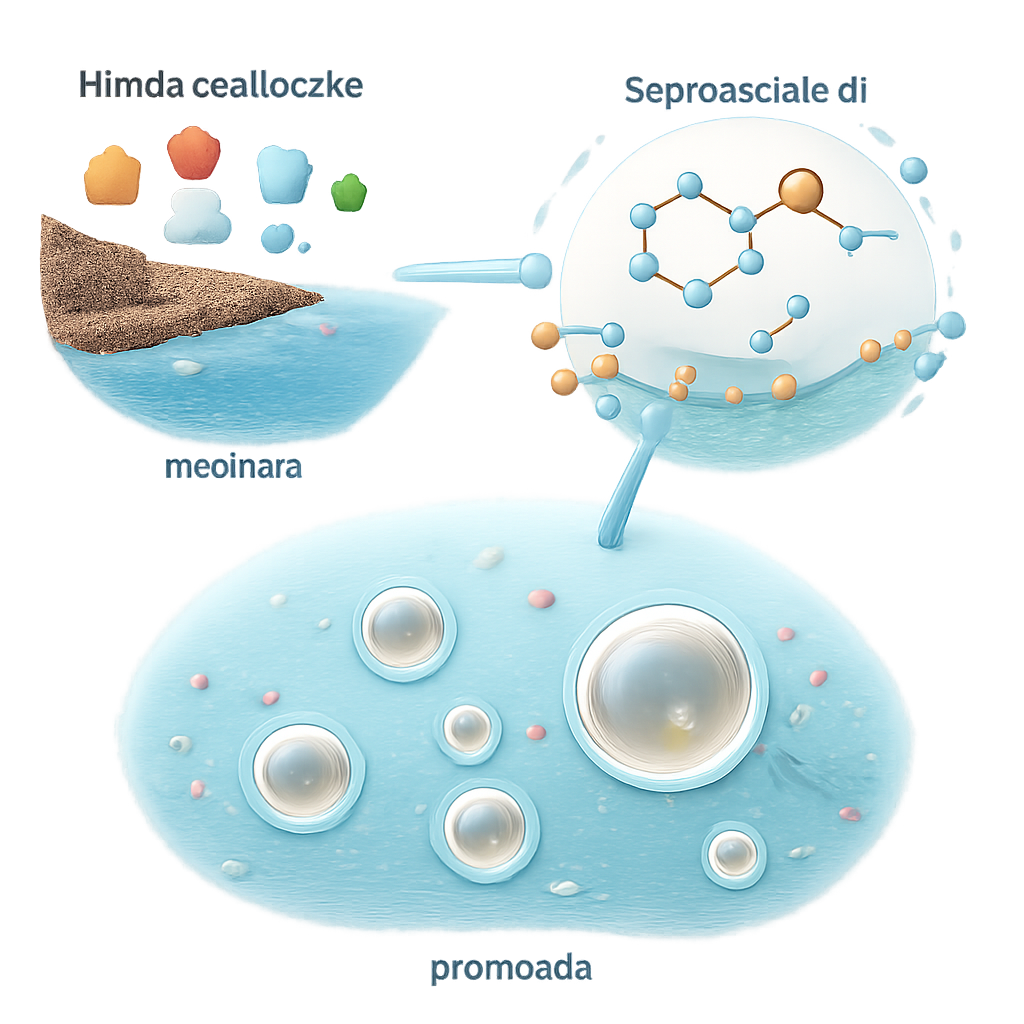
Lipide von Grund auf aufbauen
Die Autoren beschreiben einen Bottom-up-Weg, der bei Acetaldehyd beginnt, einem kleinen, plausiblen Molekül der frühen Erde, das aus Kohlendioxid durch Minerale in vulkanischem Material oder Meteoriten entstehen kann. In schwach saurem Wasser setzen sie einen einfachen schwefelhaltigen organischen Katalysator ein, das Imidazolidin-4-thion. Dieser Katalysator verknüpft Acetaldehyd-Einheiten schrittweise zu sich wiederholenden Mustern und baut so längere Kohlenstoffketten mit einigen Sauerstoffatomen auf. Mit fortschreitender Reaktion wird Wasser aus diesen Ketten entfernt, wodurch sie zunehmend öliger, lipidähnlicher werden und Längen von bis zu etwa 20 Kohlenstoffatomen erreichen — derselbe Größenbereich, der auch von modernen biologischen Membranen bevorzugt wird.
Katalysatoren, die sich beim Arbeiten verändern
Eine auffällige Wendung ist, dass der Katalysator selbst kein passiver Zuschauer ist. Die neuen, lipidähnlichen Aldehyde können sich chemisch an den Katalysator anlagern und dessen Struktur neu ordnen. Der Katalysator tauscht sozusagen seine Seitenketten gegen Produkte aus, die er gerade erzeugt hat, und erzeugt eine Familie verwandter Katalysatormoleküle mit unterschiedlichen Resten. Diese modifizierten Versionen bleiben aktiv und können weiter beeinflussen, welche Produkte als Nächstes entstehen. Das System verhält sich damit ein Stück weit wie eine primitive Form molekularer Evolution: Das Reaktionsnetzwerk erzeugt ein Gemisch von Katalysatoren, von denen einige besser darauf abgestimmt sind, den Prozess unter bestimmten pH-, Temperatur- und Salzbedingungen fortzuführen, die den frühen Ozeanen ähneln.
Spontane Bildung von Protocells
Mit zunehmender Anreicherung lipidähnlicher Moleküle trübt sich das Reaktionsgemisch. Mikroskopie, dynamische Lichtstreuung und Kryo-Elektronenmikroskopie zeigen, dass winzige Tröpfchen zuerst erscheinen, dann wachsen und in der Größe von etwa 10 Nanometern bis zu mehreren Mikrometern diversifizieren. Anfangs verhalten sich die Tröpfchen wie Öltropfen im Wasser, wobei die Katalysatormoleküle die Oberfläche auskleiden, sodass ihre wasserliebenden Köpfe nach außen und die öligen Schwänze nach innen zeigen. Mit fortschreitender Reaktion entfernt die Chemie beständig Wasser aus der öligen Phase und erzeugt zusätzliches Wasser, das in kleinen Taschen getrennt austritt. Diese inneren Wassertropfen verschmelzen und drücken sich manchmal nach außen, wodurch der Öltropfen zu einer Struktur mit einer dünnen, lipidreichen Grenze wird, die ein inneres wässriges Kompartiment umschließt — im Wesentlichen ein Protocell. Die Membran bleibt durchlässig genug, um fluoreszierende Farbstoffe hineinzulassen und, analog, andere kleine organische Moleküle, sodass diese sich im Inneren anreichern können.
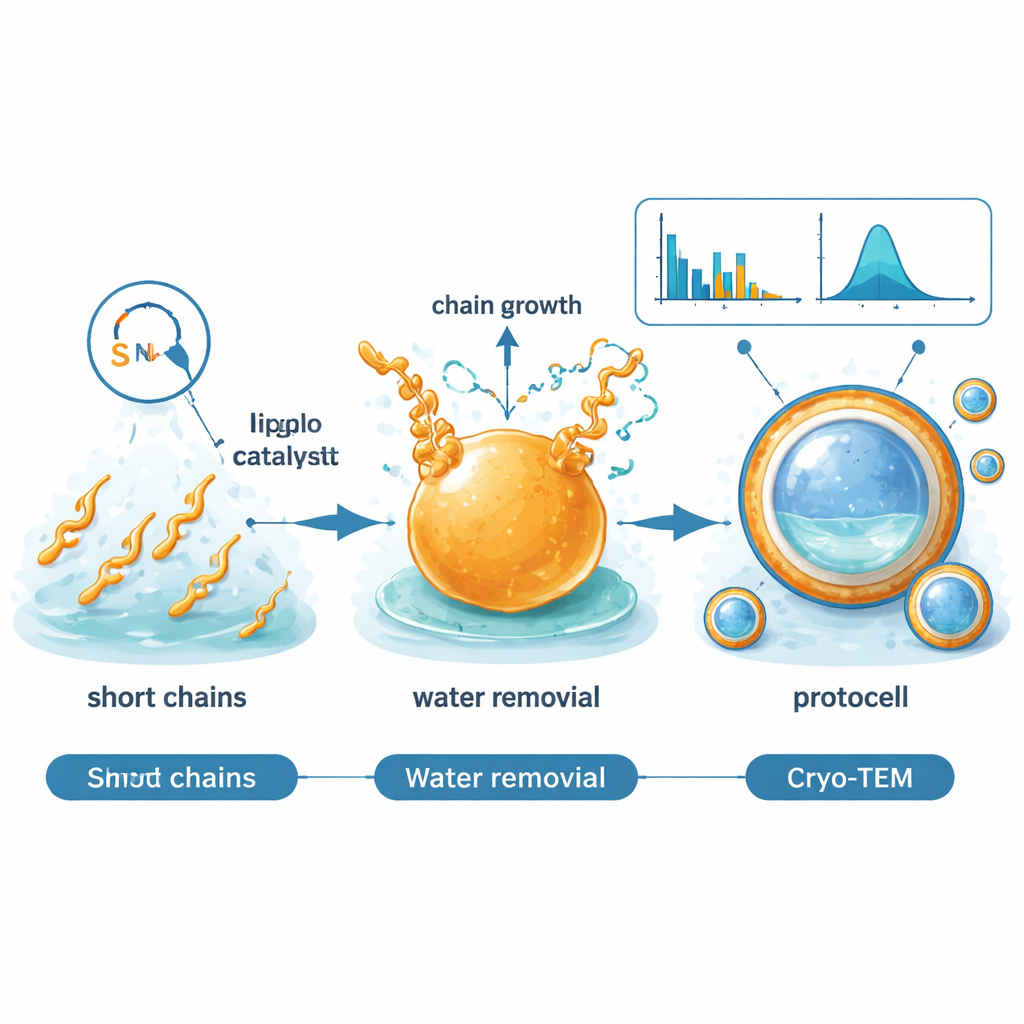
Robust unter Bedingungen der frühen Erde
Das Team prüfte, wie stabil diese Protocells bei unterschiedlichen pH-Werten, Temperaturen und Salzgemischen sind, die primitive Meere nachahmen sollen. Das organokatalytische System toleriert solche Variationen nicht nur, sondern profitiert teilweise sogar davon: Bestimmte Salze beschleunigen die Reaktion, und leicht saure Bedingungen begünstigen sowohl den Kettenaufbau als auch die Wasserentfernung. Anders als viele moderne Fettsäuremembranen, die in Gegenwart häufiger Metallionen auseinanderfallen, bleiben diese Protocell-Strukturen in Gegenwart von Magnesium und Calcium stabil. Einmal gebildet, können sie wachsen und in der Zahl zunehmen, während mehr lipidähnliches Material entsteht und gleichzeitig organische Verbindungen in ihren Innenräumen konzentriert werden.
Was das für den Ursprung des Lebens bedeutet
Für Nichtfachleute lautet die Hauptbotschaft: Man kann mit sehr einfachen Chemikalien anfangen, sie milden Bedingungen aussetzen und trotzdem winzige, zellähnliche Behälter erhalten, die ihre innere Chemie organisieren und anreichern. Diese Arbeit legt einen realistischen Weg nahe, wie die frühe Umgebung der Erde sowohl die Bausteine von Membranen als auch die ersten Protocells gleichzeitig erzeugt haben könnte, wobei kleine, plausible Katalysatoren statt komplexer Enzyme wirken. Solche selbstassemblierenden, katalytisch aktiven Protocells bieten eine natürliche Bühne, auf der sich komplexere Moleküle — etwa RNA — bilden, ansammeln und schließlich die Rollen übernehmen könnten, die wir heute mit lebenden Zellen verbinden.
Zitation: Ebeling, M.S.R., Berninghausen, O., Nguyen, K.H. et al. Organocatalyzed bottom-up formation of protocells. Nat Commun 17, 1983 (2026). https://doi.org/10.1038/s41467-026-69597-5
Schlüsselwörter: Ursprung des Lebens, Protocells, präbiotische Chemie, Selbstassemblierung, Organokatalyse