Clear Sky Science · de
Doppelte Rekrutierung von zwei CCM2-Molekülen an KRIT1 unterdrückt die KLF4-Expression
Warum die Blutgefäße im Gehirn sorgfältig kontrolliert werden müssen
Die Blutgefäße im Gehirn müssen ein sensibles Gleichgewicht halten: Sie müssen stabil genug sein, um Lecks zu vermeiden, aber gleichzeitig flexibel genug, um auf die Bedürfnisse des Körpers zu reagieren. Versagt dieses Gleichgewicht, können sich zerebrale kavernöse Malformationen entwickeln — Ansammlungen fragiler, blasenartiger Gefäße, die bluten und Anfälle oder Schlaganfälle auslösen können. Diese Studie enthüllt einen zuvor unbekannten molekularen „Handschlag“ zwischen drei Proteinen, der hilft, die Stabilität der Gehirngefäße zu bewahren, und zeigt, wie das Zerbrechen dieses Zusammenspiels Krankheit fördern kann.
Die Wächter der Gefäßgesundheit
Die Zellen, die Blutgefäße auskleiden, verlassen sich auf Hauptschalter, genannt KLF2 und KLF4, um Gene zu steuern, die die Stärke und Identität der Gefäße erhalten. Werden diese Schalter übermäßig aktiviert, werden Gefäße abnormal und anfällig für Schäden. Zwei weitere Proteine, KRIT1 und CCM2, sind dafür bekannt, dieses System zu bewachen. Menschen, die fehlerhafte Versionen eines dieser Proteine erben, haben ein hohes Risiko für zerebrale kavernöse Malformationen. Bislang war jedoch unklar, wie KRIT1 und CCM2 genau zusammenarbeiten, um KLF4 in Schach zu halten.
Ein überraschendes Trio
Die Forschenden verwendeten im Labor gezüchtete humane endothelähnliche Zellen und verringerten gezielt die Menge an CCM2 oder KRIT1 mit genetischen Werkzeugen. Wurde eines der beiden Proteine reduziert, stieg der KLF4-Spiegel deutlich an, wie es auch in Tiermodellen und bei Patientinnen und Patienten beobachtet wird. Die Wiederherstellung von normalem CCM2 oder KRIT1 senkte KLF4 wieder — allerdings nur, wenn die wieder eingeführten Proteine noch aneinander binden konnten. Durch gezielte Veränderungen in den Regionen, in denen CCM2 und KRIT1 interagieren, zeigte das Team, dass dieser physische Kontakt für die Verhinderung des KLF4-Anstiegs unerlässlich ist. Diese Experimente verorten die Partnerschaft von KRIT1 und CCM2 fest im Zentrum des Kontrollsystems für diesen kraftvollen Transkriptionsfaktor.
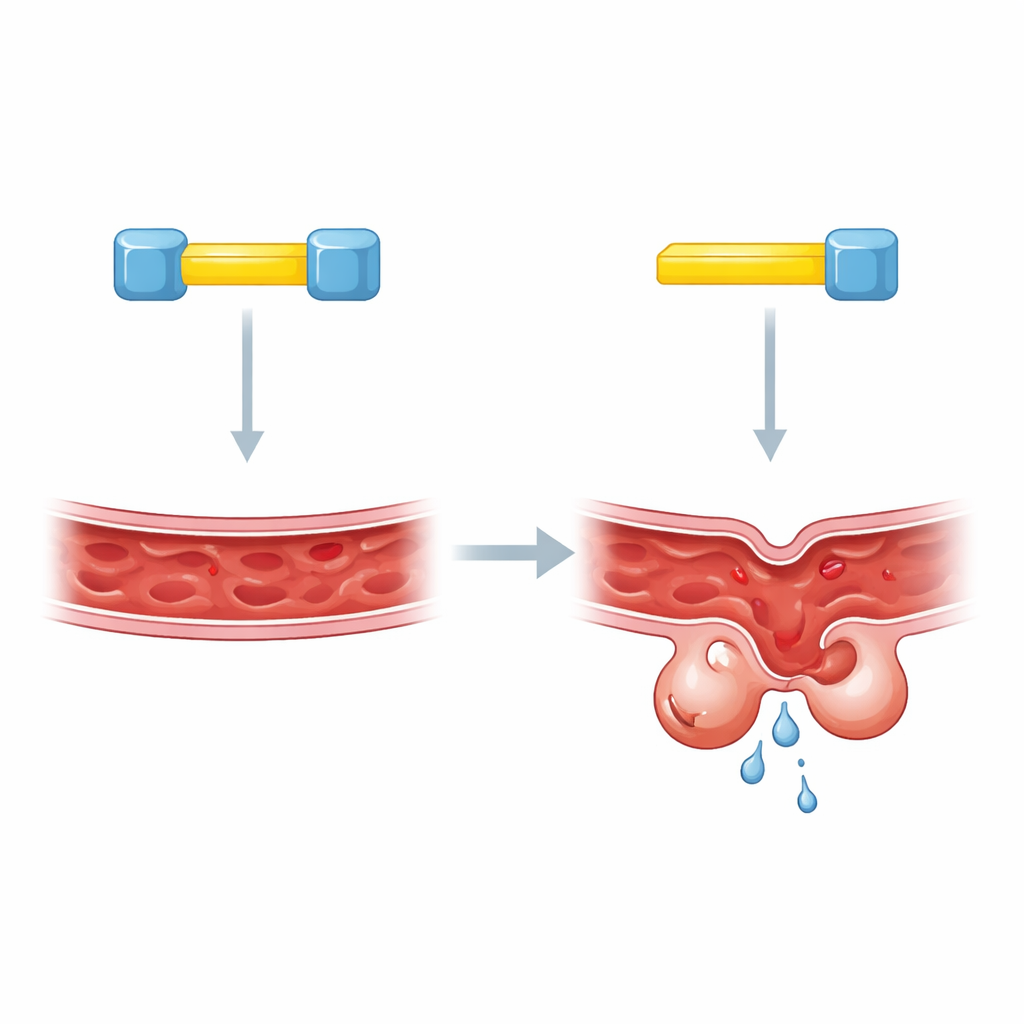
Zwei Schlösser an einem Schlüssel
Um tiefer zu bohren, konzentrierten sich die Autorinnen und Autoren auf kurze Segmente innerhalb von KRIT1, die als molekulare Andockstellen dienen. Frühere Arbeiten legten nahe, dass CCM2 an einer dieser Stellen an KRIT1 bindet, doch verschiedene Methoden hatten widersprüchliche Antworten darüber geliefert, welche genau gemeint ist. Die neue Studie zeigt, dass die Verwirrung daher rührte, dass das wahre Bild komplexer ist: KRIT1 trägt zwei nahe beieinanderliegende Andocksegmente, und beide sind erforderlich. Wird eines der Segmente gestört, bleiben die KLF4-Werte ungewöhnlich hoch, so als fehle KRIT1 ganz. Biochemische Tests in konstruierten Zellen zeigten, dass ein einzelnes KRIT1-Protein gleichzeitig zwei separate CCM2-Moleküle verbinden kann, was auf eine unerwartete Drei-Teil-Zusammenlagerung hindeutet.
Den molekularen Klammermechanismus im Detail sehen
Das Team reinigte dann die relevanten Stücke von CCM2 und KRIT1 und untersuchte, wie sie sich in Lösung und in Kristallen zusammensetzen. Messungen der Masse des Komplexes zeigten, dass zwei Kopien einer Schlüsselregion von CCM2 an einen einzelnen Streifen von KRIT1 binden, der die beiden Andockstellen trägt. Hochauflösende Strukturaufnahmen bestätigten dieses 2:1-Verhältnis: Ein ausgedehntes KRIT1-Peptid fädelt sich zwischen zwei CCM2-Domänen, wobei jede Andockstelle in einer ähnlichen Tasche eines unterschiedlichen CCM2-Moleküls liegt. Ein kurzes helikales Segment zwischen den Andockstellen hilft, die beiden CCM2-Domänen nebeneinander zu positionieren und schafft so eine enge, klammerartige Struktur. Diese Form der doppelten Einbindung — zwei Bindedomänen, die an Tandemstellen eines Partners ansetzen — wurde für diese Familie von Proteinmodulen zuvor nicht beobachtet.
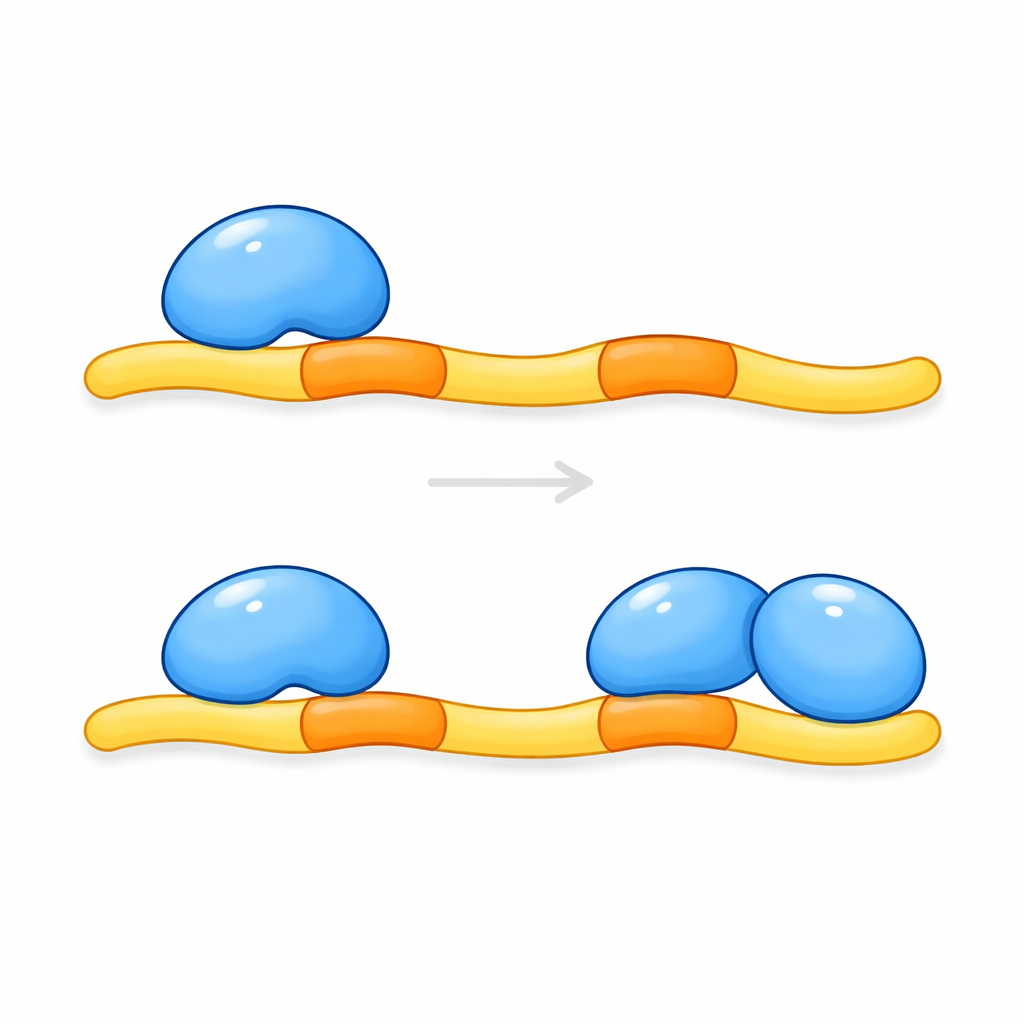
Folgen für Gehirnkrankheiten und darüber hinaus
Diese Ergebnisse zeigen, dass KRIT1 nicht einfach ein CCM2-Molekül bindet; vielmehr fungiert es als Gerüst, das ein Paar von CCM2-Proteinen rekrutiert. Nur wenn beide Andockstellen auf KRIT1 besetzt sind, kann der Komplex die KLF4-Produktion angemessen dämpfen und damit helfen, das Wachstum fragiler Gefäße zu verhindern. Mutationen in KRIT1, die eine der Andockstellen stören, dürften diese schützende Klammer schwächen und könnten einige erbliche Formen zerebraler kavernöser Malformationen erklären. Da viele andere menschliche Proteine ähnliche doppelte Andockmotive tragen, deutet diese Studie zudem auf ein allgemeineres Prinzip hin: Die doppelte Bindung durch Paare verwandter Domänen könnte eine verbreitete Strategie sein, mit der Zellen Signalnetzwerke feinjustieren. Das Verständnis dieser Drei-Partner-Interaktion könnte schließlich dazu beitragen, Strategien zu entwickeln, um die Blutgefäße bei Menschen mit Blutungsrisiko im Gehirn zu stabilisieren.
Zitation: Huet-Calderwood, C., Fisher, O.S., Das, S. et al. Dual recruitment of two CCM2 molecules to KRIT1 suppresses KLF4 expression. Nat Commun 17, 2719 (2026). https://doi.org/10.1038/s41467-026-69595-7
Schlüsselwörter: zerebrale kavernöse Malformationen, Endothelzellen, KRIT1, CCM2, KLF4