Clear Sky Science · de
Kontrastfreie Identifizierung des Blut‑Hirn‑Schranken‑Status bei Gliomen mittels generativer Diffusions‑KI und nicht‑kontrastmittelgestützter MRT
Warum das für Patientinnen und Patienten mit Hirntumoren wichtig ist
Menschen mit Hirntumoren erhalten routinemäßig MRT‑Untersuchungen, und viele bekommen zusätzlich ein injiziertes Kontrastmittel, damit Ärztinnen und Ärzte sehen können, ob die schützende Blut‑Hirn‑Schranke geschädigt ist. Diese Information beeinflusst Operationen, Strahlentherapie und Prognose – das Kontrastmittel kann jedoch Risiken bergen, Zeit und Kosten erhöhen und ist nicht immer verfügbar. Diese Studie stellt ein System der künstlichen Intelligenz (KI) vor, das aus Routine‑MRTs ohne Kontrast virtuell die fehlenden Kontrastbilder rekonstruiert und es so ermöglicht, den Status der Blut‑Hirn‑Schranke ohne Injektion eines Kontrastmittels abzuleiten.
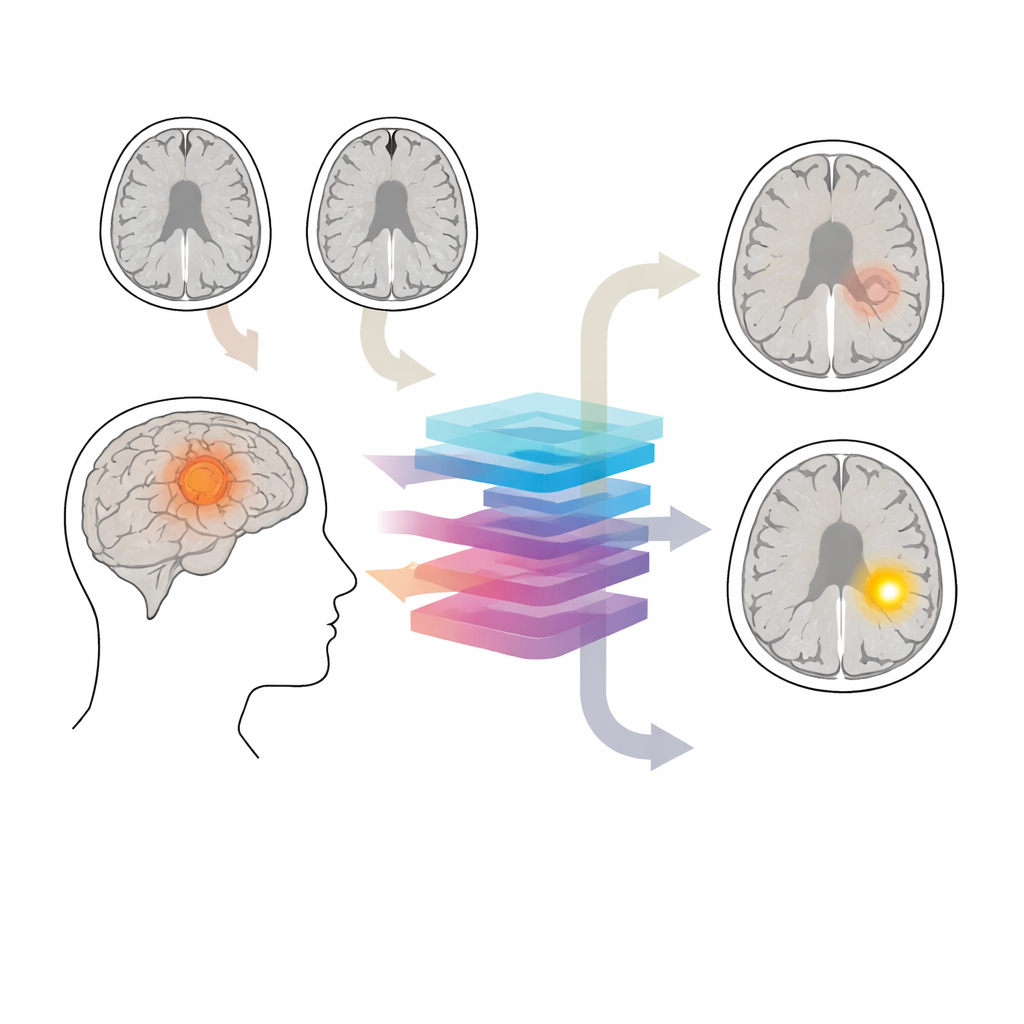
Das schützende Tor des Gehirns
Die Blut‑Hirn‑Schranke wirkt wie ein mikroskopischer Filter um die Blutgefäße im Gehirn und lässt nur sehr kleine Moleküle passieren. Bei vielen Gliomen wird diese Barriere durchlässig. In standardmäßigen Kontrast‑MRTs leuchten undichte Bereiche nach der Injektion auf, während intakte Regionen dunkel bleiben. Diese Muster beeinflussen, wie aggressiv ein Tumor behandelt wird, und helfen zu bestimmen, was operativ entfernt oder bestrahlt werden sollte. Kontrastaufnahmen werden jedoch manchmal ausgelassen – etwa bei frühen Abklärungen oder in der langfristigen Nachsorge langsam wachsender Tumoren – und einige Patientinnen und Patienten sollten Kontrastmittel ganz meiden wegen Nierenerkrankungen, allergischen Reaktionen oder Bedenken hinsichtlich Gadolinium‑Ablagerungen im Gehirn.
Aus gewöhnlichen Aufnahmen virtuelle Kontraste erzeugen
Die Autorinnen und Autoren fragten, ob nicht‑kontrastierte MRTs, die ohnehin häufig erhoben werden, genug subtile Informationen enthalten, damit eine KI rekonstruieren kann, was eine Kontrastaufnahme gezeigt hätte. Sie konzentrierten sich auf zwei gängige Sequenzen: T1 und T2‑FLAIR. Diese Sequenzen zeigen nicht direkt Leckagen der Blut‑Hirn‑Schranke, erfassen aber Tumorstruktur, umgebende Schwellungen und Gewebeschäden, die häufig mit einem Barriereschaden einhergehen. Das Team entwickelte ein System namens CBSI, das zunächst synthetische kontrastverstärkte Bilder aus diesen nicht‑kontrastierten Scans erzeugt und diese zusammen mit den Originalbildern verwendet, um zu entscheiden, ob die Schranke bei jedem Gliom intakt oder gestört ist.
Wie das neue KI‑System funktioniert
Im Kern von CBSI steht ein Diffusionsmodell — eine Form der KI, die von verrauschten Bildern ausgeht und diese iterativ „entzerrt“, bis realistische Bilder entstehen. Es lernt hier, nicht‑kontrastierte Eingaben in zwei alternative virtuelle Kontrastbilder zu verwandeln: eines unter der Annahme einer intakten Schranke und eines unter der Annahme einer undichten Schranke. Ein Steuerungsmechanismus gibt dem Modell vor, welches Enhancements‑Muster angestrebt werden soll, und ein zusätzlicher Segmentierungsschritt hilft, die Aufmerksamkeit besonders auf die Tumorregion zu richten. In einer zweiten Stufe vergleicht ein separates Netzwerk die beiden synthetischen Ergebnisse für jede Patientin bzw. jeden Patienten und bewertet, welches Ergebnis konsistenter mit den ursprünglichen MRT‑Daten ist. Diese Entscheidung wird dann in den vorhergesagten Status der Blut‑Hirn‑Schranke übersetzt.
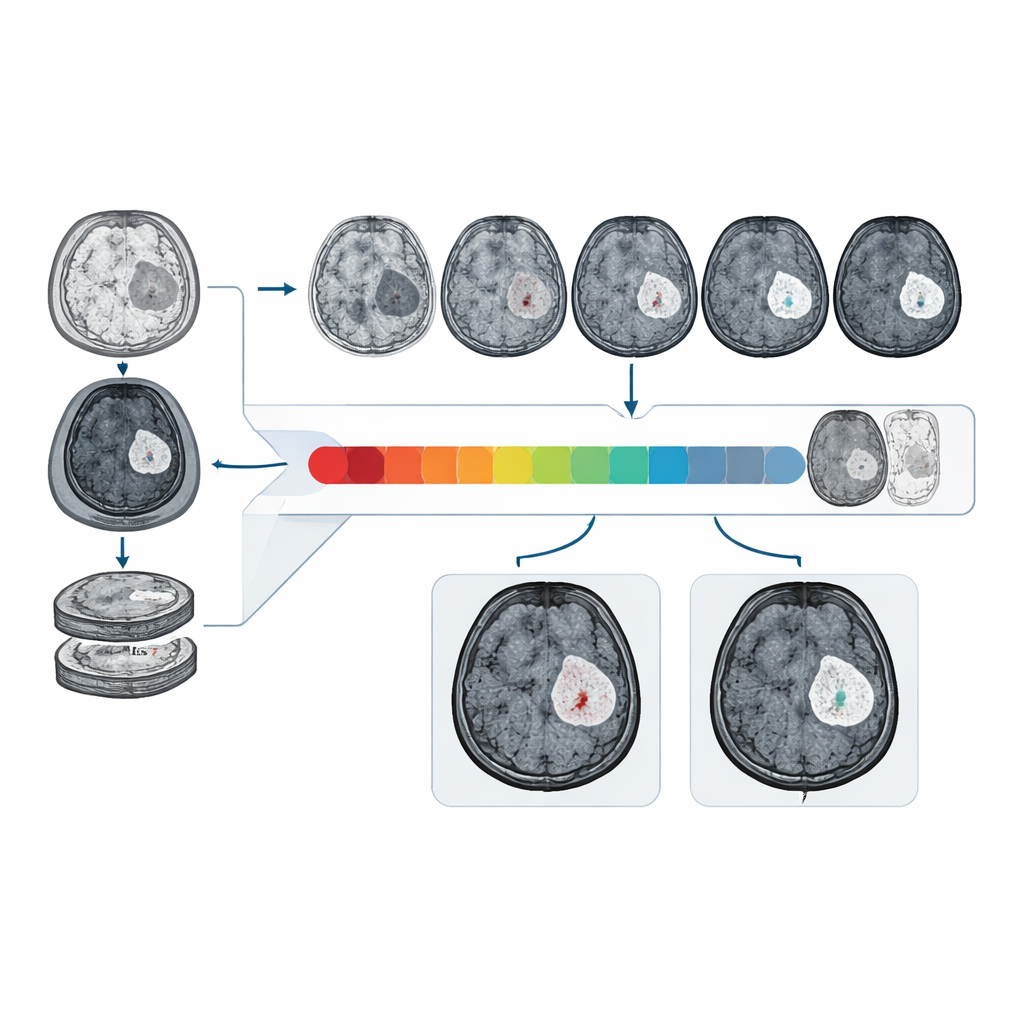
Wie gut es an realen und vielfältigen Daten funktioniert
Die Forschenden trainierten und testeten CBSI an MRT‑Daten von 1.535 Gliompatientinnen und ‑patienten, die an mehreren Kliniken und aus internationalen öffentlichen Datensätzen gesammelt wurden. In einem externen klinischen Testdatensatz unterschied CBSI intakte von gestörten Schranken mit einer Fläche unter der Kurve von etwa 81 %, deutlich besser als Modelle, die nur auf nicht‑kontrastierten Bildern beruhten, und in Reichweite der Leistung von Modellen, die echte Kontrastaufnahmen nutzten. Radiologinnen und Radiologen bewerteten bei randomisiert gemischten echten und synthetischen Kontrastbildern des Systems über 90 % der synthetischen Bilder als diagnostisch hochwertig, und ihre Fähigkeit, Kontrastverstärkung auf synthetischen Bildern zu erkennen, war ähnlich wie bei realen Aufnahmen.
Vorteile für die Behandlungsplanung und künftige Versorgung
Weil die synthetischen Kontrastbilder von CBSI Tumordetails und Enhancements‑Muster abbilden, verbesserten sie auch nachgelagerte Aufgaben wie die Abgrenzung von Tumorrändern und die Abschätzung des Tumorgrades – beides hängt stark vom Verhalten der Blut‑Hirn‑Schranke ab. Die Methode generalisierte gut auf unterschiedliche Scanner, Bildgebungsprotokolle und Patientengruppen, einschließlich Daten aus Subsahara‑Afrika und größeren internationalen Kohorten. Die Autorinnen und Autoren betonen zwar, dass jedes Deep‑Learning‑System ein statistisches Werkzeug und kein direkter Blick in die Biologie bleibt, doch deuten ihre Ergebnisse darauf hin, dass virtuelle Kontrastbildgebung die Abhängigkeit von injizierten Agenzien verringern könnte, insbesondere bei vulnerablen Patientinnen und Patienten oder in Umgebungen, in denen Kontrastaufnahmen schwer zu beschaffen sind. Praktisch könnte dieser KI‑Ansatz es Ärztinnen und Ärzten ermöglichen, aus den bereits vorhandenen Scans schlüsselinformative, therapieprägenden Informationen über die Blut‑Hirn‑Schranke zu gewinnen – ohne einen zusätzlichen Nadelstich.
Zitation: Zheng, K., Zhang, Y., Shu, H. et al. Contrast-free identification of glioma blood-brain barrier status via generative diffusion AI and non-contrast MRI. Nat Commun 17, 2162 (2026). https://doi.org/10.1038/s41467-026-69578-8
Schlüsselwörter: Gliom, Blut‑Hirn‑Schranke, Gehirn‑MRT, medizinische Bildgebungs‑KI, kontrastfreie Bildgebung