Clear Sky Science · de
Nanobody-basierte IgG hemmen gleichzeitig die allergene und enzymatische Aktivität des dominanten Bienengift‑Allergens
Warum Bienenstich‑Allergien wichtig sind
Für die meisten Menschen ist ein Honigbienenstich schmerzhaft, aber von kurzer Dauer. Bei anderen kann er jedoch eine lebensbedrohliche Reaktion am ganzen Körper auslösen, die als Anaphylaxie bezeichnet wird. Die heute gebräuchliche vorbeugende Behandlung, die Venom‑Immuntherapie, hilft vielen Patientinnen und Patienten, erfordert jedoch Jahre, ist mit häufigen Injektionen verbunden und kann selbst allergische Nebenwirkungen hervorrufen. Diese Studie untersucht einen neuen, gezielteren Ansatz, um Menschen mit lebensgefährlicher Honigbienen‑Allergie zu schützen, indem eine Schlüsselkomponente des Giftes entwaffnet wird, bevor sie Schaden anrichten kann.
Der Hauptstörer im Bienengift
Honigbienen‑Gift ist ein Cocktail aus verschiedenen Molekülen, aber ein Protein, die Phospholipase A2 (auch Api m 1 genannt), sticht hervor. Es ist das dominierende Allergen bei honigbienenallergischen Patienten und kommt bei nahezu allen Betroffenen vor. Api m 1 hat eine doppelte Rolle: Es schädigt Zellmembranen und trägt so zu Schmerz und Entzündung an der Einstichstelle bei, und es ist zugleich ein primäres Ziel für allergieauslösende Antikörper vom Typ IgE. Wenn Api m 1 an IgE bindet, das an Immunzellen wie Mastzellen und Basophilen verankert ist, kann dies eine Kaskade auslösen, die zur plötzlichen Freisetzung entzündungsfördernder Substanzen und in schweren Fällen zur Anaphylaxie führt.
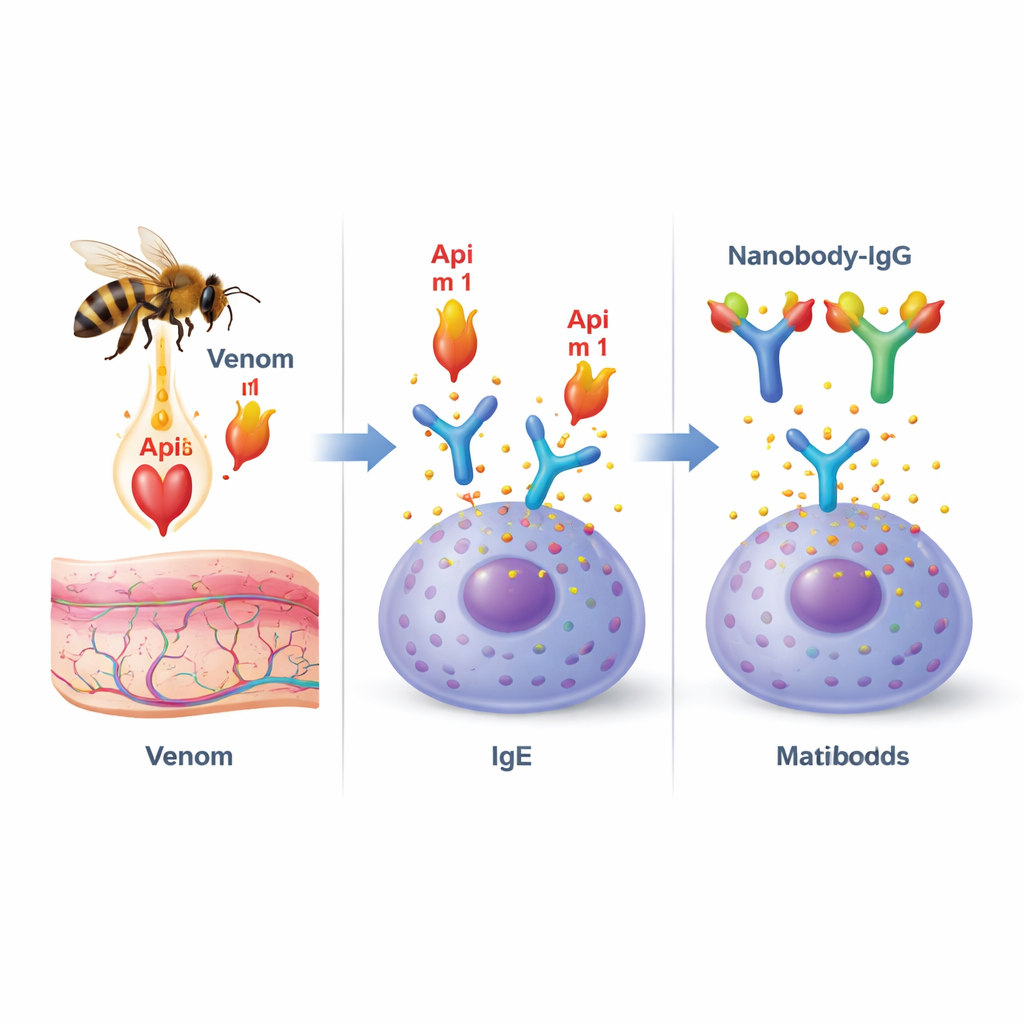
Entwurf winziger Antikörper, die das Allergen blockieren
Die Forschenden setzten auf „Nanobodies“, winzige, stabile Antikörperfragmente, die ursprünglich bei Kameliden entdeckt wurden. Durch ihre geringe Größe und gestreckte Form eignen sie sich besonders gut, in Ritzen und Taschen von Proteinen zu passen. Das Team isolierte Api m 1‑spezifische Nanobodies aus einer Immunbibliothek und wählte zwei herausragende Kandidaten, AM1‑1 und AM1‑4. Detaillierte Strukturuntersuchungen mittels Röntgenkristallographie zeigten, dass diese beiden Nanobodies auf gegenüberliegenden Seiten von Api m 1 ansetzen und sich nicht gegenseitig stören. Ein Nanobody, AM1‑1, sitzt direkt über dem aktiven Zentrum des Enzyms, was darauf hindeutet, dass er die membranschädigende Funktion von Api m 1 blockieren könnte, während AM1‑4 in eine separate Tasche auf der Proteinoberfläche andockt.
Nanobodies in potente Blocker verwandeln
Um diese kleinen Bindemoleküle in langwirksame Wirkstoffe zu verwandeln, fusionierten die Wissenschaftler jede Nanobody mit dem Schwanzteil (Fc‑Region) des menschlichen IgG1 und schufen so größere, antikörperähnliche Moleküle mit verbesserter Stabilität im Blutkreislauf. Sie konstruierten zudem eine „bispezifische“ Variante, die sowohl AM1‑1 als auch AM1‑4 in einem einzigen IgG‑ähnlichen Molekül vereint. Labortests zeigten, dass diese Nanobody‑IgG‑Fusionsproteine mit extrem hoher Affinität an Api m 1 binden und in ihrer Gegenwart die Bindung von IgE aus dem Blut honigbienenallergischer Patientinnen und Patienten an Api m 1 stark reduzieren können. In zellbasierten Assays verringerten sie die Aktivierung von Basophilen, den Immunzellen, die bei exponierten Allergikern normalerweise heftig auf Api m 1 reagieren.
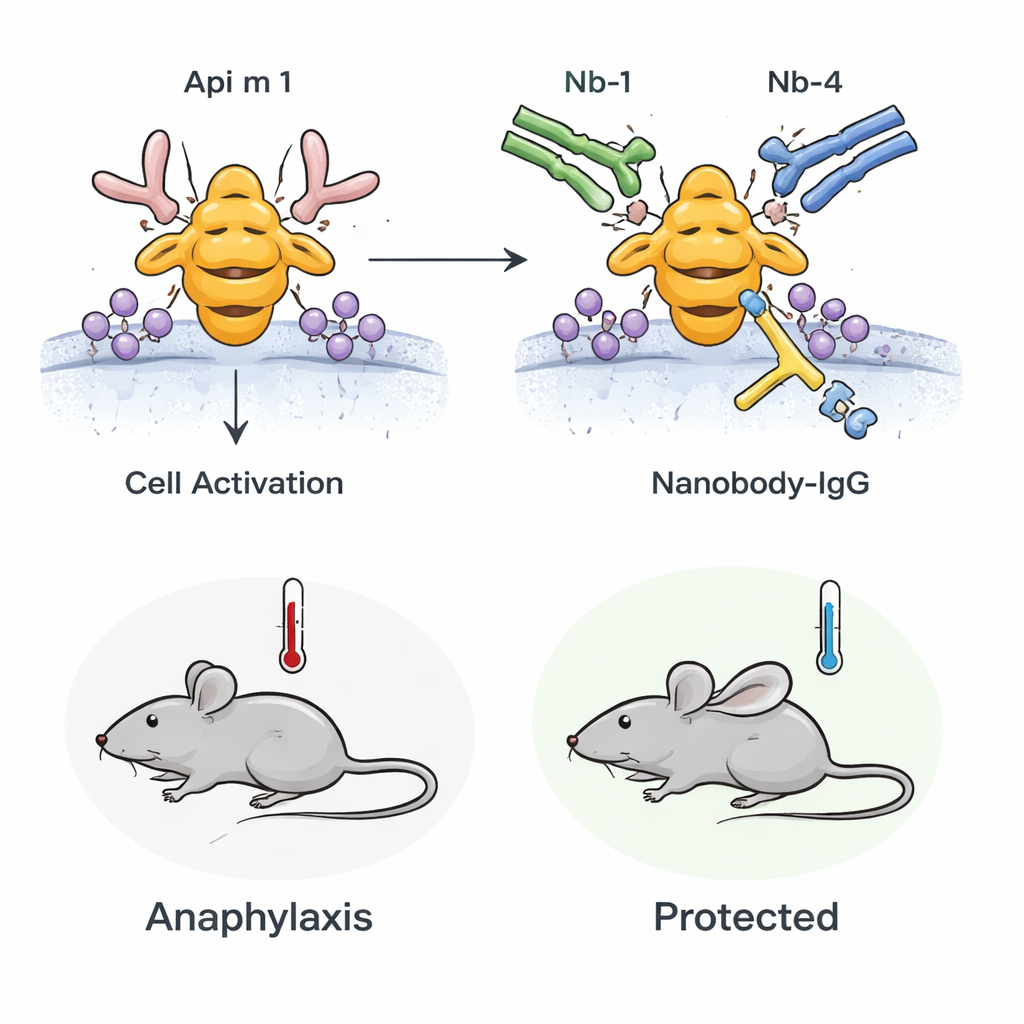
Vom Reagenzglas ins lebende Tier
Als Nächstes prüfte das Team, ob dieser Blockierungseffekt auch in einem lebenden Organismus anhält. Sie verwendeten Mäuse, die auf Bienengift sensibilisiert waren, sodass ihr Immunsystem auf Api m 1 in einer Weise reagierte, die der menschlichen Allergie ähnelt. Wenn diese Mäuse mit Api m 1 herausgefordert wurden, entwickelten sie Anzeichen einer Anaphylaxie, darunter einen Abfall der Körpertemperatur und Marker für die Mastzellaktivierung im Blut. Wurden die Tiere jedoch vorab mit dem bispezifischen Nanobody‑IgG behandelt, waren sowohl der Temperaturabfall als auch die Mastzellaktivierung deutlich reduziert. Dies zeigt, dass bereits vorhandene, hochaffine blockierende Antikörper die systemische allergische Reaktion auf Api m 1 in vivo abschwächen können.
Was das für Menschen mit Bienengiftallergie bedeuten könnte
Zusammengefasst zeigt die Studie, dass sorgfältig konstruierte, nanobody‑basierte IgG‑Moleküle sowohl die allergene als auch die enzymatische Wirkung von Api m 1 blockieren können, dem Hauptverursacher der Honigbienen‑Giftallergie. Für Patientinnen und Patienten eröffnet sich die Möglichkeit einer saisonalen, passiven Immunisierung: Einige Injektionen solcher Antikörper in den Monaten mit erhöhter Stichgefahr könnten vorübergehenden Schutz vor schweren Reaktionen bieten, ohne die lange Verpflichtung und die Risiken der traditionellen Venom‑Immuntherapie. Zwar sind weitere Arbeiten nötig, um den Ansatz auf andere Giftkomponenten auszuweiten und Sicherheit sowie Wirksamkeit beim Menschen zu prüfen, doch bietet die Nanobody‑Strategie einen präzisen neuen Weg, gefährdete Personen vor gefährlichen Bienenstichen zu schützen.
Zitation: Aagaard, J.B., Gandini, R., Ballegaard, AS.R. et al. Nanobody-based IgG simultaneously inhibit the allergenic and enzymatic activity of the dominant honeybee venom allergen. Nat Commun 17, 1814 (2026). https://doi.org/10.1038/s41467-026-69572-0
Schlüsselwörter: Bienengiftallergie, Nanobodies, passive Immuntherapie, Phospholipase A2, Prävention von Anaphylaxie