Clear Sky Science · de
Kooperative Klammer-vermittelte Promotorerkennung durch poxvirale RNA‑Polymerase und ihr TBP/TFIIB‑ähnlicher Partner
Wie ein Virus die Genkontrolle in unseren Zellen umprogrammiert
Poxviren, zu denen auch das historisch für die Pocken verantwortliche Virus zählt, führen ihre gesamte Genexpression im Zytoplasma unserer Zellen aus, fern vom zellulären DNA‑Kontrollzentrum im Zellkern. Dafür bringen sie eine eigene, kompakte „genetische Fabrik“ mit. Diese Studie legt auf atomarer Ebene offen, wie ein solcher Virus, das Vaccinia‑Virus, eine bestimmte Welle seiner Gene mitten in der Infektion einschaltet — mit Hilfe eines unerwarteten, klammerähnlichen Proteins, das zusammen mit der viralen Kopiervorrichtung wirkt.
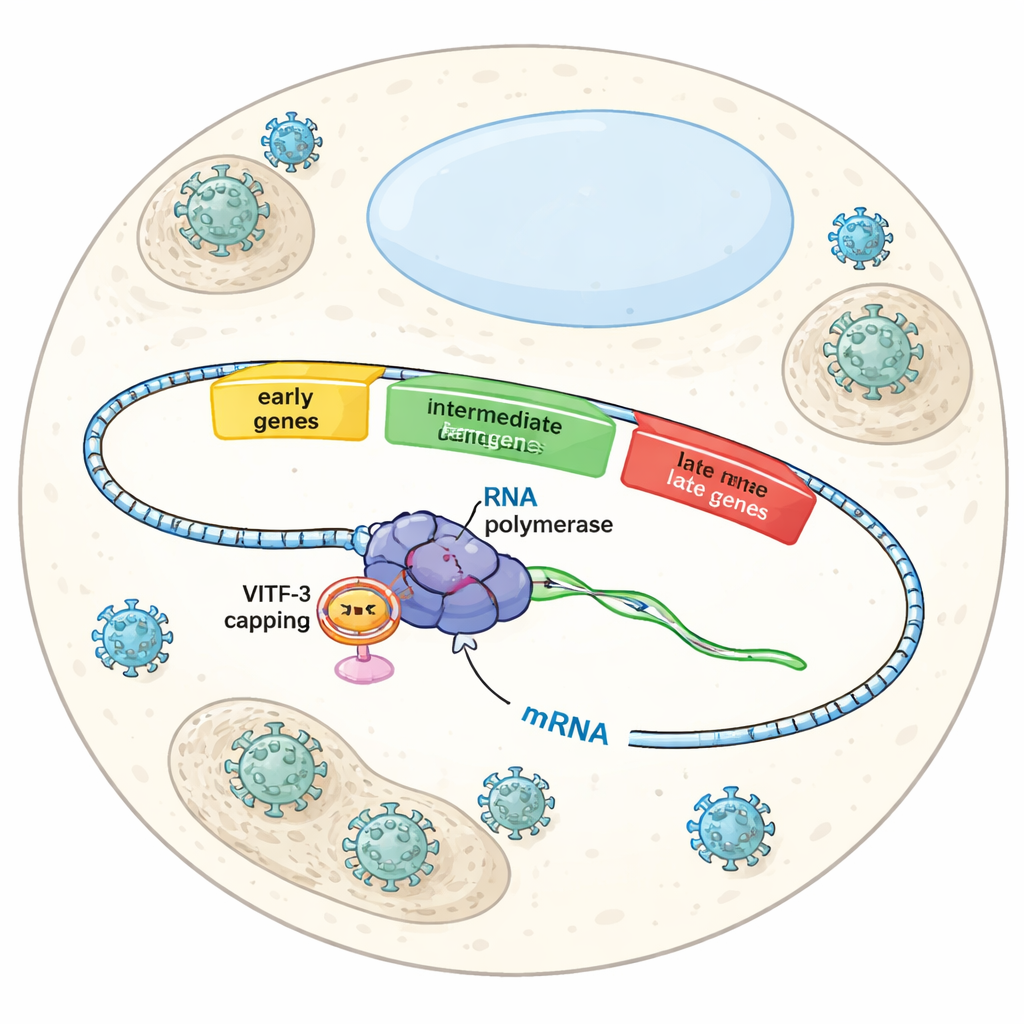
Drei Wellen bei einer viralen Übernahme
Wenn Vaccinia eine Zelle infiziert, schaltet es nicht alle seine Gene zugleich an. Stattdessen folgt es einem zeitlich abgestimmten Drehbuch mit frühen, intermediären und späten Genen. Frühe Gene bereiten die Bedingungen für die virale Replikation vor, intermediäre Gene helfen beim Aufbau der Maschinerie zur Herstellung neuer Viruspartikel, und späte Gene vervollständigen Zusammenbau und Verpackung. Jede Welle hängt von derselben viralen RNA‑Polymerase ab — dem Enzym, das DNA abliest, um RNA zu erzeugen —, aber unterschiedliche Helferfaktoren sagen der Polymerase, welche Genklasse in welchem Stadium aktiviert werden soll. Bisher war die Kontrolle früher Gene relativ gut verstanden; wie der Virus jedoch spezifisch intermediäre Gene erkennt und aktiviert, blieb unbekannt.
Ein ringförmiger Helfer, der einen Partner braucht
Die Forscher konzentrierten sich auf ein zweiteiliges Protein namens VITF‑3, das für das Anschalten intermediärer Gene erforderlich ist. Viele Organismen, einschließlich des Menschen, benutzen ein Proteinduo namens TBP und TFIIB, um ihre RNA‑Polymerase an die richtige Startstelle auf der DNA zu führen. Das Team zeigte, dass VITF‑3 eine stark modifizierte Version dieses alten Duos ist. Anders als seine zellulären Verwandten bindet VITF‑3 jedoch alleine nicht an DNA. Stattdessen verhaken sich seine beiden Untereinheiten zu einem geschlossenen Ring, der gegenüber DNA inaktiv ist, solange die virale RNA‑Polymerase nicht vorhanden ist. Das war unerwartet, denn in den meisten Systemen bindet die TBP‑ähnliche Komponente zuerst an die Promotor‑DNA und rekrutiert dann die Polymerase; hier scheint der Virus die Reihenfolge der Ereignisse umprogrammiert zu haben.
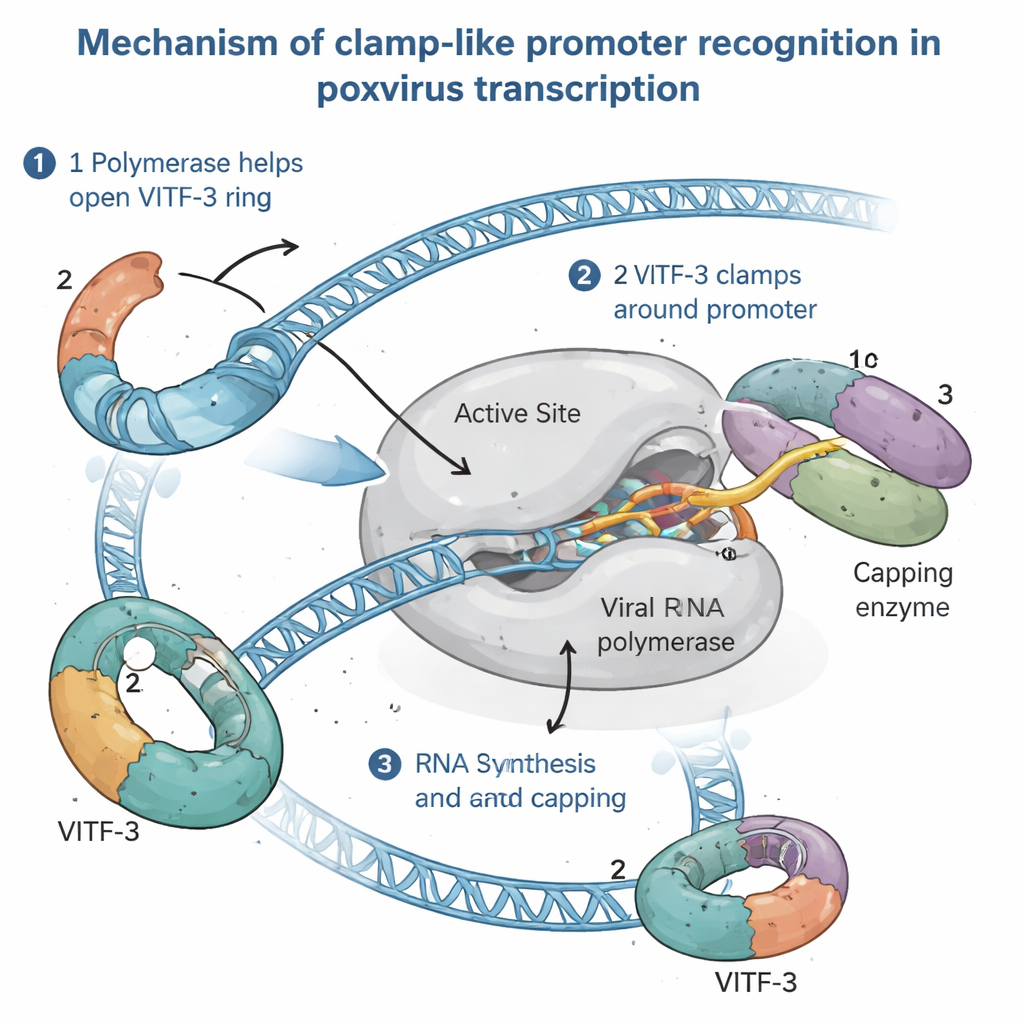
Die intermediäre Transkriptionsmaschine in Aktion sehen
Um zu verstehen, wie dieses ungewöhnliche System funktioniert, isolierten die Autoren den vollständigen intermediären Präinitiation‑Komplex — die Assemblierung kurz bevor die RNA‑Synthese beginnt — aus infizierten menschlichen Zellen. Mittels hochauflösender Kryo‑Elektronenmikroskopie visualisierten sie den Komplex bei etwa 2,4 Ångström Auflösung, fein genug, um Seitenketten von Aminosäuren und einzelne DNA‑Basen zu erkennen. Die Bilder zeigten die virale RNA‑Polymerase, die die Promotor‑DNA umfasst, während VITF‑3 einen engen Ring um eine AT‑reiche DNA‑Region direkt stromaufwärts der Startstelle bildet. Dieser Ring knickt die DNA scharf um etwa 90 Grad und führt sie in eine Spalte der Polymerase. Gleichzeitig ist ein virales Kappenzym — zuständig für das Anfügen der schützenden Kappe an das 5′‑Ende viraler RNA — an die Polymerase angedockt und bereit, neue Transkripte sofort nach ihrem Austritt zu modifizieren.
Ein in der Idee entlehner Klammer‑Lade‑Mechanismus
Durch die Kombination struktureller Momentaufnahmen mit biochemischen Tests schlägt die Studie vor, dass die virale RNA‑Polymerase aktiv VITF‑3 auf die DNA lädt und dabei wie ein „Klammer‑Lader“ wirkt. Zunächst bindet die Polymerase an einen intermediären Promotor und hilft, den VITF‑3‑Ring aufzubrechen. Dann schließt sie gemeinsam mit dem Kappenzym den Ring um die AT‑reiche Region, sodass das Komplex an Ort und Stelle geklammert wird. Die DNA wird in der Nähe der Startstelle geöffnet, und die Polymerase liest direkt ein kurzes vierbuchstabiges Signal (ein TAAA‑Motiv), das genau markiert, wo die RNA‑Synthese beginnen soll. Während die RNA wächst, folgt sie demselben Pfad, den ein Teil von VITF‑3 im Anfangskomplex einnahm, sodass die entstehende RNA wahrscheinlich VITF‑3 aus dem Weg schiebt und der Polymerase erlaubt, den Promotor zu verlassen und weiter entlang des Gens zu arbeiten, während VITF‑3 möglicherweise zurückbleibt, um die erneute Nutzung desselben Promotors zu beschleunigen.
Was das für das Verständnis und die Bekämpfung von Poxviren bedeutet
Einfach ausgedrückt zeigt diese Arbeit, dass das Vaccinia‑Virus ein universelles Genkontrollmodul zu einer Klammer umfunktioniert hat, die die DNA nur dann umgreift, wenn seine eigene RNA‑Polymerase es anweist. Dieser clevere Trick erlaubt es dem Virus, mit einem Kernenzym drei sehr unterschiedliche Transkriptionsprogramme zu betreiben, allein durch den Austausch stadiumsspezifischer Helfer. Da dieselben Faktoren in vielen Poxviren, einschließlich humaner Krankheitserreger, konserviert sind, bieten der neu aufgedeckte Klammer‑Lade‑Mechanismus und der einzigartige VITF‑3‑Ring konkrete strukturelle Angriffspunkte für antivirale Strategien, die darauf abzielen, die Fähigkeit des Virus zu stören, seine Gene während der Infektion zeitlich zu steuern und zu kontrollieren.
Zitation: Jungwirth, S., Bartuli, J., Lamer, S. et al. Cooperative clamp-mediated promoter recognition by poxviral RNA polymerase and its TBP/TFIIB-like partner. Nat Commun 17, 1648 (2026). https://doi.org/10.1038/s41467-026-69571-1
Schlüsselwörter: Transkription von Poxviren, Vaccinia‑Virus, RNA‑Polymerase, Promotorerkennung, Transkriptionsfaktoren