Clear Sky Science · de
Phosphoglycerat-Dehydrogenase-vermittelte Serin‑Umschaltung verschärft Makrophagen‑Hyperinflammation in einer murinen Pseudomonas aeruginosa‑Pneumonie
Wenn die Verteidiger des Körpers über die Stränge schlagen
Eine von Pseudomonas aeruginosa verursachte Pneumonie ist berüchtigt schwer zu behandeln, besonders bei Menschen mit vorgeschädigten Lungen. Antibiotika richten sich gegen den Erreger, doch diese Krankheit ist oft nicht nur wegen der Bakterien tödlich, sondern weil die körpereigene Immunantwort außer Kontrolle geraten kann. Diese Studie zeigt, wie ein einziger metabolischer „Schalter“ in Immunzellen sie von hilfreich zu schädlich umschalten kann — und legt nahe, dass eine gezielte Beeinflussung von Ernährung oder Zellstoffwechsel lebensbedrohliche Lungenentzündungen dämpfen könnte.
Ein gefährlicher Tanz zwischen Erreger und Immunsystem
Pseudomonas aeruginosa ist ein häufiges gramnegatives Bakterium, das in die unteren Atemwege eindringen und schwere Pneumonien auslösen kann. Normalerweise patrouillieren im Lungengewebe ansässige Immunzellen, die Makrophagen, in den Lungenbläschen, fressen Eindringlinge auf und schlagen mit chemischen Signalen Alarm. Bei hoher bakterieller Last rekrutieren diese Zellen jedoch große Zahlen zusätzlicher Makrophagen aus dem Blutkreislauf. Das kann zu einem Sturm entzündlicher Botenstoffe führen, der das fragile Lungengewebe schädigt, Reparaturprozesse behindert und in schweren Fällen zu Atemversagen und Tod führt. Die Autoren fragten, ob der interne Stoffwechsel dieser Makrophagen diese schädliche Überreaktion antreiben könnte.
Ein Stoffwechselenzym im Fokus
Das Team konzentrierte sich auf ein Enzym namens Phosphoglycerat‑Dehydrogenase (PHGDH), einen wichtigen Einstiegspunkt in den Weg, mit dem Zellen die Aminosäure Serin aus Glukose herstellen. In Mausmodellen einer Pseudomonas‑Lungeninfektion stiegen PHGDH‑Spiegel und ‑Aktivität in der Lunge deutlich an, besonders in Makrophagen. Wurden Mäuse mit einem kleinen Molekül‑Inhibitor von PHGDH behandelt oder das PHGDH‑Gen spezifisch in myeloiden Zellen (zu denen Makrophagen gehören) ausgeschaltet, erholten sich die Tiere besser: Sie überlebten länger, zeigten weniger Lungenschäden, hatten geringere Bakterienzahlen und produzierten geringere Mengen potenter entzündlicher Zytokine wie Interleukin‑6 und Interleukin‑1β. Auf zellulärer Ebene verschob die Blockade von PHGDH Makrophagen aus einem stark pro‑inflammatorischen Zustand, ohne gleichzeitig den gegensätzlichen, wunde‑heilenden Phänotyp zu verstärken.
Den Brand schüren: Serin und ein überaktiver Signalkreislauf
Tiefer gehend zeigten die Forschenden, dass die Infektion Makrophagen so umprogrammiert, dass mehr Glukose in die Neusynthese von Serin geleitet wird, und dass dieses Serin wiederum die Entzündung verschlimmert. Zusätzliches Serin veranlasste Makrophagen, mehr entzündliche Zytokine freizusetzen und mehr Aktivierungsmarker auf der Oberfläche zu exprimieren, während serinreduzierte Diäten infizierte Mäuse schützten und die Bakterienlast senkten. Mechanistisch floss Serin in den sogenannten Ein-Kohlenstoff‑Stoffwechsel, der methylgruppenliefernde Stoffwechselwege versorgt, also chemische Marken, die in der epigenetischen Regulation verwendet werden. Das verstärkte eine spezifische Histonmodifikation, H3K27‑Trimethylierung, in der Nähe des Gens für ein dämpfendes Protein namens DUSP4, das normalerweise hilft, den ERK1/2‑Signalweg auszuschalten. Wurde DUSP4 unterdrückt, blieb ERK1/2 aktiv und verstärkte entzündliche Signale. Die Hemmung von PHGDH oder die Reduktion von Serin kehrte diese Kaskade um, stellte DUSP4 wieder her und reduzierte die Phosphorylierung von ERK1/2.
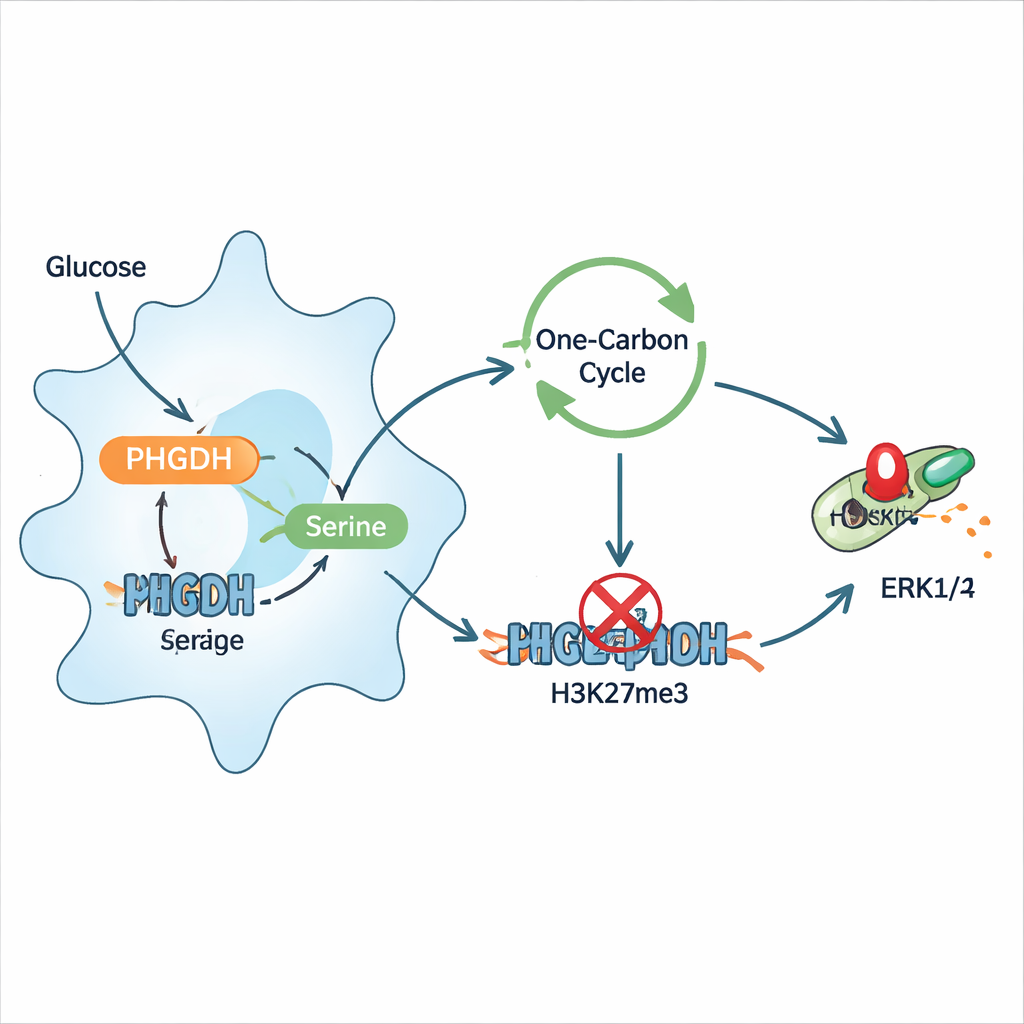
Makrophagen neu justieren, ohne die Abwehr zu schwächen
Wichtig ist, dass das Herunterregeln von PHGDH das Immunsystem nicht einfach lähmte. Tatsächlich waren Makrophagen ohne PHGDH früh nach der Infektion besser darin, Pseudomonas aufzunehmen und abzutöten, während sie gleichzeitig weniger schädliche Zytokine produzierten. Die Übertragung dieser PHGDH‑defizienten Makrophagen in normale Mäuse verbesserte die Ergebnisse nach bakterieller Herausforderung und unterstreicht, dass der Nutzen aus der Umprogrammierung der Wirtsantwort und nicht aus einem direkten Angriff auf den Erreger resultierte. Die Arbeit deutet außerdem an, dass serinreiche Diäten unbeabsichtigt Hyperinflammation bei schwerer bakterieller Pneumonie begünstigen könnten, während kontrollierte Serinreduktion einen neuen Weg bieten könnte, exzessive Lungenschädigung zu zähmen.
Was das für die Behandlung schwer zu heilender Pneumonien bedeutet
Anschaulich zeigt diese Studie, dass manche Makrophagen bei Pseudomonas‑Pneumonie Zucker so verstoffwechseln, dass sie zusätzliches Serin produzieren, und dass dieser metabolische Umweg ihre entzündliche Maschinerie dauerhaft überaktiviert. Durch Blockade des Enzyms PHGDH oder Begrenzung von Serin konnten die Forschenden diese Überreaktion dämpfen, Lungengewebe schützen und dennoch die bakterielle Eliminierung durch Immunzellen ermöglichen. Obwohl die Arbeit an Mäusen durchgeführt wurde und weit von einer klinischen Anwendung entfernt ist, weist sie auf eine vielversprechende Idee hin: Die Kombination traditioneller Antibiotika mit Medikamenten oder diätetischen Maßnahmen, die den Stoffwechsel von Immunzellen fein modulieren, könnte ein zerstörerisches immunologisches Feuer in eine kontrollierte, bakterienbekämpfende Flamme verwandeln.
Zitation: Chen, R., Zeng, R., Shi, M. et al. Phosphoglycerate dehydrogenase-mediated serine reprogramming aggravates macrophage hyperinflammation in murine Pseudomonas aeruginosa pneumonia. Nat Commun 17, 1944 (2026). https://doi.org/10.1038/s41467-026-69539-1
Schlüsselwörter: Pseudomonas‑Pneumonie, Makrophagenstoffwechsel, Serinbiosynthese, Lungenentzündung, PHGDH