Clear Sky Science · de
Ustilago maydis stört Kohlenhydrat‑Signalnetzwerke, um Hypertrophie in Wirtszellen auszulösen
Wenn Pflanzenkrankheiten Zellen in „Tumoren“ verwandeln
Mais ist eine der weltweit wichtigsten Nutzpflanzen für Nahrung und Futter — und hat einen ungewöhnlichen Gegner: den Brandpilz Ustilago maydis, der geschwollene, tumorähnliche Wucherungen auf Blättern und Kolben verursacht. Über das markante Erscheinungsbild hinaus lenken diese Wucherungen stillschweigend die Zucker der Pflanze von normalem Wachstum und Abwehrmechanismen hin zum Vorteil des Pilzes um. Diese Studie zeigt, wie ein einziges Pilzprotein die inneren Energieschalter der Pflanze umlegt und gewöhnliche Blattzellen in aufgequollene, mit Stärke gefüllte Fabriken verwandelt, die den Erreger versorgen.
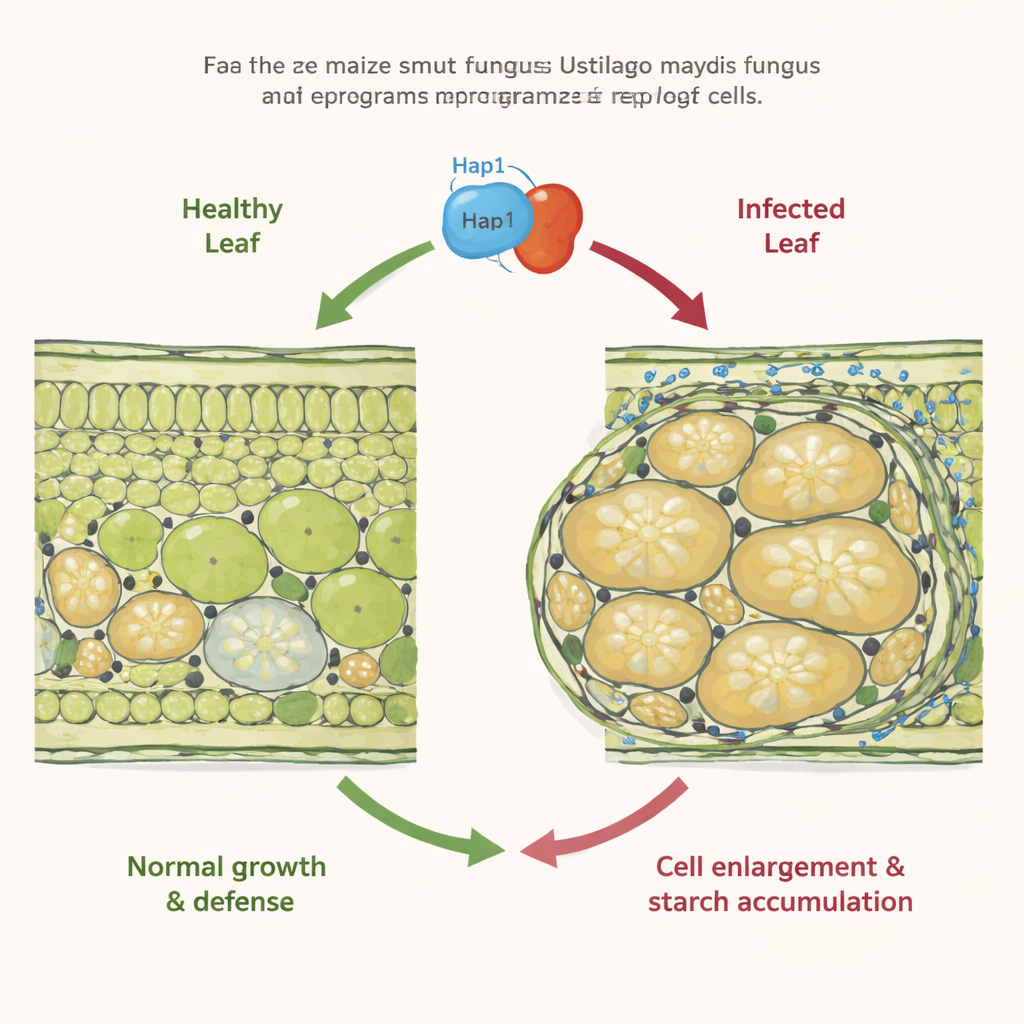
Ein Pilz, der Pflanzenwachstum umverdrahtet
Die meisten Brandpilze breiten sich unauffällig in Getreide aus und deformieren vor allem die Blüten. Ustilago maydis unterscheidet sich: Er kann lokale Tumoren an nahezu jedem oberirdischen Teil des Maises bilden. Frühere Arbeiten zeigten, dass in infizierten Blättern einige Zellen übermäßig oft teilen (Hyperplasie), während benachbarte Mesophyllzellen, die normalerweise die Photosynthese übernehmen, stattdessen dramatisch anschwellen (Hypertrophie) und die Teilung einstellen. Diese hypertrophischen Zellen füllen sich außerdem mit Stärkekörnchen an Stellen, an denen C4‑Pflanzen wie Mais üblicherweise keine Stärke speichern. Die molekularen Auslöser dieser extremen Zellvergrößerung und Zuckeranhäufung waren jedoch unbekannt.
Den pilzlichen Auslöser für Zellschwellung finden
Die Forschenden konzentrierten sich auf pilzliche „Effektor“proteine — in das Pflanzengewebe sezernierte Moleküle, die die Wirtsbiologie umgestalten. Aus einer Liste von Effektoren, die speziell in hypertrophischen Tumorzellen aktiv sind, setzten sie CRISPR‑Cas9 ein, um mehrere Kandidatengene in U. maydis auszuschalten. Ein Gen, UMAG_02473, hob sich hervor: Mutanten ohne dieses Gen verursachten deutlich weniger Tumoren und zeigten Pflanzenzellen mit kleineren Zellkernen und deutlich weniger Stärke im Blattmesophyll. Da vergrößerte Zellkerne ein Kennzeichen von Endoreduplication sind — Zellen, die ihre DNA ohne Teilung verdoppeln — schlossen die Autoren, dass dieser Effektor, den sie Hap1 (hypertrophy‑associated protein 1) nannten, entscheidend dafür ist, Mesophyllzellen in ein Programm von Wachstum ohne Teilung zu drängen und die Stärkezunahme zu fördern.
Die Energiesteuerung der Pflanze kapern
Um zu verstehen, wie Hap1 den Maisstoffwechsel umgestaltet, suchten die Wissenschaftler nach seinen pflanzlichen Zielmolekülen. Sie zeigten, dass Hap1 in Wirtszellen eingeschleust wird und sich sowohl im Cytoplasma als auch im Zellkern anreichert. Mit Protein‑Pull‑downs und Massenspektrometrie stellten sie fest, dass Hap1 an das Maisprotein SnRK1 bindet, einen zentralen Energiesensor, der normalerweise auf Stress und Energiemangel reagiert, indem er zuckerfreisetzende Wege aktiviert, energieaufwändige Synthesen (wie die Stärkebildung) drosselt und Abwehrantworten stärkt. Weitere Tests bestätigten, dass Hap1 physisch mit den katalytischen Untereinheiten von SnRK1 interagiert. In Gegenwart von Hap1 änderten sich Phosphorylierungsmuster an SnRK1‑Komponenten und bekannten SnRK1‑Zielproteinen, und ein direkter Kinase‑Assay zeigte, dass Hap1 die Fähigkeit von SnRK1, ein Standardsubstrat zu phosphorylieren, abschwächt. Kurz gesagt: Hap1 greift in das energetische „Thermostat“ der Pflanze ein und schwächt ihre übliche Reaktion auf Stress und Nährstoffknappheit.
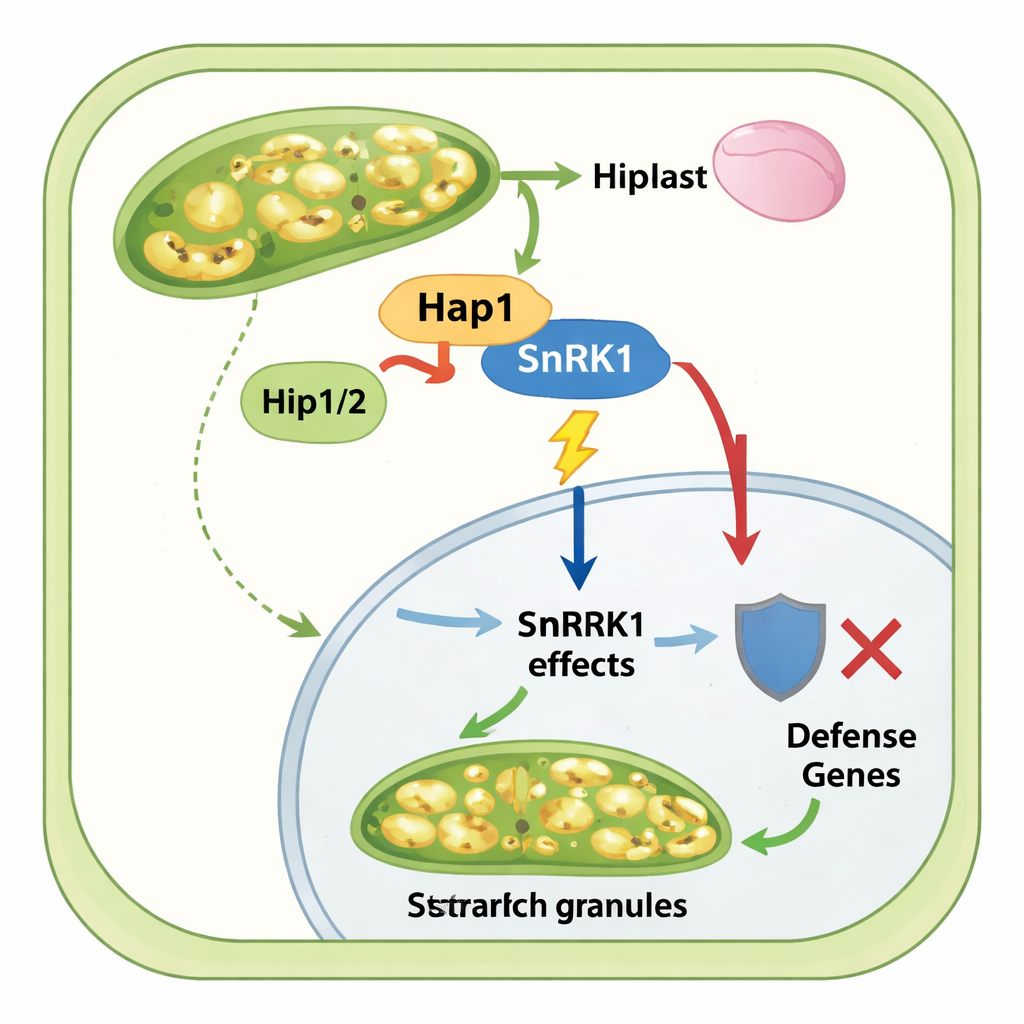
Hilfseffektoren und eine zuckerreiche Tumorumgebung
Die Geschichte endet nicht mit Hap1 allein. Das Team entdeckte zwei zusätzliche pilzliche Effektorproteine, Hip1 und Hip2, die spezifisch mit Hap1 interagieren und ebenfalls in hypertrophischen Tumorzellen exprimiert werden. Obwohl das Entfernen dieser Helfer nur begrenzte Auswirkungen auf die allgemeine Krankheitsschwere hatte, zeigten biochemische Experimente, dass Hip1 und Hip2 sowohl an Hap1 als auch an den SnRK1‑Komplex binden, helfen, Hap1‑Proteinspiegel aufrechtzuerhalten, und erforderlich sind, damit Hap1 SnRK1 effizient aus infiziertem Maisgewebe herausziehen kann. Phosphoproteomik und Genexpressionsdaten zusammen zeigten, dass in Anwesenheit von Hap1 Mais‑Tumoren Gene und Enzyme der Stärkesynthese hochregulieren, während Gene, die mit Pflanzenabwehr und normaler Proteinbiosynthese verbunden sind, gedämpft werden. Ohne Hap1 sinkt die Stärkeanhäufung im Mesophyll stark ab und Stress‑ sowie Abwehrsignalwege werden aktiver.
Was das für Mais und seine Abwehr bedeutet
Aus Sicht der Allgemeinheit zeigt diese Arbeit, dass Ustilago maydis nicht nur durch Gewebeschädigung erfolgreich ist, sondern durch geschicktes Manipulieren der inneren Energiesteuerung der Pflanze. Der Hap1‑Effektor, gestützt von seinen Partnern Hip1 und Hip2, scheint die Funktion von SnRK1 zu dämpfen — ein wichtiger Wächter, der normalerweise Energie spart und Immunabwehr unterstützt. Mit diesem Schutz geschwächt, hören Mais‑Mesophyllzellen auf, wie normale grüne Fabriken zu funktionieren: sie schwellen an, kopieren ihre DNA ohne Teilung und horten Stärke. Diese tumorähnlichen Zellen werden zu nährstoffreichen Inseln, die den Pilz ernähren. Das Verständnis dieser Pilzstrategie eröffnet Wege, Maislinien zu züchten oder gentechnisch so zu verändern, dass SnRK1 oder verwandte Wege weniger verwundbar sind und damit Tumor bildende Infektionen besser abgewehrt werden können, ohne das Pflanzenwachstum zu opfern.
Zitation: Lee, Y.J., Zhang, D., Stolze, S.C. et al. Ustilago maydis disrupts carbohydrate signaling networks to induce hypertrophy in host cells. Nat Commun 17, 1990 (2026). https://doi.org/10.1038/s41467-026-69532-8
Schlüsselwörter: Maisbrand, Pflanzenimmunität, fungale Effektorproteine, Stoffwechsel von Stärke, SnRK1‑Signalgebung