Clear Sky Science · de
Eine synthetische Zelle mit integrierter DNA-Selbstdublikation und Lipidsynthese
Lebensentstehung von Grund auf
Was macht eine lebende Zelle mehr als nur einen Beutel voller Moleküle? Eine Antwort liegt in ihrer Fähigkeit, ihre genetischen Anweisungen zu kopieren und ihre eigene Schutzmembran zu bauen. Diese Studie macht einen großen Schritt, um dieses Kunststück im Labor nachzubilden. Die Autoren entwerfen winzige Fettbläschen, sogenannte Liposomen, die ein DNA-Stück lesen, diese DNA kopieren und neues Membranmaterial herstellen können — alles innerhalb desselben winzigen Kompartiments. Ihre Arbeit rückt uns näher an künstliche Zellen, die wachsen, sich anpassen und vielleicht eines Tages selbst evolvieren können.
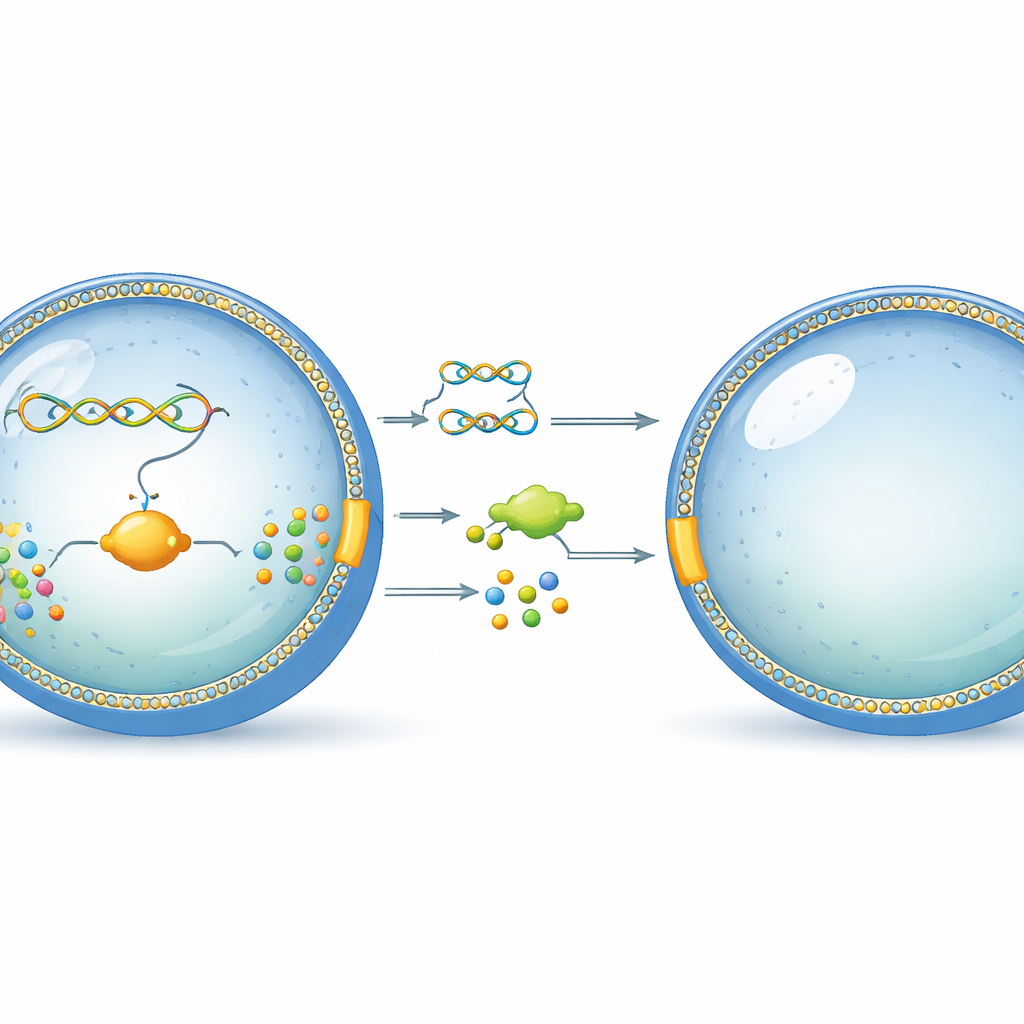
Eine winzige Blase, die sich wie eine Zelle verhält
Die Forschenden starten mit einfachen, zellgroßen Blasen aus Phospholipiden, derselben Molekülklasse, die die Außenschicht echter Zellen bildet. In diese Blasen packen sie eine sorgfältig gestaltete DNA-Strang und eine Reihe gereinigter zellulärer Maschinen, die DNA lesen und Proteine herstellen können. Dieses System, ein zellfreies Expressionssystem genannt, wirkt wie der abgespeckte Kern einer lebenden Zelle und kann genetische Information in funktionale Moleküle übersetzen, ohne dass ein lebender Organismus vorhanden ist. Die Schlüsselidee ist, alles innerhalb des Liposoms zu platzieren, sodass das genetische Programm und seine Produkte zusammenbleiben — ähnlich wie in einer natürlichen Zelle.
Ein maßgeschneidertes DNA-Programm mit zwei Aufgaben
Im Zentrum ihrer synthetischen Zelle steht ein kundenspezifisches DNA-Molekül, das die Autoren DNArep-PLsyn nennen. Diese DNA trägt die Bauanleitung für sechs Proteine. Zwei davon stammen von einem Virus, das Bakterien infiziert, und sind gemeinsam in der Lage, die DNA selbst zu kopieren und damit ein eingebautes Selbstreplikationsmodul bereitzustellen. Die anderen vier stammen von dem Darmbakterium E. coli und bilden eine Reaktionskette, die einfache Ausgangsstoffe in ein spezifisches Phospholipid für Membranen umwandelt. Um dieses ungewöhnliche Genom zusammenzubauen, musste das Team DNA-Stücke in Reagenzgläsern und in Hefezellen aneinanderfügen und das Ergebnis anschließend in einen linearen DNA-Strang umwandeln, den die virale Kopiermaschinerie erkennen und replizieren kann.
Herstellen und Testen synthetischer Aktivität
Sobald die DNA und die Proteinsynthesemaschinerie im Liposom eingeschlossen sind, werden die Blasen auf verschiedene Temperaturen erwärmt und laufen gelassen. Das Team überprüft das Ergebnis mit fluoreszierenden Markern: Ein Farbstoff leuchtet, wenn er an DNA bindet und zeigt so die vorhandene DNA-Menge an, ein anderer bindet an das neue Phospholipid, falls dieses produziert und in die Membran eingebaut wird. Mit Durchflusszytometrie und hochauflösender Mikroskopie können sie zehntausende einzelne Vesikel analysieren. Sie stellen fest, dass viele Blasen das Genom erfolgreich kopieren, viele andere neue Membranbausteine herstellen und ein kleinerer, aber signifikanter Anteil beides gleichzeitig schafft. Zusätzliche Tests mittels DNA-Quantifizierung und Massenspektrometrie bestätigen, dass das vollständige Genom amplifiziert wird und dass neue Phospholipidmoleküle tatsächlich synthetisiert werden, wenn auch in moderaten Mengen.
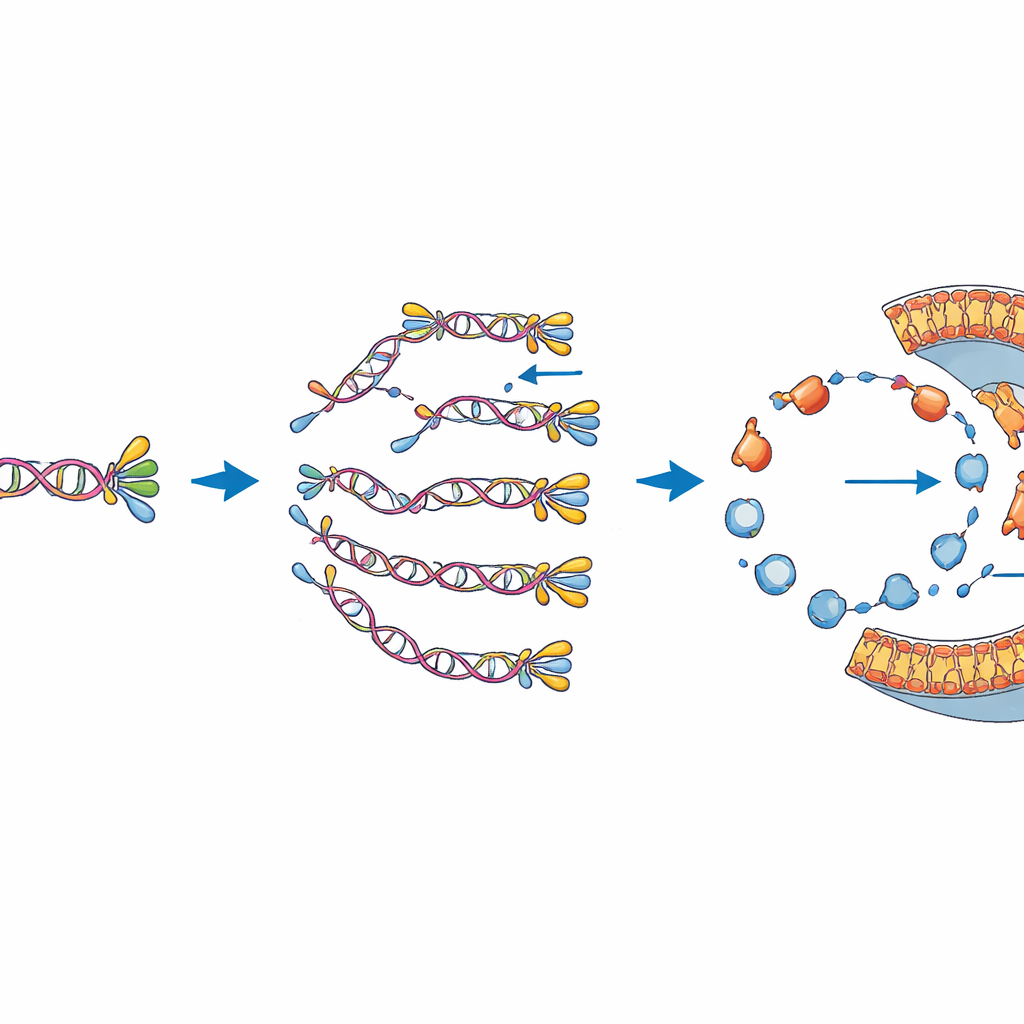
Das Gleichgewicht zwischen zwei essentiellen Aufgaben
Die Autoren untersuchen anschließend, wie diese beiden Funktionen sich gegenseitig beeinflussen. Indem sie die DNA-Kopier- oder Membranbildungschemie durch das Vorhandensein oder Fehlen der benötigten Zutaten ein- und ausschalten, zeigen sie, dass jeder Prozess weitgehend arbeiten kann, ohne den anderen zu stören. Wenn jedoch beide Module auf derselben DNA kodiert sind, erweist sich die Membransynthese als empfindlicher: Weniger Vesikel zeigen diese Aktivität im Vergleich zu Vesikeln, die nur die lipidbezogenen Gene tragen. Ähnlich wird das kombinierte Genom nicht so effizient kopiert wie eine kleinere Version, die nur die DNA-Replikationsgene enthält. Das legt nahe, dass selbst in diesem reduzierten System Ressourcen und physischer Platz auf der DNA umkämpft sind — ein Echo der Zielkonflikte, die auch in echten Zellen beobachtet werden.
Vorbereitung auf Evolution im Reagenzglas
Um über eine einmalige Demonstration hinauszukommen, entwirft das Team ihr System so, dass es prinzipiell durch Evolution verbessert werden kann. Sie erzeugen sauberere, zuverlässigere DNA-Versionen mithilfe von Plasmiden, die in Hefe und Bakterien gezüchtet werden, was den Anteil voll funktionsfähiger synthetischer Zellen erhöht. Außerdem zeigen sie, dass es möglich ist, Genome aus Vesikeln, die sowohl DNA-Kopie als auch Membransynthese leisten, zu verkapseln, auszuwählen und wieder zurückzugewinnen. Das bereitet den Boden für zukünftige Zyklen, in denen leicht unterschiedliche Genome konkurrieren und diejenigen, die besser funktionieren, angereichert und kopiert werden.
Warum das wichtig ist für das Verständnis von Leben
Alltäglich gesprochen haben die Forschenden eine mikroskopische Blase gebaut, die ihr eigenes Rezept lesen, mehr Kopien dieses Rezepts herstellen und es nutzen kann, um ihre äußere Haut zu flicken und zu erweitern. Obwohl diese synthetischen Zellen sich noch nicht wie lebende Organismen vergrößern oder teilen können, zeigt die Arbeit, dass Kernmerkmale des Lebens — Informationsspeicherung, Selbstkopie und grundlegende Selbstkonstruktion — in einem einfachen, kontrollierbaren Paket kombiniert werden können. Das legt wichtige Grundlagen dafür, zu erforschen, wie Leben aus unbelebter Chemie entstanden sein könnte und wie man künstliche Zellen entwickelt, die nützliche Aufgaben erfüllen, von intelligenten Wirkstoffabgabesystemen bis hin zu sich selbst erneuernden winzigen Fabriken.
Zitation: Restrepo Sierra, A.M., Ramirez Gomez, F., van Tongeren, M. et al. A synthetic cell with integrated DNA self-replication and lipid biosynthesis. Nat Commun 17, 2727 (2026). https://doi.org/10.1038/s41467-026-69531-9
Schlüsselwörter: synthetische Zellen, DNA-Selbstdublikation, Lipidsynthese, künstliches Leben, Bottom-up-Biologie