Clear Sky Science · de
FOXF2 reguliert die Perizyten–Endothel-Signalübertragung, die für die Gefäßhomöostase nach neonataler hyperoxischer Lungenschädigung erforderlich ist
Warum die Lungen Neugeborener besonders geschützt werden müssen
Bei zu früh geborenen Babys fällt das Atmen oft schwer. Viele benötigen zur Versorgung zusätzliches Sauerstoff, aber diese lebensrettende Therapie kann zugleich die empfindlichen Lungen und Blutgefäße schädigen und so zu einer chronischen Erkrankung, der bronchopulmonalen Dysplasie, beitragen. Diese Studie untersucht eine wenig beachtete Gruppe von Stütz-Zellen, die winzige Lungengefäße umhüllen, und entdeckt einen wichtigen genetischen Schalter, der diesen Zellen hilft, die Neugeborenenlunge nach einer Sauerstoffschädigung zu schützen und zu reparieren.
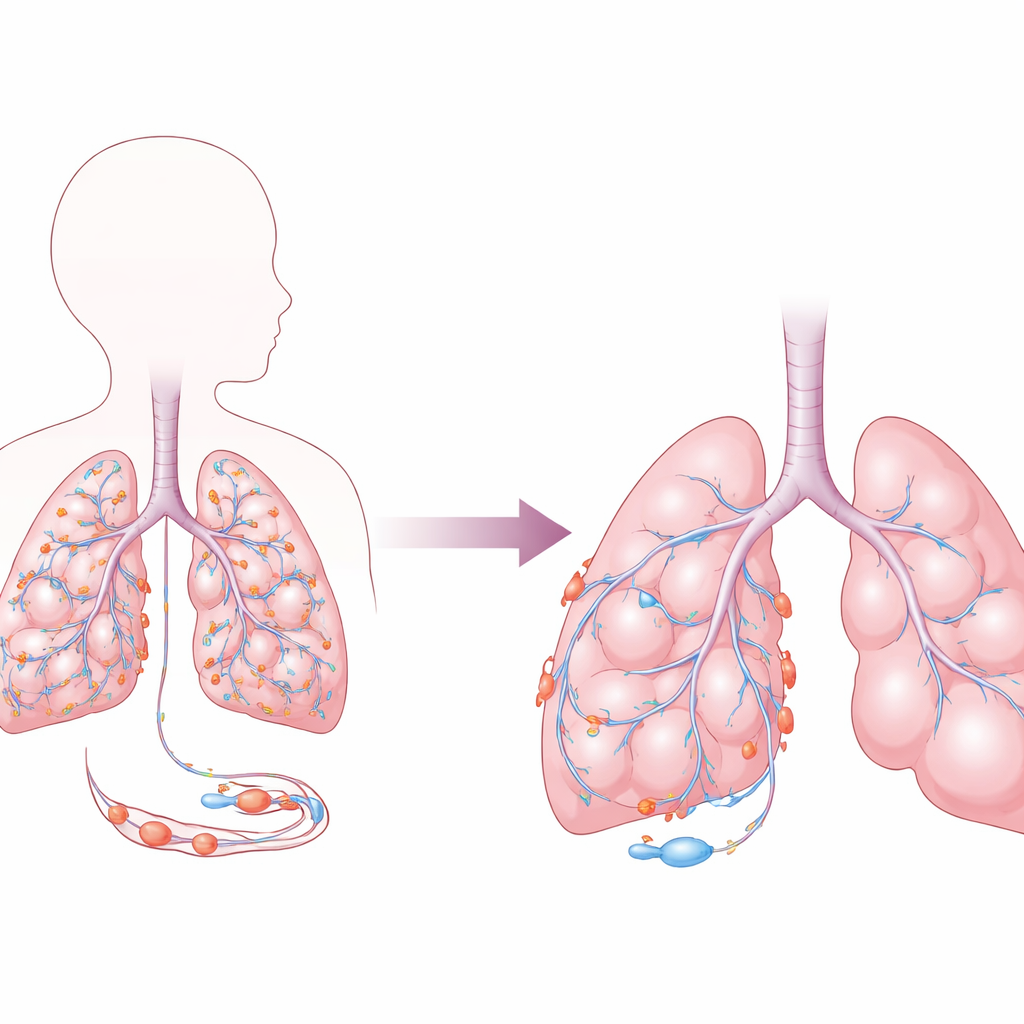
Die verborgenen Helfer rund um Lungengefäße
Die Luftsäcke in der Lunge, in denen Sauerstoff ins Blut übergeht, sind von einem dichten Kapillarnetz durchzogen. Viele dieser Kapillaren sind von Perizyten umgeben, Stützzellen, die Gefäße stabilisieren, das Wachstum neuer Gefäße lenken und eine dichte Barriere aufrechterhalten, damit keine Flüssigkeit in die Lufträume austritt. Die Autoren konzentrierten sich auf ein Gen namens FOXF2, einen Transkriptionsfaktor, der steuert, welche Gene in Perizyten an- oder abgeschaltet werden. Anhand von Einzelzell‑RNA-Daten aus sich entwickelnden Mauslungen fanden sie, dass die Foxf2-Aktivität in Perizyten nach der Geburt ansteigt – parallel zu Genen, die mit Perizytenreife, Gefäßentwicklung und Zellmigration verknüpft sind. Dagegen ist seine Aktivität in anderen benachbarten Zelltypen deutlich geringer, was auf eine spezialisierte Rolle in diesen vaskulären Stützzellen hindeutet.
Wenn die Bremse für Perizyten wegfällt
Um zu prüfen, was FOXF2 tatsächlich bewirkt, erzeugte das Team Mäuse, bei denen Foxf2 gezielt in PDGFRβ-positiven Perizyten kurz nach der Geburt gelöscht werden konnte. Unter normalen Sauerstoffbedingungen wirkten die allgemeine Lungenstruktur und die Blutsauerstoffwerte weitgehend normal, doch die Details zeichneten ein anderes Bild. Perizyten vermehrten sich übermäßig und lagen dicht gepackt um die Kapillaren, während Marker für reife, gut funktionierende Perizyten abnahmen. Diese Perizyten befanden sich häufiger in der DNA-Synthesephase des Zellzyklus, und Versuche an kultivierten Perizyten bestätigten, dass das Blockieren von Foxf2 ihre Proliferation fördert und ihre Migration reduziert. Gleichzeitig wurden Gene, die normalerweise das Gefäßwachstum und die Stabilität unterstützen, wie Angptl4 und Angpt2, herunterreguliert, während Gene für Zellteilung und Energieproduktion hochgefahren wurden. Zusammen ergibt das das Bild vieler, aber weniger kompetenter Perizyten.
Sauerstoffstress legt eine kritische Schwäche offen
Die Konsequenzen wurden weitaus ernster, als die neugeborenen Mäuse hohen Sauerstoffkonzentrationen ausgesetzt wurden, einem Standardmodell für frühkindliche Lungenschädigung. Sowohl in Mauslungen als auch in menschlichen Proben von Säuglingen mit bronchopulmonaler Dysplasie war FOXF2 in Perizyten nach einer solchen Schädigung deutlich reduziert. Bei hyperoxischen Bedingungen sank die Überlebensrate der Foxf2-defizienten Mäuse stark, die Blutsauerstoffsättigung fiel, und die Luftsäcke vergrößerten und vereinfachten sich – ein Zeichen mangelhafter Alveolarentwicklung. Gleichzeitig nahm die Kapillarabdeckung in den Alveolen ab, Endothelzellen teilten sich weniger und mehr fluoreszenter Tracer trat aus den Blutgefäßen in das Lungengewebe über – ein Hinweis auf eine versagende Gefäßbarriere. Die Durchflusszytometrie bestätigte, dass unter Schädigung die Endothelzellzahlen abnahmen, während Perizyten weiter zunahmen und hoch proliferativ blieben, was einen Zusammenbruch der normalen Partnerschaft zwischen diesen beiden Zelltypen unterstreicht.
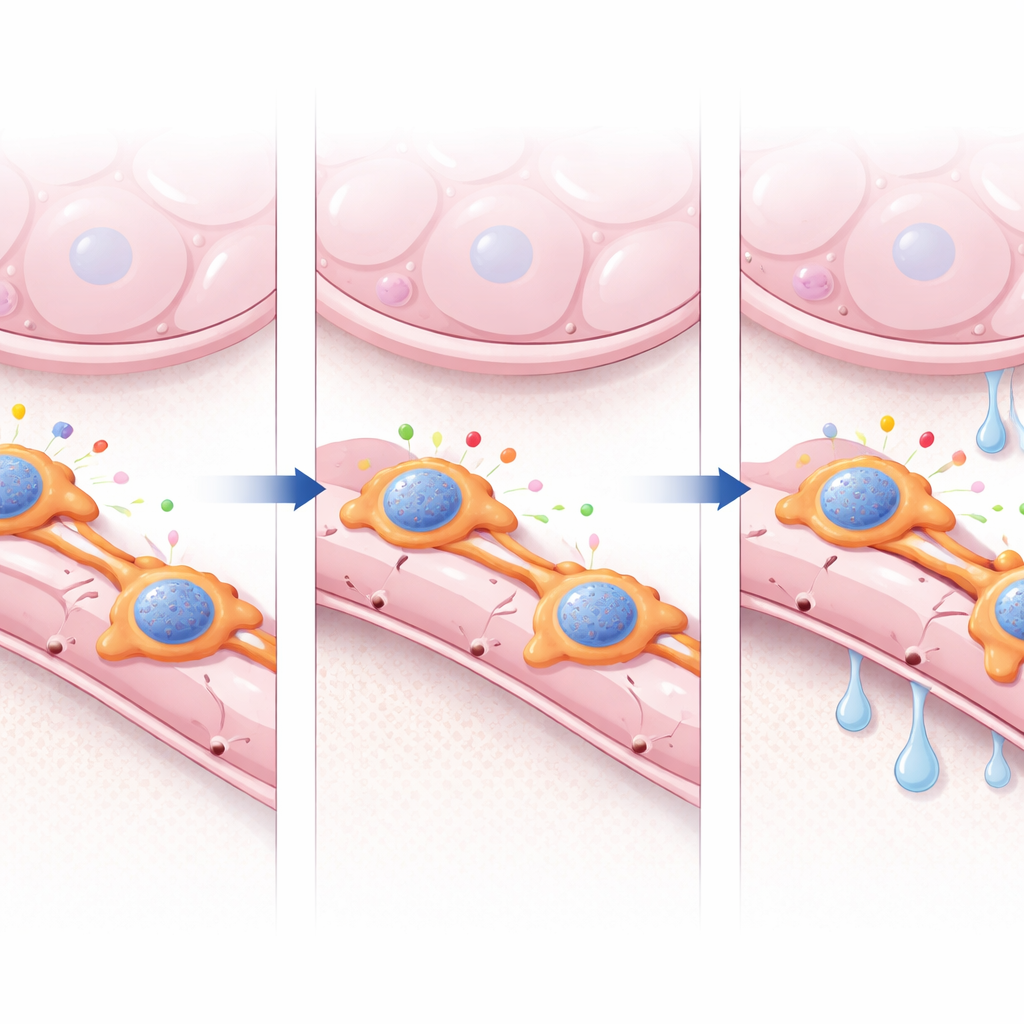
Wie Perizyten‑Signale die Gefäßreparatur formen
Um die molekulare Kommunikation genauer zu untersuchen, nutzten die Forscher rechnerische Werkzeuge, um Signalwege zwischen Perizyten und Endothelzellen zu kartieren. In gesunden Lungen waren Wege, die Gefäßwachstum und Stabilität fördern, prominent, darunter solche mit ANGPTL4, einem sezernierten Protein mit pro‑angiogenen und barriemodulierenden Eigenschaften. In Foxf2-defizienten Lungen schwächten sich diese hilfreichen Signale, während Stress‑ und Entzündungswege zunahmen. Konditionierte Medien von Perizyten ohne Foxf2 unterstützten die Röhrenbildung menschlicher Lungenendothelzellen in Kultur weniger gut, doch die Zugabe von rekombinantem ANGPTL4 verbesserte diesen Defekt teilweise – ein Hinweis auf eine FOXF2–ANGPTL4‑Achse als entscheidenden Reparaturtreiber. Chromatin‑Profiling zeigte weiter, dass FOXF2 in der Nähe vieler pro‑angiogener Gene bindet und deren umgebende DNA‑Regionen offen hält. Beim Verlust von FOXF2 nahm die Zugänglichkeit an Tausenden solcher Stellen ab, einschließlich des Angptl4‑Locus, was darauf hindeutet, dass FOXF2 als Chromatin‑Organisator wirkt und anderen Faktoren ermöglicht, ein gesundes Perizytenprogramm aufrechtzuerhalten.
Was das für empfindliche Neugeborenenlungen bedeutet
Insgesamt zeigen die Ergebnisse, dass FOXF2 als Masterregulator wirkt, der neonatale Lungenperizyten reif hält, ihr Wachstum bremst und sie befähigt, die richtigen Signale an benachbarte Endothelzellen zu senden. Fällt FOXF2 nach einer Sauerstoffschädigung ab, werden Perizyten überzählig, aber dysfunktional: Sie schicken weniger nährende Botenstoffe wie ANGPTL4, Kapillaren regenerieren nicht richtig, Gefäßwände werden undicht und die Architektur der Luftsäcke verschlechtert sich. Für Familien und Kliniker, die Frühgeborene betreuen, hebt diese Arbeit Perizyten – und die von FOXF2 gesteuerten Gennetzwerke in ihnen – als vielversprechende Ziele für künftige Therapien hervor, mit denen sich feine Blutgefäße schützen, der Gasaustausch verbessern und langfristige Lungenschäden nach frühzeitiger Sauerstoffexposition verringern lassen.
Zitation: Sun, F., Zhao, Y., Do, J. et al. FOXF2 regulates pericyte–endothelial signaling required for vascular homeostasis after neonatal hyperoxic lung injury. Nat Commun 17, 2691 (2026). https://doi.org/10.1038/s41467-026-69525-7
Schlüsselwörter: bronchopulmonale Dysplasie, Lungenentwicklung, Perizyten, Angiogenese, neonatale Hyperoxie