Clear Sky Science · de
Laser-interstitielle Thermotherapie und adjuvantes Pembrolizumab bei rezidivierendem hochgradigem Astrozytom: eine Phase‑1/ randomisierte Phase‑2b‑Studie
Warum diese Studie zu Hirnkrebs wichtig ist
Rezidivierendes hochgradiges Astrozytom, einschließlich Glioblastom, gehört zu den tödlichsten Hirntumoren, und die etablierten Therapien halten die Erkrankung selten über längere Zeit unter Kontrolle. Diese Studie prüft eine zweistufige Strategie: Zuerst wird Hitze aus einem Laser genutzt, um Tumorgewebe zu zerstören und die Barrieren des Gehirns zu öffnen, anschließend wird ein Immunmedikament eingesetzt, das die körpereigenen T‑Zellen dabei unterstützt, verbleibende Krebszellen anzugreifen. Für Patientinnen und Patienten sowie ihre Familien, die mit dieser Diagnose konfrontiert sind, untersucht die Arbeit, ob ein minimalinvasiver Eingriff einen fast nicht ansprechbaren Tumor in einen verwandeln kann, der auf Immuntherapie reagiert.
Ein neuer Weg, hartnäckige Hirntumoren anzugehen
Die Teilnehmenden dieser Studie litten alle an hochgradigen Astrozytomen, die nach Standardtherapie—häufig Operation, Bestrahlung und Chemotherapie—wieder aufgetreten waren. Die Forschenden konzentrierten sich auf zwei Mittel. Erstens: die laserinterstitielle Thermotherapie (LITT), ein Schlüssellochverfahren, bei dem eine dünne Sonde unter MRT‑Kontrolle in den Tumor geführt wird und diesen erhitzt, um Krebsgewebe zu vernichten, während ein Großteil des umliegenden Gehirns geschont wird. Zweitens: Pembrolizumab, ein weit verwendetes Immuntherapeutikum, das PD‑1 blockiert, eine molekulare „Bremse“, die T‑Zellen oft daran hindert, Tumore anzugreifen. Frühere Versuche, solche Wirkstoffe allein bei diesen Hirntumoren einzusetzen, waren enttäuschend. Das Team fragte daher, ob der Laser zuerst den Tumor und das Immunsystem so vorbereiten kann, dass auf Pembrolizumab besser reagiert wird. 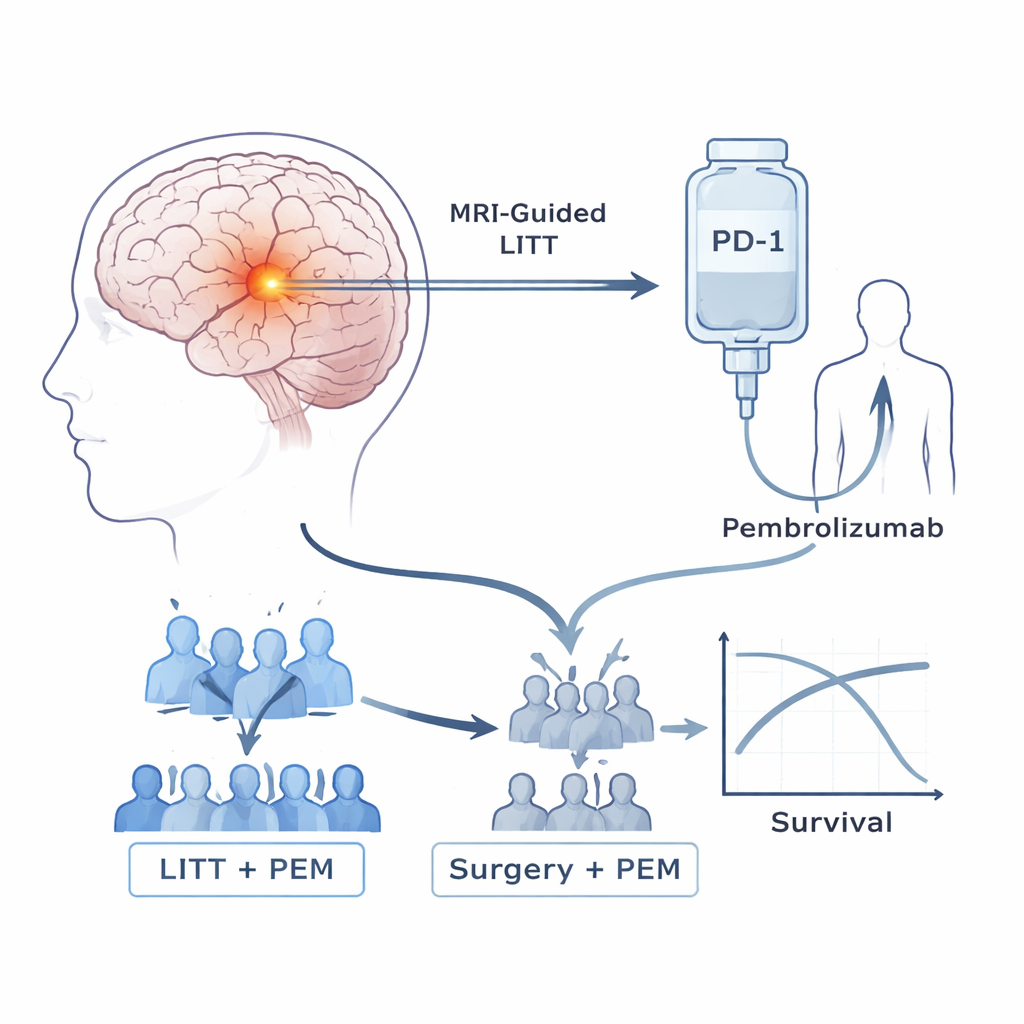
Wie die klinische Studie durchgeführt wurde
Die Untersuchung begann mit einer kleinen Sicherheitsphase, die zeigte, dass Patientinnen und Patienten nach LITT alle drei Wochen sicher Pembrolizumab erhalten konnten, ohne dosislimitierende Nebenwirkungen. Anschließend ging es in eine Phase‑2b‑Studie. Zunächst wurden die Teilnehmenden randomisiert einer von zwei Gruppen zugeordnet: LITT gefolgt von Pembrolizumab oder eine konventionelle wiederholte Hirnoperation ohne Laser, gefolgt von Pembrolizumab. Als außerhalb der Studie mehr Hinweise darauf auftauchten, dass Operation plus Immuntherapie allein wenig Nutzen brachte, prüfte ein unabhängiges Gremium frühe Ergebnisse dieser Studie. Da sich zeigte, dass die Nicht‑Laser‑Gruppe schlechter abschnitt, während die LITT‑Gruppe offenbar länger lebte, beendete man die weitere Randomisierung, und alle späteren Patientinnen und Patienten erhielten die Kombination aus Laser und Medikament.
Was mit Überleben und Tumorkontrolle geschah
Unter 39 Patientinnen und Patienten, die wie geplant behandelt wurden, lebten diejenigen, die LITT plus Pembrolizumab erhielten, deutlich länger als die, die eine Operation plus Pembrolizumab hatten. Das mediane Gesamtüberleben betrug mit dem kombinierten LITT‑Ansatz etwa 11,8 Monate gegenüber 5,2 Monaten unter der Operation allein; keiner der Operierten war bei 18 Monaten mehr am Leben im Vergleich zu 42 % der LITT‑Gruppe. Auch die Zeit bis zum erneuten Tumorwachstum verbesserte sich von 1,6 Monaten in der OP‑Gruppe auf 4,5 Monate mit LITT. Etwa 27 % der mit LITT behandelten Patienten zeigten eine messbare Tumorverkleinerung, und 70 % erreichten zumindest vorübergehende Krankheitskontrolle, während alle Patienten, die eine nicht‑Laser‑Operation plus Pembrolizumab erhielten, Progression erlebten. Nebenwirkungen der kombinierten Behandlung waren überwiegend mild und handhabbar, mit einigen Fällen von Durchfall, Muskelschwäche und erhöhten Leberwerten, aber keinen therapiebedingten Todesfällen.
Was das Immunsystem tat
Um zu verstehen, warum die Kombination wirken könnte, untersuchten die Forschenden Blutzellen über die Zeit mithilfe von Einzelzell‑RNA‑Sequenzierung und T‑Zell‑Rezeptor‑Verfolgung genau. Nach LITT beobachteten sie, dass eine spezifische Gruppe angeborener Immunzellen, sogenannte nicht‑klassische Monozyten, in einen aktiveren Zustand wechselte, der mit Migration, Entzündung und Interaktion mit T‑Zellen assoziiert ist—Veränderungen, die nach einer Standardoperation nicht zu sehen waren. Mit Beginn von Pembrolizumab zeigten Patientinnen und Patienten mit längerem Überleben starke Wellen der CD8‑T‑Zell‑Aktivierung und klonaler Expansion, das heißt viele identische T‑Zellen, die dieselben Antigene anvisieren, vermehrten sich. Diese T‑Zellen neigten dazu, in Gedächtnis‑ und Effektorzustände überzugehen, die Tumorzellen erkennen und abtöten können, statt erschöpft und wirkungslos zu werden. Langzeitüberlebende zeigten zudem einen Rückgang von IDO‑1, einem Molekül, das mit Immunsuppression einhergeht, was darauf hindeutet, dass die Kombination mehrere Ebenen immunologischer Bremsen lösen könnte. 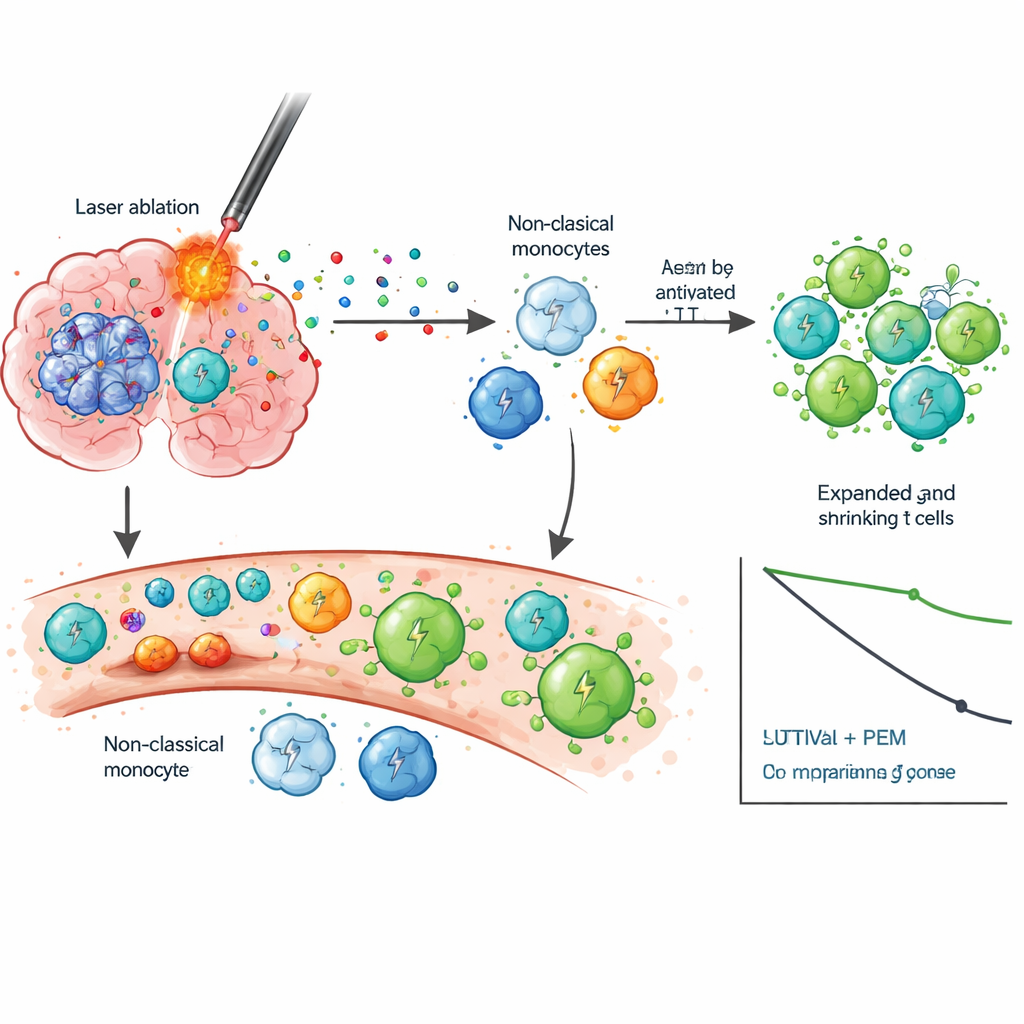
Was das für Patientinnen und Patienten bedeuten könnte
Für Menschen mit rezidivierendem hochgradigem Astrozytom legt diese Arbeit nahe, dass eine MRT‑gesteuerte Laserablation zur Volumenreduktion des Tumors, zur kurzzeitigen Lockerung der Blut‑Hirn‑Schranke und zum Freisetzen von Tumorfragmenten in den Kreislauf das Terrain so vorbereiten kann, dass Immuntherapie dort wirkt, wo sie normalerweise versagt. Indem ein „Signalfeuer“ für das Immunsystem entzündet und anschließend die PD‑1‑Bremse mit Pembrolizumab gelöst wird, scheint die Kombination robustere T‑Zell‑Antworten zu erzeugen und das Überleben in einem Krankheitsbild mit wenigen Optionen zu verlängern. Da die Studie relativ klein war und die Randomisierung früh beendet wurde, betonen die Autoren, dass größere, vollständig kontrollierte Studien weiterhin nötig sind. Dennoch weisen die Ergebnisse auf eine vielversprechende neue Strategie hin: gezielt physische Tumorzerstörung und Immunmedikamente zu koppeln, um einen kalten, resistenten Hirntumor in einen zu verwandeln, den der Körper endlich erkennt und bekämpft.
Zitation: Campian, J.L., Le, S.B., Ghiaseddin, A. et al. Laser interstitial thermal therapy and adjuvant pembrolizumab in recurrent high-grade astrocytoma: a Phase 1/randomized Phase 2b trial. Nat Commun 17, 1763 (2026). https://doi.org/10.1038/s41467-026-69522-w
Schlüsselwörter: Glioblastom, Laserablation, Pembrolizumab, Immuntherapie, Hirntumor