Clear Sky Science · de
Übermäßige FGFR3-Signalisierung bei Achondroplasie stört den Umsatz der Ruheschicht-Chondrozyten über CREB-Signalgebung
Warum diese Studie zum Knochenwachstum wichtig ist
Achondroplasie ist die häufigste genetische Ursache für Kleinwuchs mit verkürzten Gliedmaßen. Sie betrifft nicht nur die Körpergröße, sondern auch die Wirbelsäule, Mobilität und Lebensqualität. Bestehende Behandlungen helfen, stellen aber das Knochenwachstum nicht vollständig wieder her. Diese Studie verwendet ein ausgefeiltes Mausmodell, um eine bislang wenig beachtete Problemzone in wachsenden Knochen aufzudecken, und identifiziert einen neuen Signalgeber, genannt CREB, als vielversprechendes Ziel für künftige Therapien.
Wie gesunde Knochen an Länge gewinnen
Lange Knochen, etwa der Oberschenkelknochen, wachsen an Wachstumsfugen nahe ihren Enden. Diese Wachstumsfugen sind in drei Hauptschichten von Knorpelzellen organisiert. Oben liegt die Ruheschicht, in der die Zellen wie ein Stammzellpool langsam teilen und Tochterzellen nach unten schicken. Darunter enthält die proliferative Zone schnell teilende Zellen, die in geordneten Säulen angeordnet sind und das Längenwachstum vorantreiben. Am weitesten entwickelt ist die hypertrophe Zone mit vergrößerten, reifen Zellen, die die Bildung neuen Knochens unterstützen. Das Gleichgewicht zwischen diesen Zonen sorgt dafür, dass Knochen mit der richtigen Geschwindigkeit und Form wachsen.
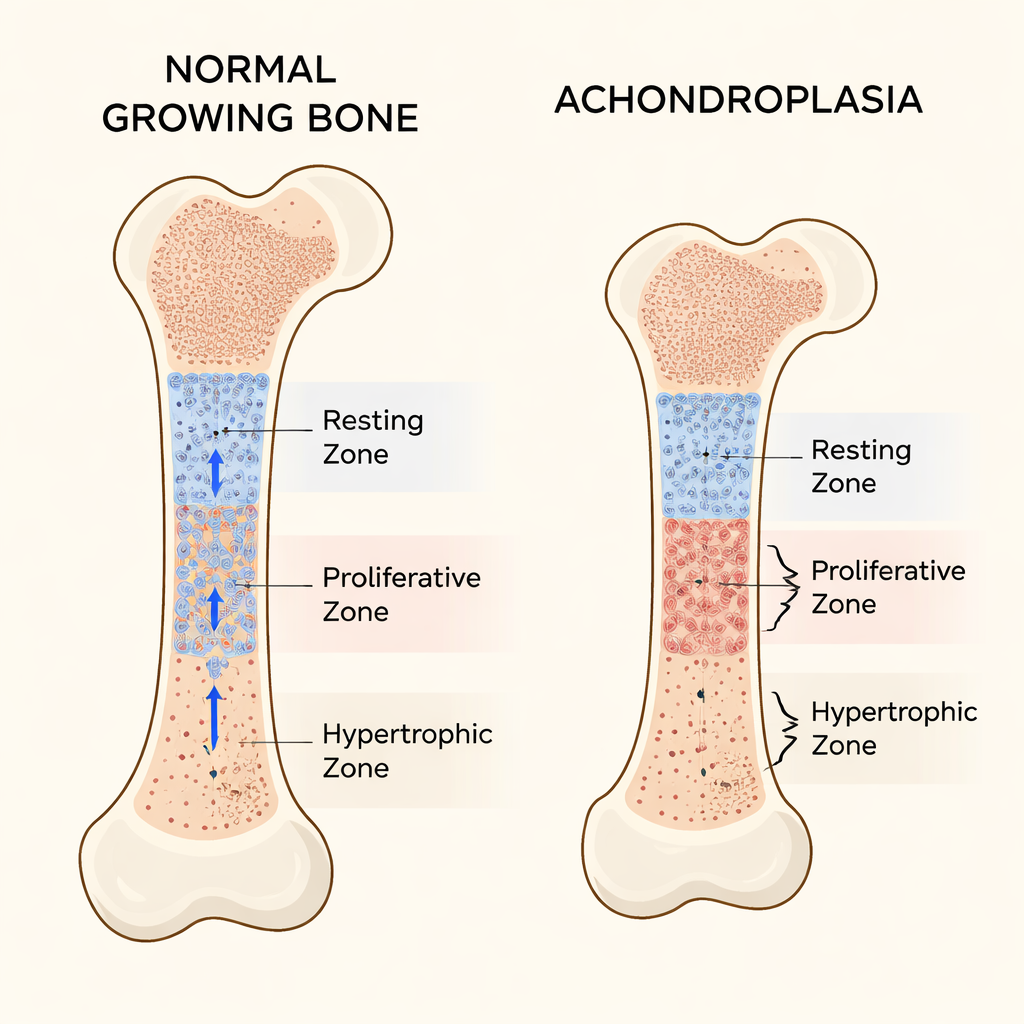
Was bei Achondroplasie schiefgeht
Bei den meisten Menschen mit Achondroplasie führt eine einzelne Mutation im FGFR3-Gen dazu, dass sein Rezeptor überaktiv ist und das Knochenwachstum bremst. Frühere Arbeiten zeigten, dass diese Signalgebung die Zellteilung in der proliferativen Zone verlangsamt und die abschließende Vergrößerung der Zellen in der hypertrophen Zone blockiert. Die Autoren bestätigten mit Mäusen, die die menschliche Achondroplasie-Mutation tragen, stark verkürzte Gliedmaßen und verkürzte Wachstumsfugen. Detaillierte Messungen enthüllten jedoch etwas, das weitgehend übersehen worden war: Die Ruheschicht wurde ungewöhnlich dick. Statt als stabiler, gut funktionierender Stammzellpool zu fungieren, weitete sich diese Region aus und enthielt Zellen mit geringem Gehalt an gewöhnlicher Knorpelmatrix.
Ruheschicht-Zellen verlieren ihr „stammzellähnliches“ Verhalten
Um diese Ausdehnung zu verstehen, verfolgte das Team, wie sich Wachstumsfugen-Zellen über die Zeit teilten und bewegten. Bei normalen Mäusen teilten sich Ruheschicht-Zellen selten, und ihre Nachkommen wanderten in geraden Säulen nach unten, um die proliferative Zone aufzufüllen. In den Mutanten teilten sich deutlich mehr Zellen in der Ruheschicht langsam und blieben an Ort und Stelle, wodurch eine überfüllte Schicht entstand, die die unteren Zonen nicht richtig speiste. Linienverfolgung mit mehrfarbigen genetischen Markern zeigte, dass klonale Säulen kurz und unordentlich waren und Tochterzellen in zufällige Richtungen abwichen, anstatt ordentliche Stapel zu bilden. Marker stammzellähnlicher Identität, wie das Protein CD73, gingen in der erweiterten Ruheschicht verloren, was darauf hindeutet, dass überaktive FGFR3 die normale Stammzellnische beschädigt hatte.
Ein neuer Signalstörer: CREB
Die Forscher nutzten dann Einzelzell-RNA-Sequenzierung, um Tausende einzelner Wachstumsfugen-Zellen zu profilieren. Sie identifizierten einen eigenen Zellcluster, der zur erweiterten Ruheschicht passte und unter anderem reich an dem Gen Spon1 war. Die Analyse von Signalwegen hob die Aktivierung von CREB hervor, einem Protein, das Gene einschaltet, wenn es phosphoryliert ist. Mikroskopie zeigte, dass Ruheschicht-Zellen in den Mutanten stark aktiviertes CREB und dessen Co-Aktivator CBP exprimierten, zusammen mit hohen Mengen an FGFR3 und nachgeschalteten Molekülen wie STAT5. In Zellkultur erhöhte die Stimulierung des FGFR3-Wegs die CREB-Aktivität und steigerte SPONDIN1 (das SPON1-Protein), während die Blockade von FGFR3 oder CREB diese Signale verringerte. Damit steht CREB als zentrale Verbindung zwischen dem überaktiven Rezeptor an der Zelloberfläche und dem fehlerhaften Verhalten der Ruheschicht-Zellen.
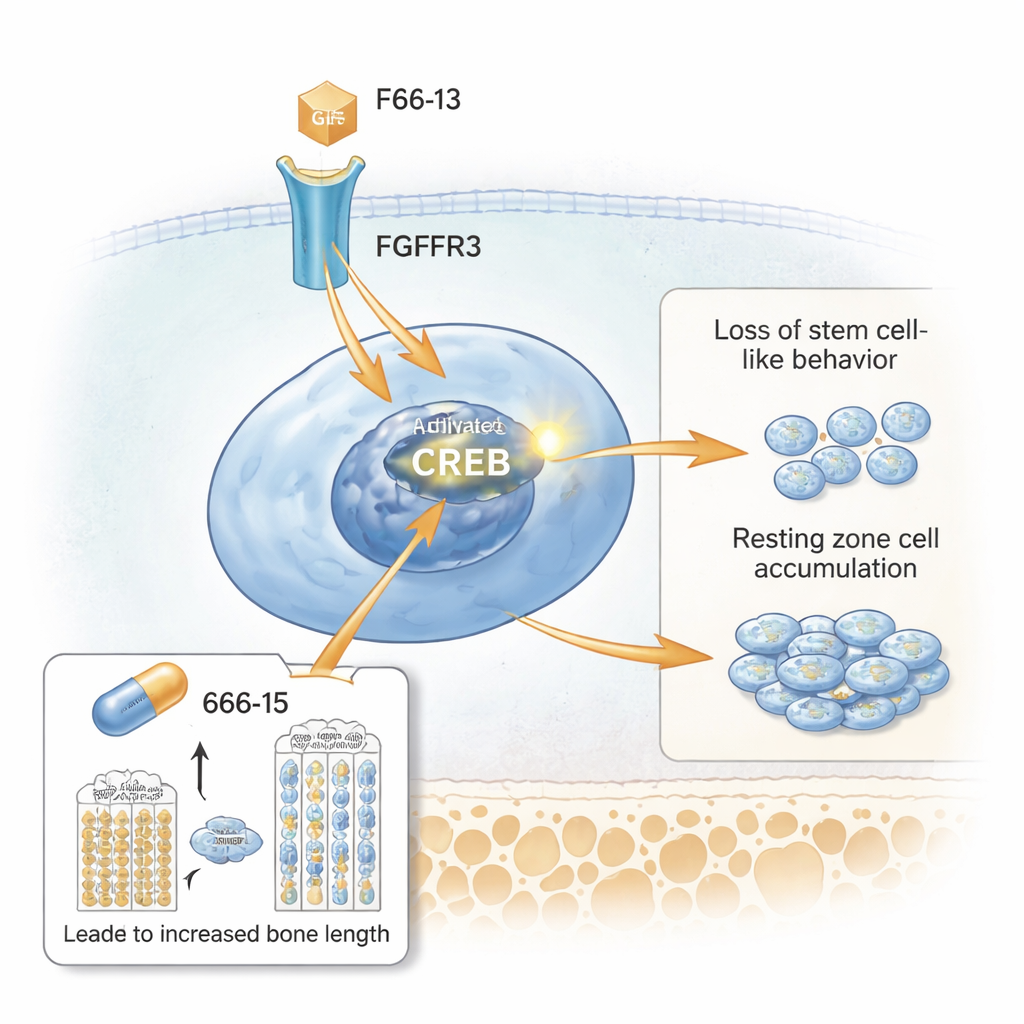
Test eines Wirkstoffs, der CREB dämpft
Schließlich untersuchten die Autoren, ob eine Reduktion von CREB die Wachstumsprobleme mildern könnte. Sie behandelten Achondroplasie-Modellmäuse während der schnellen Wachstumsphase nach der Geburt mit einem kleinen CREB-Inhibitor namens 666-15. Im Vergleich zu unbehandelten Mutanten hatten die mit 666-15 behandelten Tiere ein höheres Körpergewicht und längere Oberschenkelknochen. Ihre Wachstumsfugen wirkten normaler: Die Ruheschicht wurde dünner, die proliferative und hypertrophe Zone erholten sich in der Höhe, und Knorpelmatrixproteine traten wieder auf. Marker überaktiver CREB-Signalgebung, einschließlich phospho-CREB, SPONDIN1 und STAT5, fielen in der Ruheschicht, während der stammzellähnliche Marker CD73 zurückkehrte. Wichtig ist, dass das gleiche Medikament bei gesunden Kontrollmäusen in der getesteten Dosis kaum Wirkung zeigte, was nahelegt, dass es vor allem dann wirkt, wenn CREB abnormal hoch ist.
Was das für künftige Behandlungen bedeutet
Die Studie zeigt, dass bei Achondroplasie überaktives FGFR3 mehr bewirkt als nur das Verlangsamen der Teilung und Vergrößerung von Zellen: Es bringt die ruhige, stammzellähnliche Ruheschicht durch Aktivierung von CREB aus dem Tritt. Diese Störung beraubt die unteren Wachstumsfugen-Schichten der notwendigen neuen Zellen und trägt so zu kurzen Knochen bei. Bestehende Medikamente wie Vosoritid zielen hauptsächlich auf andere Wege in der proliferativen und hypertrophen Zone und stellen die Knochenlänge nur teilweise wieder her. Indem CREB als weiteres Ziel – insbesondere in der Ruheschicht – hinzugefügt wird, könnten künftige Kombinationstherapien das Wachstum bei Kindern mit Achondroplasie umfassender normalisieren.
Zitation: Horike, N., Oura, S., Koyamatsu, S. et al. Excess FGFR3 signaling in achondroplasia disrupts turnover of resting zone chondrocytes via CREB signaling. Nat Commun 17, 1856 (2026). https://doi.org/10.1038/s41467-026-69507-9
Schlüsselwörter: Achondroplasie, FGFR3, Wachstumsfuge, Knorpelstammzellen, CREB-Signalgebung