Clear Sky Science · de
Hydrierte Metallladungsdichte als universeller Deskriptor zur Erklärung mechanistischer Unterschiede bei der Aktivierung von Periodat zur Schadstoffabbauung
Wasserreinigung mit intelligenter Chemie
Viele Arzneimittel und Industriechemikalien passieren konventionelle Wasseraufbereitungsanlagen und gelangen in Flüsse und Trinkwasser. Diese Studie untersucht einen vielversprechenden Weg, um solche hartnäckigen Schadstoffe mit einem verbreiteten Oxidationsmittel, Periodat, zu zersetzen, und zeigt, dass eine einfache Eigenschaft von Metallionen in Wasser vorhersagen kann, wie gut — und wie sicher — diese Chemie funktioniert. Das Verständnis dieser Regel könnte Ingenieuren helfen, sauberere und effizientere Aufbereitungssysteme für vielfältige reale Wasserqualitäten zu entwickeln.
Warum die Metallwahl für den Schadstoffabbau wichtig ist
Fortgeschrittene Oxidationsverfahren nutzen hochreaktive Spezies, um organische Moleküle zu zerstören. Periodat ist ein solches Oxidationsmittel und kann durch gelöste Metallionen „aktiviert“ werden. Die Autoren verglichen drei eng verwandte Metalle — Eisen, Ruthenium und Osmium — die zur selben Gruppe des Periodensystems gehören und daher ähnlich reagieren könnten. Alle drei können Periodat aktivieren und helfen, den Modellschadstoff Carbamazepin abzubauen. Experimente zeigten jedoch auffällige Unterschiede: Ruthenium wirkte extrem schnell, Eisen war langsamer und Osmium lag dazwischen. Noch rätselhafter war, dass Osmium eine breite Palette von Schadstoffen ohne starke Vorliebe entfernte, während Eisen und Ruthenium wählerisch waren und einige Verbindungen deutlich leichter angreifen als andere.
Zwei sehr unterschiedliche chemische Wege
Um die Ursache dieser Unterschiede zu klären, verfolgte das Team, welche kurzlebigen Oxidationsspezies in jedem Metall‑Periodat‑System auftraten. Bei Eisen und Ruthenium dominierten „Metall‑Sauerstoff“-Einheiten, die wie präzise Werkzeuge wirken und ein Sauerstoffatom direkt auf bestimmte Stellen eines Schadstoffs übertragen. Diese Wege führten tendenziell zu Epoxidprodukten — Ringstrukturen, die ein einzelnes Sauerstoffatom einfügen — und zeigten damit eine relativ hohe Selektivität. Im Osmium‑System dagegen waren die Hauptakteure Hydroxylradikale, extrem reaktive Fragmente, die nahezu jedes benachbarte organische Molekül angreifen und zu hydroxylierten Produkten und kleineren ringaufgebrochenen Fragmenten führen. Tests mit chemischen Sonden und Spin‑Trapping‑Spektroskopie bestätigten, dass Hydroxylradikale und verwandte reaktive Sauerstoffspezies — und nicht hochvalente Osmium‑Sauerstoff‑Einheiten — den größten Teil der Schadstoffzerstörung im Anwesenheit von Osmium antreiben.
Wie Wasserbedingungen die Reaktionen formen
Das Team untersuchte außerdem, wie pH‑Wert und natürliche Wasserbestandteile diese Prozesse beeinflussen. Bei Osmium verstärkte sich die Schadstoffentfernung, je alkalischer das Wasser wurde, da zusätzliche Hydroxid‑Liganden um das Metall die Elektronenbewegung erleichtern und die Bildung von Radikalen fördern. Bei hohen Metall‑ oder Oxidantendosen „löschte“ sich das Osmium‑System jedoch selbst aus, weil die neu gebildeten Radikale von überschüssigen Chemikalien statt von Schadstoffen abgefangen wurden. Natürliche organische Substanz, die Oxidationsprozesse oft stört, hatte überraschend geringen Einfluss auf die Osmium‑getriebene Zersetzung, was darauf hindeutet, dass der Radikalweg in realistischen Wässern robust bleibt. Im Gegensatz dazu arbeiteten Eisen und Ruthenium am besten unter sauren Bedingungen, und natürliche organische Substanz unterdrückte ihre Aktivität stark, indem sie die wichtigen Metall‑Sauerstoff‑Oxidanten auffing.
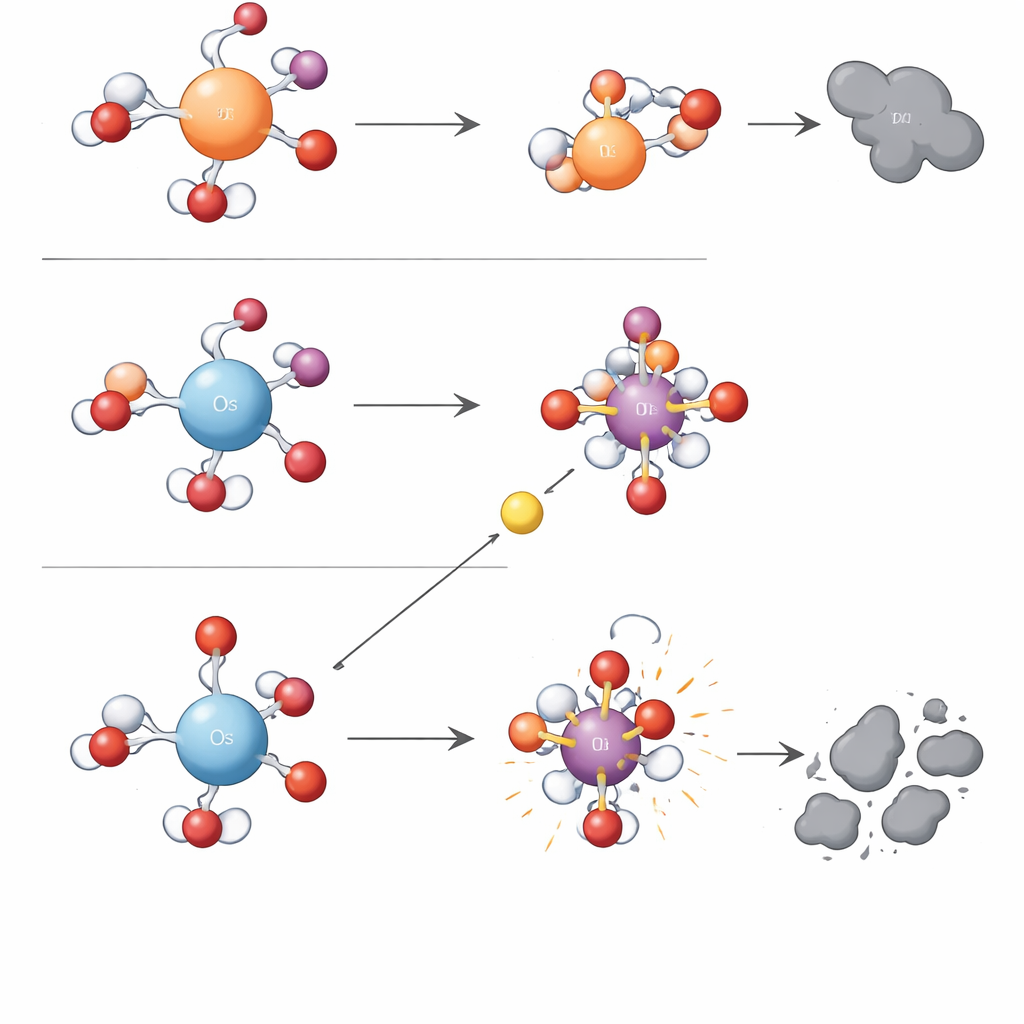
Eine einfache Ladungsregel hinter komplexer Chemie
Um über Trial‑and‑Error hinauszukommen, nutzten die Forschenden quantenchemische Rechnungen. Sie fanden, dass ein einziges elektronisches Merkmal — die positive Ladungsdichte des hydratisierten Metallzentrums — die Aufspaltung in die beiden Reaktionstypen erklären kann. Osmium im Wasser trägt eine höher konzentrierte positive Ladung als Eisen oder Ruthenium. Dieses starke positive Zentrum hält sein gebundenes Sauerstoffatom sehr fest, wodurch die Metall‑Sauerstoff‑Einheit stabil, aber träge gegenüber direktem Sauerstofftransfer wird. Gleichzeitig senkt die starke Anziehung auf benachbartes Wasser und Ionen die Aktivierungsbarriere für Ein‑Elektron‑Schritte, die letztlich eine Sauerstoffbindung im Periodat knacken und Hydroxylradikale freisetzen. Metalle mit niedrigerer Ladungsdichte, wie Eisen und Ruthenium, halten Elektronen stärker und begünstigen die Bildung und Nutzung der selektiven Metall‑Sauerstoff‑Oxidanten statt freier Radikale. Die Autoren nennen diese ordnende Idee den „Charge Density Control Mechanism“ und zeigen, dass sie auch Trends für andere Metalle wie Mangan rationalisiert.
Bessere Wasseraufbereitung mit einem einzigen Stellrad entwerfen
Indem sie eine schwierige Beobachtungsgruppe mit einem einfachen Deskriptor — der Ladungsdichte eines von Wasser umgebenen Metallzentrums — verknüpfen, liefert diese Arbeit eine Roadmap zur Anpassung fortgeschrittener Oxidationsverfahren. Metalle mit hoher Ladungsdichte sollten breit angelegten, radikalbasierten Abbau komplexer Schadstoffgemische begünstigen, insbesondere in alkalischen oder organisch reichen Wässern. Metalle mit niedrigerer Ladungsdichte eignen sich besser, wenn selektivere, schonendere Oxidation gewünscht ist, beispielsweise um spezifische Kontaminanten zu transformieren, ohne mit allem anderen überzureagieren. Praktisch bedeutet das, dass Chemiker und Ingenieure Katalysatoren für die Wasserreinigung durch Abstimmung der Ladungsbindung an Metallzentren in ihrer wässrigen Umgebung screenen oder entwerfen können, anstatt jedes System nur durch Versuch und Irrtum zu optimieren.
Zitation: Qian, Y., Sun, Y., Xu, J. et al. Hydrated metal charge density as a universal descriptor explaining mechanistic variations in periodate activation toward pollutant degradation. Nat Commun 17, 2683 (2026). https://doi.org/10.1038/s41467-026-69496-9
Schlüsselwörter: fortgeschrittene Oxidationsverfahren, Periodat‑Aktivierung, Wasseraufbereitung, Katalyse durch Übergangsmetalle, Hydroxylradikale